§ 46. Химические свойства, получение и применение аминов
Химические свойства насыщенных аминов
1. Оснóвные свойства
В молекулах аминов у атома азота имеется неподелённая электронная пара, поэтому они могут присоединять катион водорода H+: 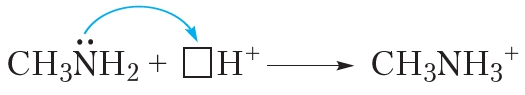
или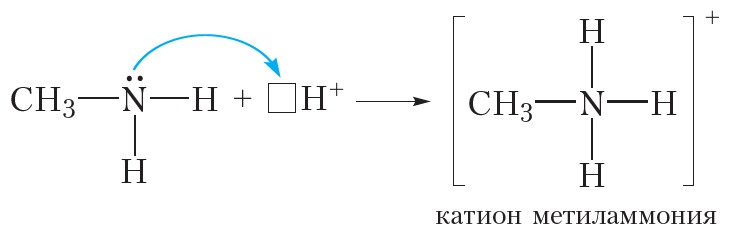
То есть так же, как и аммиак, амины обладают оснóвными свойствами.
Так, при растворении метиламина в воде протекает обратимая реакция:
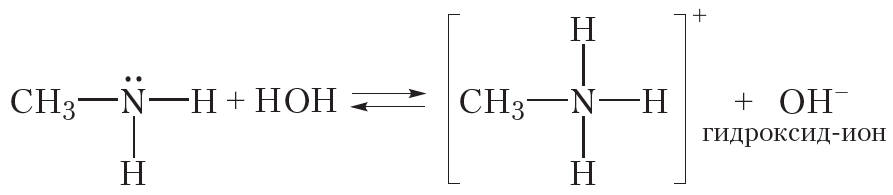
Видно, что при взаимодействии с водой молекула метиламина присоединяет катион водорода. При этом образуются ион метиламмония CH3NH3+ и гидроксид-ион OH–. Наличие ионов OH– обусловливает щелочную реакцию водного раствора метиламина, поэтому раствор метиламина в воде окрашивает фенолфталеин в малиновый цвет.
Оснóвные свойства аминов проявляются также в реакциях с кислотами. Например, при взаимодействии метиламина с соляной кислотой образуется соль — хлорид метиламмония:![]()
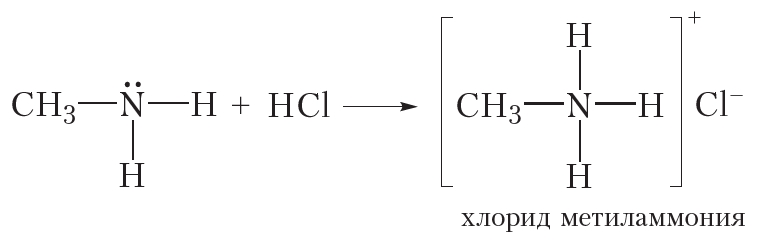
Как и все соли, хлорид метиламмония имеет ионное строение. Он состоит из катиона метиламмония и хлорид-аниона. Хлорид метиламмония — твёрдое, хорошо растворимое в воде вещество.
Аналогично протекают реакции метиламина и с другими кислотами:![]()
или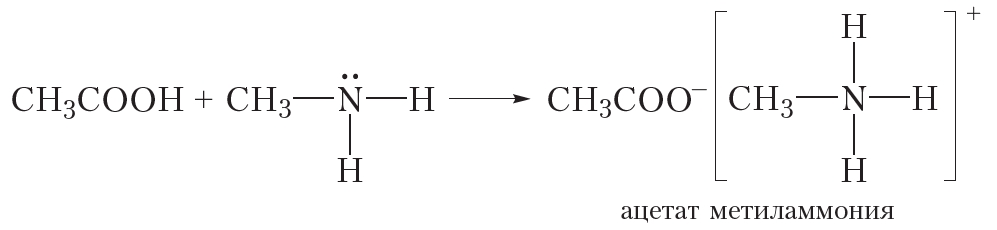
Эти реакции заключаются в присоединении катиона водорода H+ к молекуле метиламина.
Мы рассмотрели взаимодействие метиламина с водой и кислотами. Очевидно, подобным образом эти реакции будут протекать и для других аминов:![]()
или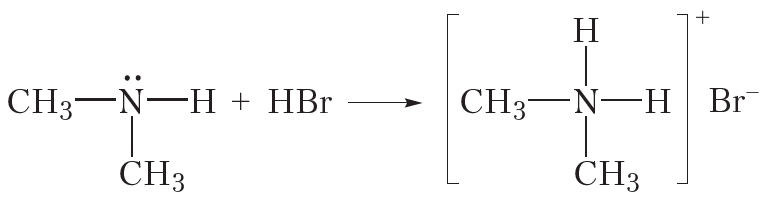 Соли аминов — твёрдые, хорошо растворимые в воде вещества. Щёлочи вытесняют амины из солей:
Соли аминов — твёрдые, хорошо растворимые в воде вещества. Щёлочи вытесняют амины из солей:
![]()
Подобную реакцию вы встречали при изучении неорганической химии, когда рассматривали вытеснение аммиака из солей аммония под действием щелочей.
2. Горение
Как и большинство органических соединений, амины горят в кислороде.
При этом образуются углекислый газ, вода и азот:
![]()