§ 46. Химические свойства, получение и применение аминов
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 46. Химические свойства, получение и применение аминов |
| Напечатано:: | Гость |
| Дата: | Monday, 4 May 2026, 02:17 |
Химические свойства насыщенных аминов
1. Оснóвные свойства
В молекулах аминов у атома азота имеется неподелённая электронная пара, поэтому они могут присоединять катион водорода H+: 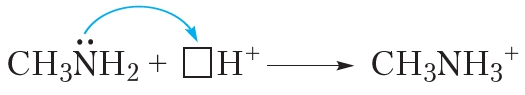
или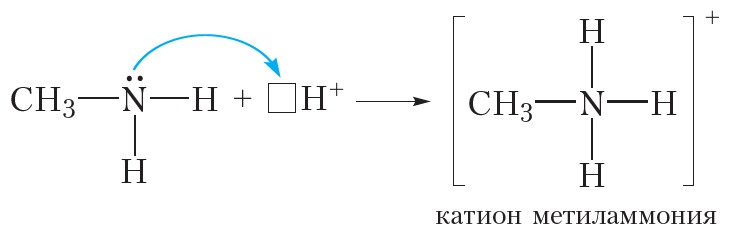
То есть так же, как и аммиак, амины обладают оснóвными свойствами.
Так, при растворении метиламина в воде протекает обратимая реакция:
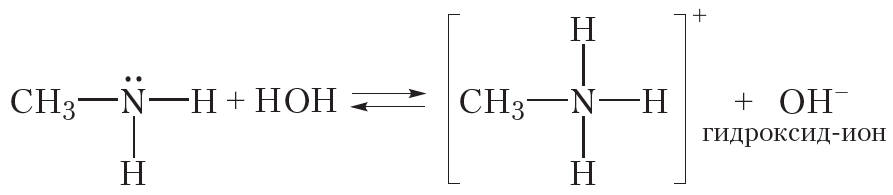
Видно, что при взаимодействии с водой молекула метиламина присоединяет катион водорода. При этом образуются ион метиламмония CH3NH3+ и гидроксид-ион OH–. Наличие ионов OH– обусловливает щелочную реакцию водного раствора метиламина, поэтому раствор метиламина в воде окрашивает фенолфталеин в малиновый цвет.
Оснóвные свойства аминов проявляются также в реакциях с кислотами. Например, при взаимодействии метиламина с соляной кислотой образуется соль — хлорид метиламмония:![]()
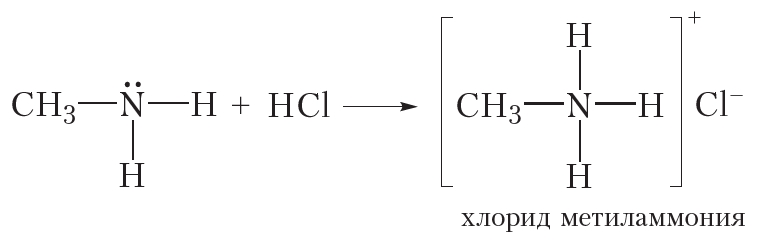
Как и все соли, хлорид метиламмония имеет ионное строение. Он состоит из катиона метиламмония и хлорид-аниона. Хлорид метиламмония — твёрдое, хорошо растворимое в воде вещество.
Аналогично протекают реакции метиламина и с другими кислотами:![]()
или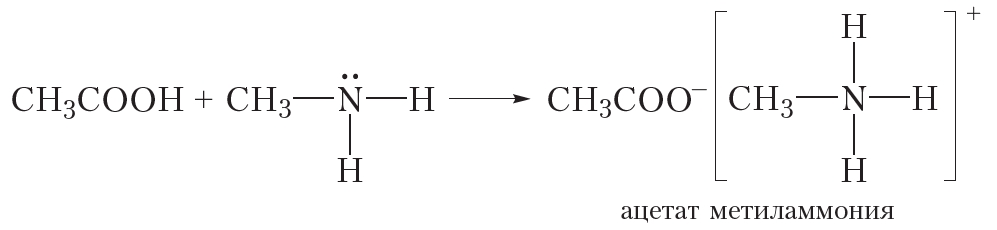
Эти реакции заключаются в присоединении катиона водорода H+ к молекуле метиламина.
Мы рассмотрели взаимодействие метиламина с водой и кислотами. Очевидно, подобным образом эти реакции будут протекать и для других аминов:![]()
или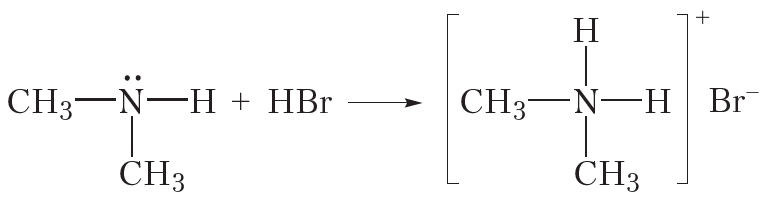 Соли аминов — твёрдые, хорошо растворимые в воде вещества. Щёлочи вытесняют амины из солей:
Соли аминов — твёрдые, хорошо растворимые в воде вещества. Щёлочи вытесняют амины из солей:
![]()
Подобную реакцию вы встречали при изучении неорганической химии, когда рассматривали вытеснение аммиака из солей аммония под действием щелочей.
2. Горение
Как и большинство органических соединений, амины горят в кислороде.
При этом образуются углекислый газ, вода и азот:
![]()
Химические свойства анилина
Структурная формула анилина: Из-за влияния бензольного кольца на аминогруппу некоторые свойства анилина отличаются от химических свойств насыщенных аминов. С другой стороны, аминогруппа в молекуле анилина оказывает влияние на свойства бензольного кольца.
Из-за влияния бензольного кольца на аминогруппу некоторые свойства анилина отличаются от химических свойств насыщенных аминов. С другой стороны, аминогруппа в молекуле анилина оказывает влияние на свойства бензольного кольца.
Реакции по аминогруппе
Из-за влияния бензольного кольца на аминогруппу оснóвные свойства анилина выражены слабее, чем у насыщенных аминов. Так, в отличие от насыщенных аминов, водный раствор анилина не изменяет окраску индикаторов. В то же время, подобно насыщенным аминам, анилин образует соли при взаимодействии с кислотами: или
или

Реакции замещения в бензольном кольце
В молекуле анилина аминогруппа влияет на свойства бензольного кольца, облегчая замещение атомов водорода. Так, при смешивании раствора анилина с бромной водой наблюдается её обесцвечивание и выпадение белого осадка. Уравнение протекающей реакции: В результате реакции происходит замещение трёх атомов водорода бензольного кольца атомами брома и образуется 2,4,6-триброманилин. Отметим, что замещение атома водорода бензольного кольца атомом брома возможно и для бензола, но условия протекания реакции гораздо более жёсткие, чем для анилина. Напомним, что подобное влияние на бензольное кольцо оказывает гидроксильная группа в молекуле фенола (§ 27).
В результате реакции происходит замещение трёх атомов водорода бензольного кольца атомами брома и образуется 2,4,6-триброманилин. Отметим, что замещение атома водорода бензольного кольца атомом брома возможно и для бензола, но условия протекания реакции гораздо более жёсткие, чем для анилина. Напомним, что подобное влияние на бензольное кольцо оказывает гидроксильная группа в молекуле фенола (§ 27).
Получение аминов
Амины можно получить из нитросоединений, с которыми вы познакомились при изучении нитрования бензола (§ 20). Сущность реакции получения аминов из нитросоединений становится понятной, если рассмотреть формулы нитросоединений и аминов:
Как видно, чтобы получить амин из нитросоединения, необходимо в молекуле нитросоединения «заменить» атомы кислорода на атомы водорода, то есть восстановить вещество. Приведём схему такой реакции:
![]()
Приведённая схема не показывает, какое вещество используется для восстановления нитросоединения, восстановитель здесь условно обозначен [H].
Рассмотрим, какие вещества используют на практике для восстановления нитросоединений.
Восстановление нитросоединений водородом в присутствии катализатора: 
Восстановление нитросоединений водородом в момент выделения. Для получения анилина таким методом в колбу помещают нитробензол, концентрированную соляную кислоту и железные опилки. Железо взаимодействует с соляной кислотой с образованием водорода, который в первый момент выделяется в атомарном виде:
![]()
Атомарный водород обладает высокой реакционной способностью и, не успев соединиться в менее активные молекулы H2, восстанавливает нитрогруппу молекулы нитробензола:
 Получающийся при этом анилин взаимодействует с соляной кислотой, образуя соль:
Получающийся при этом анилин взаимодействует с соляной кислотой, образуя соль:
Суммарное уравнение реакции восстановления нитробензола водородом в момент выделения:

Из полученной соли действием щёлочи вытесняют анилин: 
Таким образом, процесс получения анилина путём восстановления нитробензола водородом в момент выделения можно отразить схемой: 
Реакция получения аминов восстановлением нитросоединений носит имя выдающегося русского химика Николая Николаевича Зинина (1812–1880). Он не только внёс значительный вклад в развитие органической химии, но и создал блестящую школу русских химиков-органиков. Его учениками были Александр Михайлович Бутлеров — основоположник теории строения органических соединений и Александр Порфирьевич Бородин, выдающийся химик и композитор — автор оперы «Князь Игорь».
 О других методах получения аминов вы можете узнать, перейдя по ссылке в QR-коде.
О других методах получения аминов вы можете узнать, перейдя по ссылке в QR-коде.
Амины широко используются в органическом синтезе. Они являются исходными веществами для получения красителей, лекарственных препаратов и многих других веществ.
|
Амины так же, как и аммиак, обладают оснóвными свойствами. Водные растворы насыщенных аминов имеют щелочную реакцию и поэтому изменяют окраску индикаторов. Амины образуют соли при взаимодействии с кислотами. Амины горят в кислороде. При этом образуются углекислый газ, вода и азот. Оснóвные свойства анилина выражены слабее, чем у насыщенных аминов. Водный раствор анилина не изменяет окраску индикаторов. В то же время анилин, как и насыщенные амины, образует соли при взаимодействии с кислотами. Аминогруппа молекулы анилина влияет на бензольное кольцо, облегчая замещение атомов водорода в положениях 2, 4, 6, поэтому, в отличие от бензола, анилин обесцвечивает бромную воду. Амины получают восстановлением нитросоединений. |
*Получение аминов
1. Получение аминов взаимодействием спиртов с аммиаком
В промышленности простейшие амины (метиламин, диметиламин и другие) получают взаимодействием спиртов с аммиаком в присутствии катализатора при температуре 300–500 °С. При этом гидроксильная группа спирта замещается на аминогруппу. В реакции, кроме первичных аминов, образуются также вторичные и третичные амины:

2. Получение аминов взаимодействием галогеналканов с аммиаком
При взаимодействии галогеналканов с аммиаком происходит замещение галогена на аминогруппу. Эта реакция была открыта немецким химиком А. В. Гофманом. В реакции, как и в случае спиртов, кроме первичных аминов образуются также вторичные и третичные амины:

Вопросы и задания
1.  Органическое вещество А растворили в воде. В полученный раствор добавили несколько капель фенолфталеина. В результате раствор приобрёл малиновую окраску. Укажите формулу вещества А.
Органическое вещество А растворили в воде. В полученный раствор добавили несколько капель фенолфталеина. В результате раствор приобрёл малиновую окраску. Укажите формулу вещества А.

Приведите уравнение реакции, протекающей при растворении вещества А в воде.
2. Напишите уравнение реакции между этиламином (2 моль) и раствором серной кислоты (1 моль). Назовите продукт реакции.
3. Как можно получить анилин, используя в качестве исходного вещества бензол? Напишите уравнения соответствующих реакций.
4. В колбу поместили нитробензол, бромоводородную кислоту (избыток) и железные опилки. При этом образовалось органическое вещество X, массовая доля брома в котором равна 46,0 %.
а) Напишите уравнение протекающей реакции и назовите вещество X.
б) Напишите молекулярное и ионное уравнения реакции вещества X с гидроксидом натрия в водном растворе.
в) Напишите молекулярное и ионное уравнения реакции вещества X с нитратом серебра в водном растворе.
5. Твёрдое, растворимое в воде органическое вещество А при взаимодействии с водным раствором нитрата серебра образует белый творожистый осадок. При действии гидроксида калия на вещество А образуется соединение В, бесцветная маслянистая жидкость, малорастворимая в воде. При действии бромной воды на В образуется белый осадок вещества С. Массовая доля азота в веществе А равна 10,8 %. Что собой представляют вещества А, В и С? Приведите их формулы и уравнения описанных реакций.
6. Дана схема превращений:

Напишите уравнения протекающих реакций.
7. При сгорании 0,45 г органического вещества выделилось 0,448 л (н. у.) углекислого газа, 0,63 г воды и 0,112 л (н. у.) азота. Относительная плотность паров органического вещества по азоту равна 1,607. Установите молекулярную формулу этого вещества.
8. Некоторое органическое соединение, помимо углерода и водорода, содержит азот, массовая доля которого 23,7 %. Это соединение взаимодействует с соляной кислотой с образованием соли, его молекула содержит два углеводородных радикала и один атом азота. На основании этих данных:
а) Установите молекулярную формулу органического соединения.
б) Составьте его структурную формулу.
в) Приведите уравнение реакции его взаимодействия с соляной кислотой.
9*. Можно ли получить метиламин взаимодействием метана с аммиаком? Кратко поясните свой ответ.
10*. Предложите схему получения метиламина, исходя из метана и неорганических веществ. Напишите уравнения соответствующих реакций.
11*. Предложите схему получения этиламина, исходя из этилена, воды и аммиака. Напишите уравнения соответствующих реакций.
