§ 42. Угольная и кремниевая кислоты, их соли
Угольная кислота и её соли
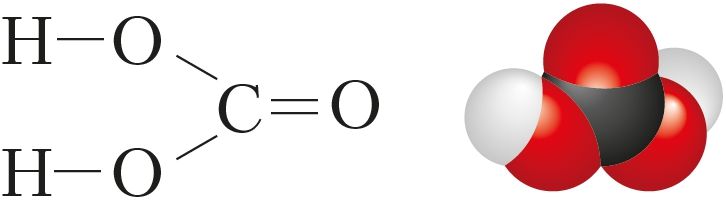
Угольная кислота H2CO3 является двухосновной и относится к слабым кислотам (рис. 100). В свободном состоянии в виде кристаллов она выделена при температуре ниже ‒30 °С лишь во втором десятилетии XXI века.
В водном растворе угольная кислота диссоциирует ступенчато:
В обычных условиях она распадается на углекислый газ и воду:
.
Угольной кислоте соответствуют два ряда солей: карбонаты (средние) и гидрокарбонаты (кислые). Отметим два важнейших свойства солей угольной кислоты.
1. Взаимодействие с кислотами. Общим свойством карбонатов и гидрокарбонатов является «вскипание» при действии более сильных кислот как на твёрдую соль, так и на её раствор. Происходит выделение газа без цвета и запаха:

Взаимодействие солей с сильными кислотами используют как тест (качественную реакцию) на присутствие солей угольной кислоты — карбонатов и гидрокарбонатов (Приложение 3).
Кроме того, такие реакции могут использоваться для получения углекислого газа в лаборатории, например, из мрамора CaCO3:
.
2. Термическое разложение. Вторая особенность солей угольной кислоты — их невысокая термическая устойчивость (кроме карбонатов натрия и калия, рубидия и цезия). При нагревании они разлагаются:
Анализируя вышесказанное и уравнения химических реакций предыдущего параграфа, можно сделать заключение, что карбонаты и гидрокарбонаты способны к взаимопревращениям, которые условно можно выразить схемой:
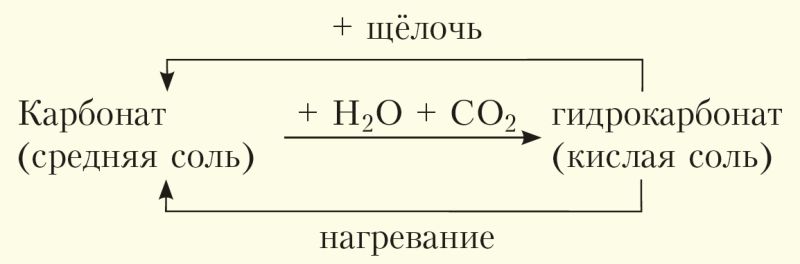
На примере карбоната кальция уравнения реакций, соответствующие данной схеме, выглядят так:
Карбонаты и гидрокарбонаты находят широкое применение в строительстве, быту, оптике, медицине, а также в производстве мыла, стекла, бумаги, являются наполнителями огнетушителей.
Таблица 30.1. Применение солей угольной кислоты
| Химическая формула и систематическое название | Тривиальное название, природные минералы | Область применения |
| Na2СO3 Карбонат натрия |
Кальцинированная сода | Производство моющих средств, стекла, красителей; целлюлозно-бумажная, текстильная, нефтехимическая промышленность |
| Na2СO3 ∙ 10H2O Декагидрат карбоната натрия |
Кристаллическая сода — минерал | |
| NaHCO3 Гидрокарбонат натрия |
Питьевая сода | Кулинария, дезинфекция полости рта, средство от изжоги. Пожаротушение. Безопасное мытьё посуды |
| СаСО3 Карбонат кальция |
Мел — горная порода | Побелка, производство стекла, резины |
| Кальцит — минерал | Химическое производство, строительство, оптика, поделочный камень | |
| Ракушечник — горная порода | Строительный материал | |
| Известняк — горная порода | Облицовочный и архитектурно-строительный материал | |
| Мрамор — горная порода | Облицовочный и архитектурно-строительный материал | |
| Жемчуг — драгоценный камень биологического происхождения, образуемый в раковинах некоторых моллюсков | Ювелирные изделия | |
| (СuOH)2CO3 Карбонат гидроксомеди(II) |
Малахит — минерал | Поделочный камень. Ранее — для добычи меди |
| MgСO3 Карбонат магния |
Магнезит — минерал | Производство огнеупорных материалов |
| CaMg(CO3)2 Двойной карбонат кальция и магния |
Доломит — минерал | Изготовление цемента, штукатурки, огнеупорных материалов, в стекольной промышленности, в сельском хозяйстве для раскисления почвы |