§ 42. Угольная и кремниевая кислоты, их соли
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 42. Угольная и кремниевая кислоты, их соли |
| Напечатано:: | Гость |
| Дата: | Thursday, 21 May 2026, 02:07 |
Угольная кислота и её соли
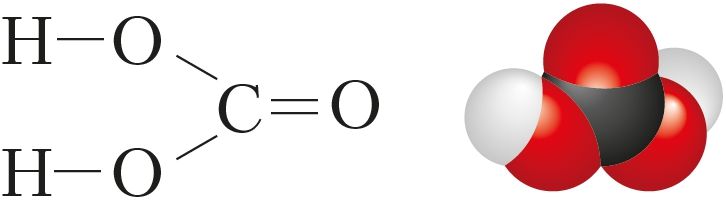
Угольная кислота H2CO3 является двухосновной и относится к слабым кислотам (рис. 100). В свободном состоянии в виде кристаллов она выделена при температуре ниже ‒30 °С лишь во втором десятилетии XXI века.
В водном растворе угольная кислота диссоциирует ступенчато:
В обычных условиях она распадается на углекислый газ и воду:
.
Угольной кислоте соответствуют два ряда солей: карбонаты (средние) и гидрокарбонаты (кислые). Отметим два важнейших свойства солей угольной кислоты.
1. Взаимодействие с кислотами. Общим свойством карбонатов и гидрокарбонатов является «вскипание» при действии более сильных кислот как на твёрдую соль, так и на её раствор. Происходит выделение газа без цвета и запаха:

Взаимодействие солей с сильными кислотами используют как тест (качественную реакцию) на присутствие солей угольной кислоты — карбонатов и гидрокарбонатов (Приложение 3).
Кроме того, такие реакции могут использоваться для получения углекислого газа в лаборатории, например, из мрамора CaCO3:
.
2. Термическое разложение. Вторая особенность солей угольной кислоты — их невысокая термическая устойчивость (кроме карбонатов натрия и калия, рубидия и цезия). При нагревании они разлагаются:
Анализируя вышесказанное и уравнения химических реакций предыдущего параграфа, можно сделать заключение, что карбонаты и гидрокарбонаты способны к взаимопревращениям, которые условно можно выразить схемой:
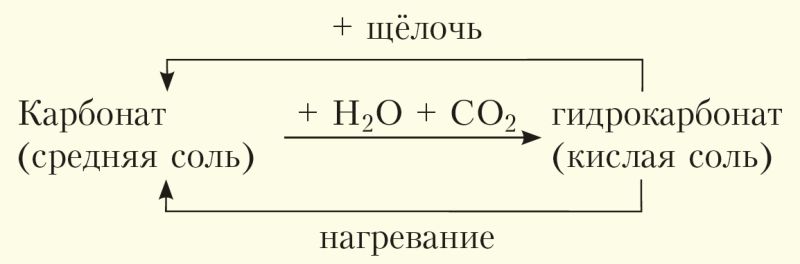
На примере карбоната кальция уравнения реакций, соответствующие данной схеме, выглядят так:
Карбонаты и гидрокарбонаты находят широкое применение в строительстве, быту, оптике, медицине, а также в производстве мыла, стекла, бумаги, являются наполнителями огнетушителей.
Таблица 30.1. Применение солей угольной кислоты
| Химическая формула и систематическое название | Тривиальное название, природные минералы | Область применения |
| Na2СO3 Карбонат натрия |
Кальцинированная сода | Производство моющих средств, стекла, красителей; целлюлозно-бумажная, текстильная, нефтехимическая промышленность |
| Na2СO3 ∙ 10H2O Декагидрат карбоната натрия |
Кристаллическая сода — минерал | |
| NaHCO3 Гидрокарбонат натрия |
Питьевая сода | Кулинария, дезинфекция полости рта, средство от изжоги. Пожаротушение. Безопасное мытьё посуды |
| СаСО3 Карбонат кальция |
Мел — горная порода | Побелка, производство стекла, резины |
| Кальцит — минерал | Химическое производство, строительство, оптика, поделочный камень | |
| Ракушечник — горная порода | Строительный материал | |
| Известняк — горная порода | Облицовочный и архитектурно-строительный материал | |
| Мрамор — горная порода | Облицовочный и архитектурно-строительный материал | |
| Жемчуг — драгоценный камень биологического происхождения, образуемый в раковинах некоторых моллюсков | Ювелирные изделия | |
| (СuOH)2CO3 Карбонат гидроксомеди(II) |
Малахит — минерал | Поделочный камень. Ранее — для добычи меди |
| MgСO3 Карбонат магния |
Магнезит — минерал | Производство огнеупорных материалов |
| CaMg(CO3)2 Двойной карбонат кальция и магния |
Доломит — минерал | Изготовление цемента, штукатурки, огнеупорных материалов, в стекольной промышленности, в сельском хозяйстве для раскисления почвы |
Кремниевая кислота и её соли
Кремниевая кислота H2SiO3 является двухосновной и более слабой, чем угольная кислота. Её получают взаимодействием силикатов (Na2SiO3 или K2SiO3) с более сильными кислотами, например H2SO4, HCl:
Кремниевая кислота при этом выделяется в виде студенистого осадка, состав которого часто выражают формулой nSiO2 · mH2O. В действительности кремниевая кислота имеет полимерную природу:
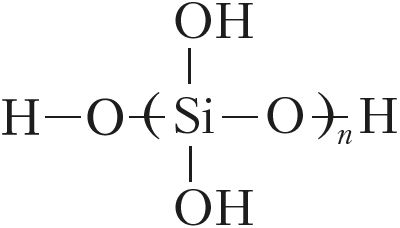
Уже при незначительном нагревании или длительном хранении кислота разлагается на оксид и воду:
.
Образующийся оксид SiO2 имеет пористую структуру и большую площадь поверхности (до 1000 м2/г), что позволяет ему адсорбировать молекулы различных веществ, в том числе и воду. Именно благодаря адсорбционным свойствам оксид SiO2 под названием «силикагель» используется как осушитель воздуха в упаковках с электроникой и обувью, а под названием «Белый уголь» — как адсорбент в медицине (рис. 101).

Соли кремниевой кислоты
Для кремниевой кислоты известны только средние соли — силикаты. Большинство из них плохо растворяются в воде. Растворимые соли силикат натрия и силикат калия называют «растворимые стёкла» и используют как «канцелярский клей». Получить силикаты можно сплавлением оксида кремния(IV) как кислотного оксида со щелочами, оксидами металлов, а также с карбонатами:
Производство строительных материалов на основе силикатов и карбонатов
Природные силикаты и карбонаты служат основой для производства цемента, бетона, стекла.
Цемент получают спеканием известняка CaCO3 и глины, одна из составных частей которой — каолинит, включающий оксиды SiO2 и Al2O3.
В процессе спекания смеси известняка СаСО3 и каолинита Al2[Si2O5](OH)4 образуется сложная смесь безводных солей — силикатов и алюминатов кальция. Напомним, что при смешивании такой тонко измельчённой смеси с водой происходит гидратация, образование кристаллогидратов, срастание отдельных частичек друг с другом (схватывание) и получение твёрдого прочного материала — цементного камня.
Бетон изготавливают из смеси песка, цемента и воды. Добавляя в такую смесь шлак, получают шлакобетон. Если свежеприготовленной смесью заливают металлический каркас, то при затвердевании получаются железобетонные конструкции. При использовании в качестве наполнителя газообразных веществ получают пенобетон.
Стекло применяют в строительной сфере (остекление окон, витражей, дверей, оранжерей), в оптической промышленности, медицине, машиностроении, приборостроении, современной архитектуре, электронике, быту. Как отмечено выше в параграфе, сырьём для производства стекла («варки стекла») являются карбонаты натрия и кальция, а также оксид кремния(IV),то есть кристаллическая сода, мел или известняк и кварцевый песок (Na2CO3, CaCO3, SiO2). Как уже отмечалось в § 41, в состав стекла входят оксиды натрия, кальция и кремния в мольном соотношении 1 : 1 : 6.
Для придания стеклу особых свойств в исходную смесь вводят добавки. Так, для его окрашивания используют различные оксиды: СuO придаёт голубой цвет, FeO — зелёный, СоО — от голубого до сине-фиолетового. Глушители уменьшают прозрачность стекла, делают его матовым. Наклеивание полимерных плёнок увеличивает прочность. Армирование металлической проволокой придаёт декоративные свойства и препятствует образованию больших осколков при растрескивании. Следует отметить возможность многократной переработки стекла.
Кремниевая и угольная кислоты — нестойкие вещества, разлагающиеся с образованием оксида и воды: кремниевая — при незначительном нагревании или длительном хранении, а угольная — сразу при образовании.
Карбонаты и гидрокарбонаты способны к взаимопревращениям.
Важнейшими строительными материалами на основе природных силикатов и карбонатов являются цемент, бетон и стекло.
Вопросы, задания, задачи
1. Выпишите характеристики, относящиеся:
- а) к угольной кислоте;
- б) к кремниевой кислоте:
- 1) слабый электролит;
- 2) термически устойчива;
- 3) разлагается на оксид и воду;
- 4) образуется при растворении оксида в воде;
- 5) при разложении образует газообразный оксид;
- 6) продукт её распада — силикагель;
- 7) образует два ряда солей;
- 8) её соли при добавлении кислоты «вскипают»;
- 9) соли называют карбонатами и гидрокарбонатами;
- 10) образуется при добавлении соляной кислоты к силикату;
- 11) соли называют силикатами;
- 12) один из атомов имеет степень окисления +4.
2. Запишите в молекулярной и ионной форме уравнения реакций, которые иллюстрируют химические свойства а) угольной и б) кремниевой кислот, названные в задании 1.
3. Заполните таблицу «Строительные материалы» (цемент, бетон, железобетон, стекло):
| Строительный материал | Сырьё для производства |
4. Заполните таблицу «Применение карбонатов и гидрокарбонатов»
| № | Химические формулы и названия | Области применения |
5. Составьте уравнения возможных реакций:
- a)
- б)
- в)
- г)
- д)
- е)
- ж)
- з)
- и)
- к)
- л)
- м)
6. Рассчитайте массу кальцинированной соды, известняка и кварцевого песка, необходимых для получения стекла массой 100 кг, допуская, что исходные вещества не содержат примесей.
7. Составьте уравнения реакций согласно схеме:

8. При длительном хранении растворов щелочей в стеклянной посуде в растворах появляется муть. Поясните, какие реакции являются причиной этого явления.
9. Предложите способы получения не менее восьми сложных веществ, имея в распоряжении силикат калия и гидрокарбонат кальция. Запишите уравнения реакций и список полученных веществ.
10. Определите объём углекислого газа (н. у.), который выделится из огнетушителя, содержащего серную кислоту и раствор объёмом 10 дм3 с массовой долей гидрокарбоната натрия 8 % (плотность раствора — 1,058 г/см3).
*Подготовьте сообщения:
- 1. Как образуются сталактиты и сталагмиты;
- 2. Производство стекла в Республике Беларусь.
*Самоконтроль
1. Угольная кислота образует соли:
- а) силикаты;
- б) карбиды;
- в) карбонаты;
- г) гидрокарбонаты.
2. Основным сырьём для производства стекла являются:
- а) известняк;
- б) глина;
- в) кальцинированная сода;
- г) кварцевый песок.
3. Соль состава Са(НСО3)2:
- а) является кислой;
- б) реагирует с углекислым газом в растворе;
- в) термически неустойчива;
- г) реагирует со щелочами.
4. Термически устойчивым веществом является:
- а) SiO2;
- б) Ca(НСO3)2;
- в) H2SiO3;
- г) H2СO3.
5. Не протекает реакция:
- а) СаСО3
;
- б) K2СO3
;
- в) MgO + SiO2
;
- г) Вa(НСO3)2
.