§ 30. Галогены
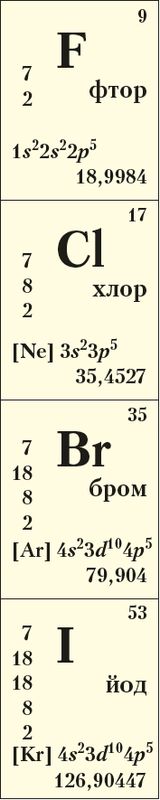
Галогены как химические элементы
К галогенам относят пять элементов VIIА-группы периодической системы: фтор F, хлор Сl, бром Вr, йод I и астат At.
Атомы галогенов содержат по 7 электронов на внешнем электронном слое, общая электронная конфигурация которого ns2np5, то есть галогены являются р-элементами (Приложение 1). Электронно-графические схемы внешнего электронного слоя атомов фтора и хлора выглядят следующим образом:
При этом на внешнем электронном слое у атома фтора четыре орбитали, а атомы остальных галогенов содержат ещё пять незаполненных d-орбиталей.
Фтор как самый электроотрицательный элемент в соединениях проявляет только отрицательную степень окисления –1. Характерные для других элементов степени окисления (–1, +1, +3, +5, +7) можно объяснить возможностью распаривания электронов внешнего электронного слоя. В случае атомов хлора это выглядит так:
Степени окисления +1, –1, 0
Степень окисления +5
Степень окисления +3
Степень окисления +7
Примерами соединений с различными степенями окисления хлора могут служить известные вам вещества: (галит),
(бертолетова соль),
(хлорная кислота).
В природе галогены существуют в виде соединений с другими элементами (табл. 21, рис. 68). Фтор и хлор принадлежат к двадцати самым распространённым элементам в земной коре.
Таблица 21. Химические элементы галогены
| Элемент | Радиус атома, нм | χ | Степени окисления | Природные соединения |
| Фтор 9F | 0,071 | 4,0 | –1, 0 | CaF2 (флюорит, плавиковый шпат); Na3[AlF6] (криолит); Са5[РО4]3F (фторапатит) |
| Хлор 17Cl | 0,099 | 3,0 | –1, 0, +1, +3, +5, +7 | NaCl (каменная соль, галит); KCl (сильвин); Смесь NaCl и KCl (сильвинит); KMgCl3 · 6H2O (карналлит) |
| Бром 35Br | 0,114 | 2,8 | –1, 0, +1, +3, +5, +7 | NaBr, KBr, MgBr2 — в отложениях хлоридов; в морской воде в виде бромид-ионов |
| Йод 53I | 0,133 | 2,5 | –1, 0, +1, +3, +5, +7 | KIO3 (йодат калия) — в залежах чилийской селитры, в подземных буровых водах, в морских водорослях |
