§ 45. Будова і фізічныя ўласцівасці амінаў
Будова малекул амінаў
Аміны можна разглядаць як вытворныя аміяку, у малекуле якога адзін, два ці тры атамы вадароду замешчаны на вуглевадародныя радыкалы.
Напрыклад, замесцім адзін атам вадароду малекулы аміяку на метыльны радыкал:
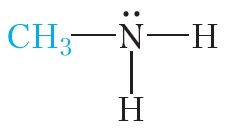
Такое злучэнне называецца метыламін. Метыламін уяўляе сабой бясколерны газ (tкіп = –6 °С) з рэзкім пахам, які нагадвае пах аміяку.
Метыламін з’яўляецца найпрасцейшым прадстаўніком амінаў. Яго формулу можна запісаць наступным чынам: CH3 ![]() NH2. Відаць, што ў малекуле метыламіну маецца група
NH2. Відаць, што ў малекуле метыламіну маецца група ![]() NH2, якая называецца амінагрупай.
NH2, якая называецца амінагрупай.
Калі замясціць два атамы вадароду малекулы аміяку на метыльныя радыкалы, то атрымаецца дыметыламін:
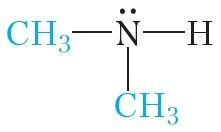
Нарэшце, пры замяшчэнні ўсіх трох атамаў вадароду малекулы аміяку на метыльныя радыкалы атрымаем трыметыламін:
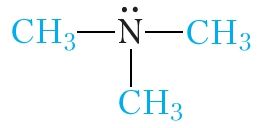
У залежнасці ад ліку замешчаных атамаў вадароду аміны падзяляюць на першасныя (замешчаны адзін атам вадароду), другасныя (замешчаны два атамы вадароду) і трацічныя (замешчаны тры атамы вадароду):

Метыламін CH3 ![]() NH2 з’яўляецца першасным амінам. Улічваючы, што агульная формула алкільных радыкалаў CnH2n+1
NH2 з’яўляецца першасным амінам. Улічваючы, што агульная формула алкільных радыкалаў CnH2n+1 ![]() , лёгка атрымаць агульную формулу гамолагаў метыламіну:
, лёгка атрымаць агульную формулу гамолагаў метыламіну:
![]()
У малекулах амінаў, як і ў малекуле аміяку, у атама азоту маецца непадзеленая электронная пара. Дзякуючы гэтаму аміны, як і аміяк, могуць далучаць катыён вадароду H+. Гэта значыць аміны з’яўляюцца арганічнымі асновамі.
Назвы амінаў складаюцца з назваў вуглевадародных радыкалаў, звязаных з атамам азоту, і канчатка -амін. Прывядзём назвы некаторых амінаў:
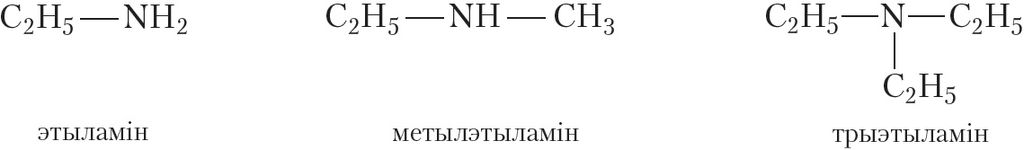
Акрамя алкільных радыкалаў малекулы амінаў могуць змяшчаць і іншыя замяшчальнікі. Прыкладам такога аміну з’яўляецца анілін:
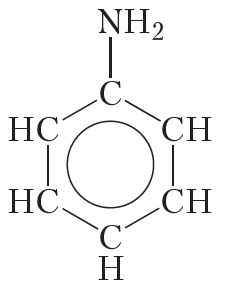
У малекуле аніліну група ![]() NH2 звязана з радыкалам
NH2 звязана з радыкалам ![]() C6H5, які называецца феніл. Таму анілін называюць таксама феніламінам.
C6H5, які называецца феніл. Таму анілін называюць таксама феніламінам.
Анілін уяўляе сабой бясколерную алеістую вадкасць, дрэнна растваральную ў вадзе, з тэмпературай кіпення 184 °С. Анілін ядавіты.