§ 29. Альдэгіды. Наменклатура. Ізамерыя. Фізічныя ўласцівасці
Будова альдэгіднай групы
Вы ўжо ведаеце, што атамы кіслароду ў малекулах арганічных злучэнняў могуць выступаць у якасці «масткоў» паміж алкільным радыкалам і атамам вадароду (спірты):
![]()
або паміж дзвюма алкільнымі групамі (простыя эфіры):
![]()
Акрамя таго, атам кіслароду можа быць звязаны з атамам вугляроду двайной сувяззю:
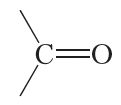
Дадзеная формула адлюстроўвае будову новай функцыянальнай групы, якая ўваходзіць у састаў мноства арганічных злучэнняў. Гэта група называецца карбанільнай групай.
Як бачна, атам вугляроду карбанільнай групы ўтварае дзве сувязі з атамам кіслароду. Дзве астатнія сувязі атам вугляроду можа ўтвараць з вуглевадароднымі радыкаламі:
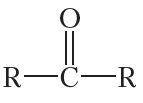
Такія арганічныя злучэнні адносяцца да класа кетонаў.
Вуглевадародныя радыкалы ў малекулах кетонаў могуць быць як аднолькавымі, так і рознымі. У малекуле найпрасцейшага кетону абодва радыкалы — метыльныя групы. Гэты кетон называецца ацэтонам:
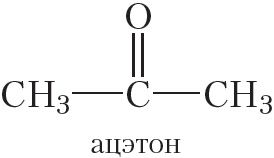
Ацэтон уяўляе сабой лёгкакіпячую вадкасць (tкіп = 56 °С) з характэрным пахам, якая неабмежавана змешваецца з вадой. Выкарыстоўваецца ў якасці растваральніка і ў арганічным сінтэзе.
Цікава ведаць
Яшчэ адзін вядомы кетон — кетон маліны — таксама мае ў саставе малекулы карбанільную групу. Гэта злучэнне больш складанай будовы:
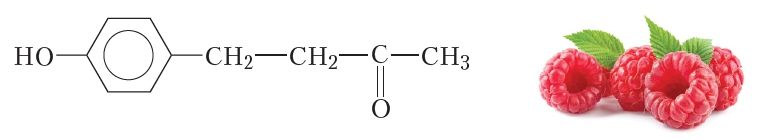
Кетон маліны змяшчаецца, натуральна, у маліне, што абумоўлівае яе характэрны пах. Сінтэтычны кетон маліны прымяняецца ў якасці дабаўкі да харчовых прадуктаў і касметычных сродкаў.
Калі злучыць карбанільную групу з атамам вадароду, то атрымаецца альдэгідная група:
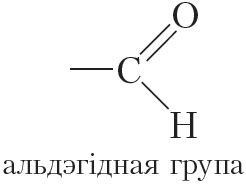
Злучэнні, якія змяшчаюць альдэгідную групу, адносяцца да класа альдэгідаў. У малекуле найпрасцейшага прадстаўніка гэтага класа злучэнняў альдэгідная група звязана з атамам вадароду:
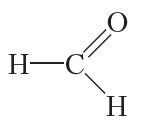
Гэта злучэнне называецца мурашыным альдэгідам або фармальдэгідам, і ўяўляе сабой бясколерны ядавіты газ з рэзкім пахам, які добра раствараецца ў вадзе. 40%-ны водны раствор фармальдэгіду называецца фармалін і выкарыстоўваецца для кансервацыі біялагічных прэпаратаў.
Атам вугляроду альдэгіднай групы знаходзіцца ў стане sp2-гібрыдызацыі. З адной s- і двух p-арбіталей фарміруюцца тры гібрыдныя арбіталі, за кошт якіх атам вугляроду ўтварае тры σ-сувязі. Негібрыдная р-арбіталь атама вугляроду ўдзельнічае ва ўтварэнні π-сувязі з атамам кіслароду:
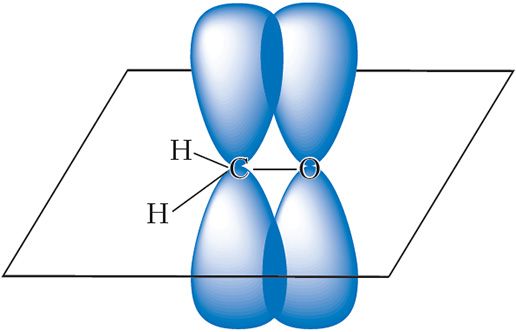
Малекула фармальдэгіду плоская, валентныя вуглы блізкія да 120°. Шарастрыжнёвая мадэль малекулы фармальдэгіду:
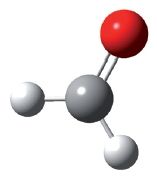
У малекуле бліжэйшага гамолага фармальдэгіду альдэгідная група звязана з метыльным радыкалам:
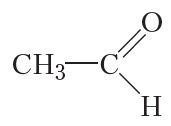
Назва гэтага злучэння — воцатны альдэгід або ацэтальдэгід. Воцатны альдэгід пры н. у. уяўляе сабой бясколерную вадкасць з пахам яблыкаў. Тэмпература кіпення воцатнага альдэгіду 21 °С.
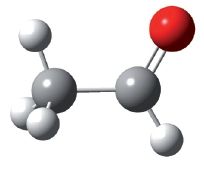
Шарастрыжнёвая мадэль малекулы воцатнага альдэгіду:
Наяўнасць групы 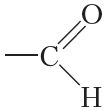 (або
(або ![]() CHO) у малекулах альдэгідаў абумоўлівае іх характэрныя хімічныя ўласцівасці. Таму альдэгідную групу называюць функцыянальнай групай. Такім чынам, альдэгіды — арганічныя злучэнні, у малекулах якіх змяшчаецца група
CHO) у малекулах альдэгідаў абумоўлівае іх характэрныя хімічныя ўласцівасці. Таму альдэгідную групу называюць функцыянальнай групай. Такім чынам, альдэгіды — арганічныя злучэнні, у малекулах якіх змяшчаецца група ![]() CHO, злучаная з атамам вадароду або вуглевадародным радыкалам.
CHO, злучаная з атамам вадароду або вуглевадародным радыкалам.
Саставім агульную формулу гамолагаў воцатнага альдэгіду. У малекулах такіх альдэгідаў група ![]() CHO злучана з алкільным радыкалам ці вадародам. Як вы ўжо ведаеце, алкільны радыкал утвараецца ў выніку адрыву ад малекулы алкану аднаго атама вадароду. Агульная формула алкільных радыкалаў CnH2n+1
CHO злучана з алкільным радыкалам ці вадародам. Як вы ўжо ведаеце, алкільны радыкал утвараецца ў выніку адрыву ад малекулы алкану аднаго атама вадароду. Агульная формула алкільных радыкалаў CnH2n+1 ![]() . Тады агульная формула гамолагаў воцатнага альдэгіду:
. Тады агульная формула гамолагаў воцатнага альдэгіду:
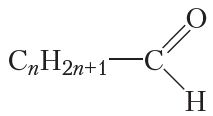
Звярніце ўвагу, што для мурашынага альдэгіду n = 0.