§ 28. Хімічныя ўласцівасці, атрыманне і прымяненне фенолу
Хімічныя ўласцівасці фенолу
У малекуле фенолу маецца гідраксільная група, таму можна чакаць, што фенол будзе праяўляць хімічныя ўласцівасці, характэрныя для спіртоў. У той жа час з-за ўплыву бензольнага кольца на гідраксільную групу некаторыя ўласцівасці фенолу адрозніваюцца ад хімічных уласцівасцей спіртоў.
1. Узаемадзеянне са шчолачнымі металамі
Падобна спіртам, фенол рэагуе са шчолачнымі металамі. Калі ў расплаўлены фенол змясціць кавалачак металічнага натрыю, назіраецца вылучэнне вадароду (тэмпература плаўлення фенолу невысокая і складае ўсяго 41 °С). У ходзе рэакцыі атам вадароду гідраксільнай групы замяшчаецца на атам натрыю:
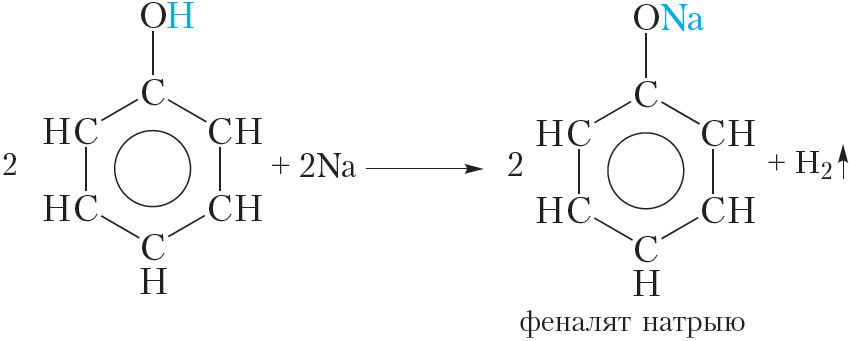
У выніку ўтвараецца феналят натрыю. Феналяты, падобна алкагалятам, уяўляюць сабой цвёрдыя солепадобныя рэчывы.
Рэакцыя фенолу са шчолачнымі металамі сведчыць аб тым, што фенол, як і спірты, праяўляе слабыя кіслотныя ўласцівасці.
2. Узаемадзеянне са шчолачамі (адрозненне фенолу ад спіртоў)
Кіслотныя ўласцівасці фенолу выяўлены мацней, чым у спіртоў. Гэта праяўляецца ў тым, што, у адрозненне ад спіртоў, фенол узаемадзейнічае са шчолачамі:
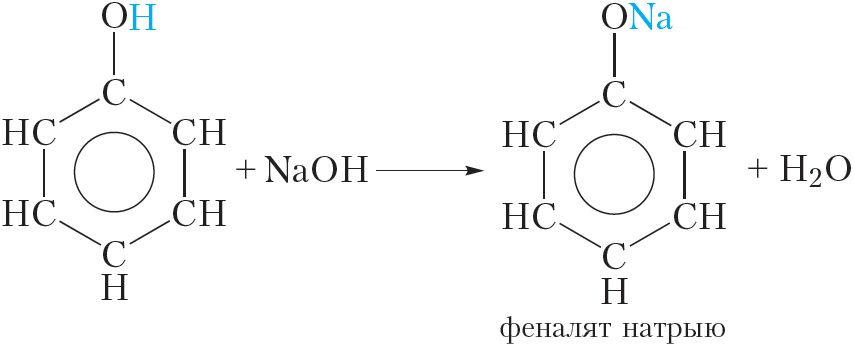
Феналят натрыю, які ўтвараецца, добра раствараецца ў вадзе. Значыць фенол умерана растварымы ў вадзе, але добра раствараецца ў растворы гідраксіду натрыю, так як пры гэтым утвараецца растварымы феналят натрыю.
Узмацненне кіслотных уласцівасцей фенолу ў параўнанні са спіртамі абумоўлена ўплывам бензольнага кольца, які прыводзіць да памяншэння трываласці сувязі О ![]() OH. У выніку атам вадароду гідраксільнай групы малекулы фенолу можа замяшчацца на атам металу не толькі пры ўзаемадзеянні са шчолачнымі металамі, але і са шчолачамі.
OH. У выніку атам вадароду гідраксільнай групы малекулы фенолу можа замяшчацца на атам металу не толькі пры ўзаемадзеянні са шчолачнымі металамі, але і са шчолачамі.
Па кіслотных уласцівасцях фенол пераўзыходзіць не толькі спірты, але і ваду. Таму феналяты, у адрозненне ад алкагалятаў, не раскладаюцца вадой. Наяўнасць у фенолу кіслотных уласцівасцей адлюстроўвае яго трывіяльная назва — карболавая кіслата.
Тым не менш фенол — вельмі слабая кіслата. Нават вугальная кіслата мацней чым фенол і таму выцясняе яго з феналяту натрыю:
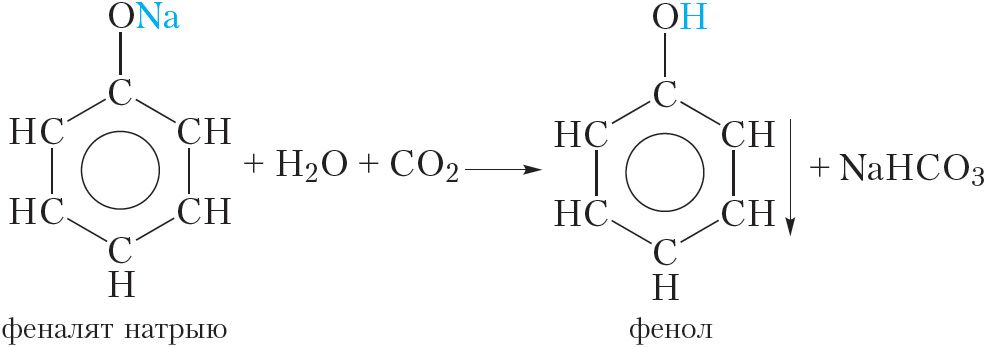
Гэту рэакцыю можна ажыццявіць наступным чынам. Праз раствор феналяту натрыю прапускаюць вуглякіслы газ, пры гэтым назіраецца памутненне раствору, так як фенол, які ўтвараецца, выпадае ў асадак.
3. Узаемадзеянне з бромнай вадой (адрозненне фенолу ад бензолу)
У малекуле фенолу змяшчаецца бензольнае кольца, таму можна чакаць, што фенол будзе праяўляць хімічныя ўласцівасці, характэрныя для араматычных вуглевадародаў, напрыклад бензолу. Як вы ўжо ведаеце, для бензолу характэрны рэакцыі замяшчэння атамаў вадароду. Так, бензол у прысутнасці каталізатара рэагуе з бромам. Пры гэтым працякае рэакцыя замяшчэння аднаго атама вадароду на бром:
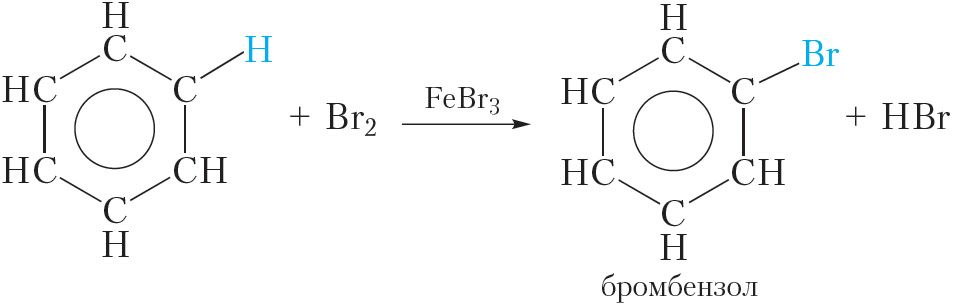
Бромную ваду бензол не абясколервае!
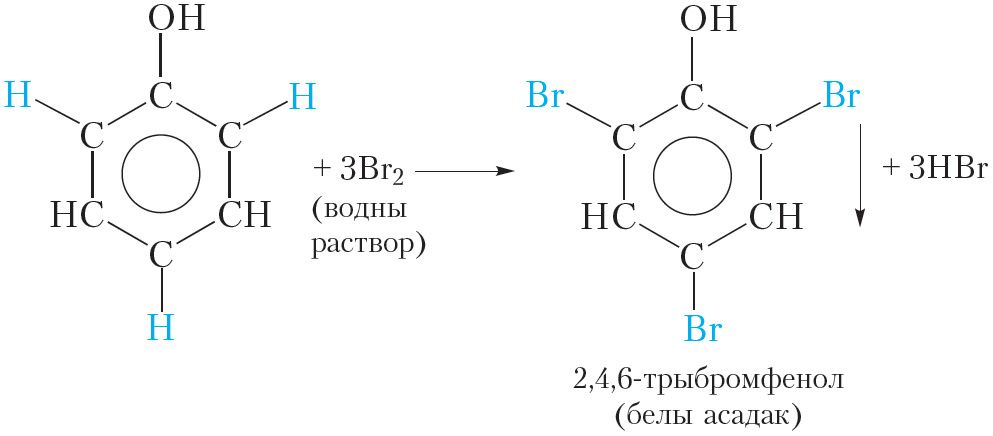
У малекуле фенолу гідраксільная група ўплывае на ўласцівасці бензольнага кольца, палягчаючы замяшчэнне атамаў вадароду, таму ўзаемадзеянне фенолу з бромам лёгка працякае і без каталізатара. Так, пры змешванні разбаўленага раствору фенолу з бромнай вадой назіраецца абясколерванне бромнай вады і выпадзенне белага асадку. Ураўненне рэакцыі, якая працякае:
Якасныя
рэакцыі на фенол
У выніку рэакцыі адбываецца замяшчэнне трох атамаў вадароду бензольнага кольца атамамі брому і ўтвараецца 2,4,6-трыбромфенол. Адзначым, што замяшчэнне атама вадароду бензольнага кольца атамамі брому магчыма і для бензолу, але ўмовы працякання рэакцыі значна больш жорсткія, чым для фенолу. Для гэтага патрабуецца бром, а не бромная вада, а таксама каталізатар. Брамаванне фенолу працякае ў мяккіх умовах, што сведчыць аб павышанай рэакцыйнай здольнасці бензольнага кольца фенолу. Гэта абумоўлена ўплывам гідраксільнай групы, якая палягчае замяшчэнне атамаў вадароду ў становішчах 2, 4, 6 бензольнага кольца малекулы фенолу.
4. Узаемадзеянне з азотнай кіслатой
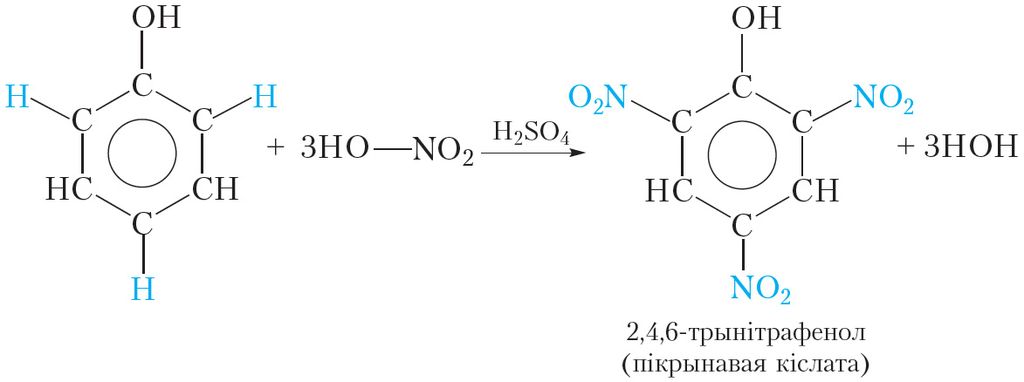
Пры ўзаемадзеянні фенолу з сумессю канцэнтраваных азотнай і сернай кіслот можна замясціць тры атамы вадароду бензольнага кольца на групы ![]() NO2:
NO2:
атрыманне фенолу
У выніку рэакцыі ўтвараецца 2,4,6-трынітрафенол. Кіслотныя ўласцівасці 2,4,6-трынітрафенолу выяўлены значна мацней, чым у фенолу. Трывіяльная назва 2,4,6-трынітрафенолу — пікрынавая кіслата. Пікрынавая кіслата і яе солі з’яўляюцца выбуховымі рэчывамі.
Разгледжаныя хімічныя ўласцівасці фенолу дэманструюць узаемны ўплыў атамаў у малекулах арганічных злучэнняў: бензольнае кольца ўзмацняе кіслотнасць гідраксільнай групы малекулы фенолу, у сваю чаргу, гідраксільная група ўплывае на бензольнае кольца, палягчаючы замяшчэнне атамаў вадароду ў становішчах 2, 4, 6.

