§ 22. Насычаныя аднаатамныя спірты. Ізамерыя, наменклатура, класіфікацыя
Насычаныя аднаатамныя спірты. Ізамерыя, наменклатура, класіфікацыя
У папярэдніх параграфах мы вывучалі вуглевадароды — арганічныя рэчывы, якія складаюцца з двух хімічных элементаў — вугляроду і вадароду. У састаў арганічных рэчываў могуць уваходзіць і іншыя элементы. У дадзенымраздзеле мы будзем вывучаць будову і ўласцівасці спіртоў. У састаў спіртоў, акрамя вугляроду і вадароду, уваходзяць атамы кіслароду.
Адзін з прадстаўнікоў класа спіртоў — этылавы спірт — мае малекулярную формулу C2H6O. Паспрабуем скласці структурную формулу этылавага спірту. На знешнім электронным слоі атама кіслароду маецца два няспараныя электроны:
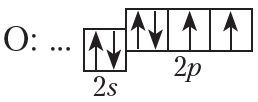
Такім чынам, валентнасць кіслароду роўная двум, таму ад сімвала O ў структурных формулах трэба маляваць дзве рысачкі.
Тады можна прапанаваць два рэчывы, якія маюць малекулярную формулу C2H6O:
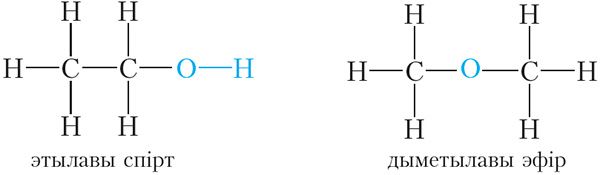
Першае злучэнне адносіцца да класа спіртоў. У малекулах спіртоў змяшчаецца група ![]() ОН, якая называецца гідраксільнай групай. Каб падкрэсліць, што ў малекуле этылавага спірту маецца гідраксільная група, яго малекулярную формулу звычайна запісваюць так: C2H5OH. Наяўнасць гідраксільнай групы ў малекулах спіртоў абумоўлівае іх характэрныя хімічныя ўласцівасці, таму групу
ОН, якая называецца гідраксільнай групай. Каб падкрэсліць, што ў малекуле этылавага спірту маецца гідраксільная група, яго малекулярную формулу звычайна запісваюць так: C2H5OH. Наяўнасць гідраксільнай групы ў малекулах спіртоў абумоўлівае іх характэрныя хімічныя ўласцівасці, таму групу ![]() ОН называюць функцыянальнай групай. У малекулах спіртоў можа змяшчацца не адна, а дзве і больш гідраксільныя групы.
ОН называюць функцыянальнай групай. У малекулах спіртоў можа змяшчацца не адна, а дзве і больш гідраксільныя групы.
Спірты — арганічныя злучэнні, малекулы якіх змяшчаюць адну або некалькі гідраксільных груп, злучаных з вуглевадародным радыкалам.
Другое злучэнне адносіцца да класа простых эфіраў. У малекулах простых эфіраў няма гідраксільнай групы. Атам кіслароду ў малекулах простых эфіраў звязаны з двума вуглевадароднымі радыкаламі.
Этылавы спірт і дыметылавы эфір маюць аднолькавую малекулярную формулу, але розную будову. Такім чынам, яны з’яўляюцца ізамерамі.