§ 22. Насычаныя аднаатамныя спірты. Ізамерыя, наменклатура, класіфікацыя
| Сайт: | Профильное обучение |
| Курс: | Хімія. 10 клас |
| Книга: | § 22. Насычаныя аднаатамныя спірты. Ізамерыя, наменклатура, класіфікацыя |
| Напечатано:: | Гость |
| Дата: | Пятница, 15 Август 2025, 02:55 |
Насычаныя аднаатамныя спірты. Ізамерыя, наменклатура, класіфікацыя
У папярэдніх параграфах мы вывучалі вуглевадароды — арганічныя рэчывы, якія складаюцца з двух хімічных элементаў — вугляроду і вадароду. У састаў арганічных рэчываў могуць уваходзіць і іншыя элементы. У дадзенымраздзеле мы будзем вывучаць будову і ўласцівасці спіртоў. У састаў спіртоў, акрамя вугляроду і вадароду, уваходзяць атамы кіслароду.
Адзін з прадстаўнікоў класа спіртоў — этылавы спірт — мае малекулярную формулу C2H6O. Паспрабуем скласці структурную формулу этылавага спірту. На знешнім электронным слоі атама кіслароду маецца два няспараныя электроны:
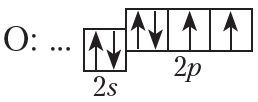
Такім чынам, валентнасць кіслароду роўная двум, таму ад сімвала O ў структурных формулах трэба маляваць дзве рысачкі.
Тады можна прапанаваць два рэчывы, якія маюць малекулярную формулу C2H6O:
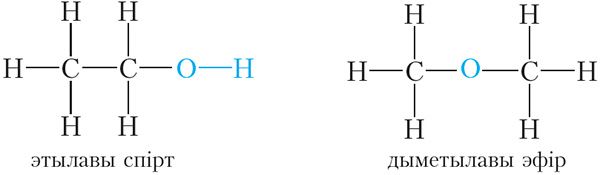
Першае злучэнне адносіцца да класа спіртоў. У малекулах спіртоў змяшчаецца група ![]() ОН, якая называецца гідраксільнай групай. Каб падкрэсліць, што ў малекуле этылавага спірту маецца гідраксільная група, яго малекулярную формулу звычайна запісваюць так: C2H5OH. Наяўнасць гідраксільнай групы ў малекулах спіртоў абумоўлівае іх характэрныя хімічныя ўласцівасці, таму групу
ОН, якая называецца гідраксільнай групай. Каб падкрэсліць, што ў малекуле этылавага спірту маецца гідраксільная група, яго малекулярную формулу звычайна запісваюць так: C2H5OH. Наяўнасць гідраксільнай групы ў малекулах спіртоў абумоўлівае іх характэрныя хімічныя ўласцівасці, таму групу ![]() ОН называюць функцыянальнай групай. У малекулах спіртоў можа змяшчацца не адна, а дзве і больш гідраксільныя групы.
ОН называюць функцыянальнай групай. У малекулах спіртоў можа змяшчацца не адна, а дзве і больш гідраксільныя групы.
Спірты — арганічныя злучэнні, малекулы якіх змяшчаюць адну або некалькі гідраксільных груп, злучаных з вуглевадародным радыкалам.
Другое злучэнне адносіцца да класа простых эфіраў. У малекулах простых эфіраў няма гідраксільнай групы. Атам кіслароду ў малекулах простых эфіраў звязаны з двума вуглевадароднымі радыкаламі.
Этылавы спірт і дыметылавы эфір маюць аднолькавую малекулярную формулу, але розную будову. Такім чынам, яны з’яўляюцца ізамерамі.
Будова малекул спіртоў
У малекулах насычаных аднаатамных спіртоў маецца адна гідраксільная група ![]() ОН, злучаная з алкільным радыкалам.
ОН, злучаная з алкільным радыкалам.
Найпрасцейшым прадстаўніком насычаных аднаатамных спіртоў з’яўляецца метылавы спірт. Яго формула СН3 ![]() ОН. Метылавы спірт уяўляе сабой бясколерную вадкасць з характэрным пахам і тэмпературай кіпення 65 °С. Метылавы спірт надзвычай ядавіты. Пападанне ў арганізм чалавека ўсяго толькі 30 мл метылавага спірту можа прывесці да смерці. Яшчэ меншая колькасць метылавага спірту прыводзіць да страты зроку.
ОН. Метылавы спірт уяўляе сабой бясколерную вадкасць з характэрным пахам і тэмпературай кіпення 65 °С. Метылавы спірт надзвычай ядавіты. Пападанне ў арганізм чалавека ўсяго толькі 30 мл метылавага спірту можа прывесці да смерці. Яшчэ меншая колькасць метылавага спірту прыводзіць да страты зроку.
Бліжэйшы гамолаг метылавага спірту — этылавы спірт, формула якога СН3 ![]() СН2
СН2 ![]() ОН, ці С2Н5
ОН, ці С2Н5 ![]() ОН.
ОН.
Этылавы спірт — бясколерная вадкасць з характэрным пахам і тэмпературай кіпення 78 °С. Этылавы спірт уваходзіць у састаў алкагольных напояў. На жаль, многія людзі злоўжываюць алкагольнымі напоямі, наносячы непапраўную шкоду свайму здароўю. Злоўжыванне этылавым спіртам прыводзіць да цяжкага захворвання — алкагалізму.
Метылавы і этылавы спірты практычна немагчыма адрозніць па знешнім выглядзе і паху. У той жа час метылавы спірт значна больш таксічны, чым этылавы. У гэтым заключаецца асаблівая небяспека метылавага спірту. Ён можа прысутнічаць у розных тэхнічных спіртазмяшчальных вадкасцях. Бытавыя атручэнні метылавым спіртам часта звязаны з ужываннем такіх вадкасцей.
Саставім агульную формулу гамолагаў метылавага спірту. У іх малекулах група ![]() ОН злучана з алкільным радыкалам. Алкільны радыкал утвараецца ў выніку адрыву ад малекулы алкану аднаго атама вадароду. Агульная формула алканаў CnH2n+2. Калі выдаліць з малекулы адзін атам вадароду, атрымаецца формула алкільнага радыкала CnH2n+1
ОН злучана з алкільным радыкалам. Алкільны радыкал утвараецца ў выніку адрыву ад малекулы алкану аднаго атама вадароду. Агульная формула алканаў CnH2n+2. Калі выдаліць з малекулы адзін атам вадароду, атрымаецца формула алкільнага радыкала CnH2n+1 ![]() . Тады агульная формула гамолагаў метылавага спірту:
. Тады агульная формула гамолагаў метылавага спірту:
CnH2n+1 ![]() OH
OH
Ізамерыя спіртоў
Метылавы спірт не мае ізамераў. Этылавы спірт таксама не мае ізамераў, якія адносяцца да класа спіртоў. Адзіны ізамер этылавага спірту — дыметылавы эфір — з’яўляецца простым эфірам.
Наступныя прадстаўнікі рада насычаных аднаатамных спіртоў змяшчаюць тры атамы вугляроду ў малекуле (C3H7OH). У гэтым выпадку гідраксільная група можа быць звязана з першым або другім атамам вугляроду. Структурныя формулы ізамерных спіртоў:
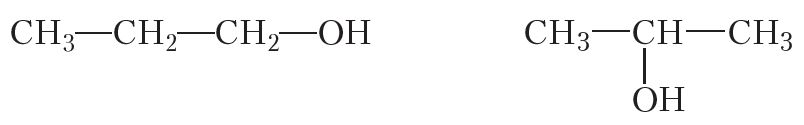
Гэтыя злучэнні з’яўляюцца ізамерамі становішча функцыянальнай групы.
Спірты, якія змяшчаюць чатыры атамы вугляроду ў малекуле (С4H9OH) таксама могуць адрознівацца становішчам функцыянальнай групы:
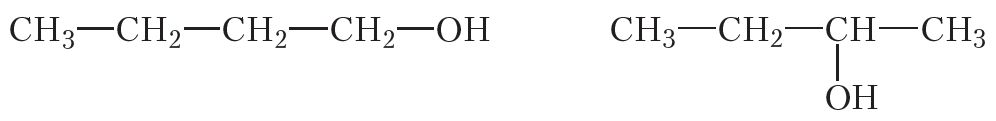
Акрамя таго, для іх магчыма ізамерыя вугляроднага шкілета:
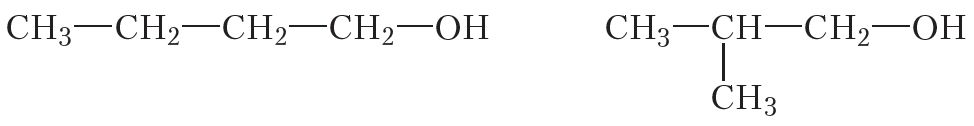
Улічваючы разгледжаныя віды ізамерыі, можна саставіць формулы чатырох ізамерных спіртоў саставу С4H9OH:
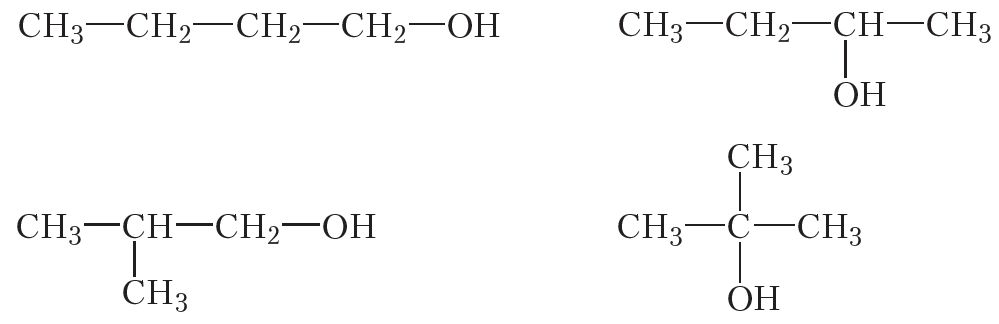
Відавочна, што з павелічэннем ліку атамаў вугляроду ў малекуле лік ізамераў будзе ўзрастаць.
Наменклатура спіртоў
Назва насычанага аднаатамнага спірту складаецца з назвы адпаведнага вуглевадароду і суфікса -ол, які абазначае гідраксільную групу. Атамы вугляроду галоўнага ланцуга нумаруюць, пачынаючы з таго канца, да якога бліжэй гідраксільная група. У канцы назвы ўказваюць становішча гідраксільнай групы ў галоўным ланцугу.
Назавём усе ўпамянутыя намі спірты. У дужках прыведзены трывіяльныя назвы некаторых спіртоў, якія шырока выкарыстоўваюцца нараўне з сістэматычнымі назвамі.
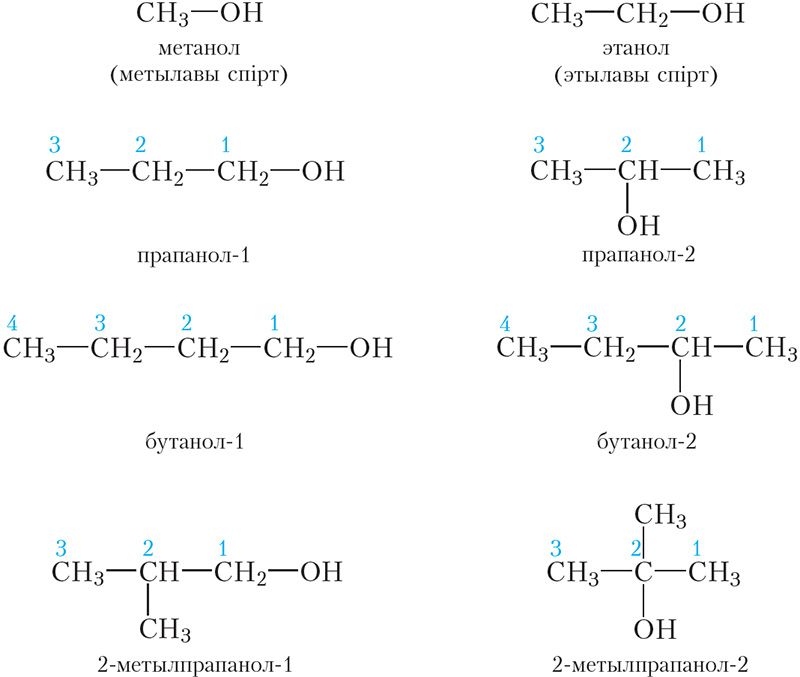
Атамы вугляроду ў малекулах арганічных рэчываў бываюць першаснымі, другаснымі, трацічнымі і чацвярцічнымі (§ 6). Першасны атам вугляроду злучаны толькі з адным атамам вугляроду, другасны — з двума, трацічны — з трыма і чацвярцічны — з чатырма атамамі вугляроду. У залежнасці ад таго, да якога атама вугляроду (першаснага, другаснага або трацічнага) далучана група ![]() OH, адрозніваюць першасныя, другасныя або трацічныя спірты.
OH, адрозніваюць першасныя, другасныя або трацічныя спірты.
З вышэйпералічаных спіртоў першаснымі з’яўляюцца этанол, прапанол-1, бутанол-1 і 2-метылпрапанол-1:
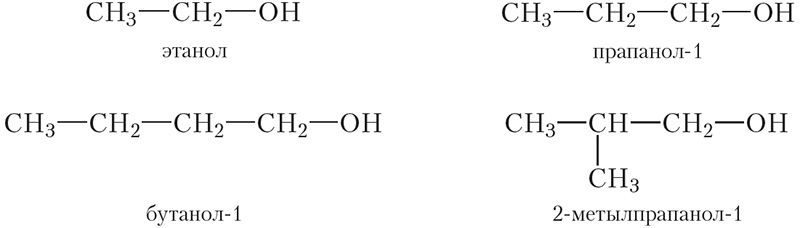
Другасныя спірты — прапанол-2, бутанол-2:

спірты
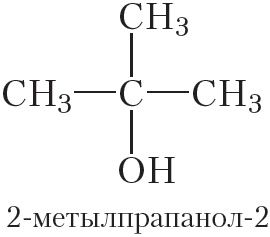
Прадстаўніком трацічных спіртоў з’яўляецца 2-метылпрапанол-2:
З ненасычанымі спіртамі вы можаце пазнаёміцца, перайшоўшы па спасылцы ў QR-кодзе.
Спірты — арганічныя злучэнні, малекулы якіх змяшчаюць адну або некалькі гідраксільных груп, злучаных з вуглевадародным радыкалам.
Наяўнасць гідраксільнай групы ў малекулах спіртоў абумоўлівае іх характэрныя хімічныя ўласцівасці. Таму групу ![]() OH называюць функцыянальнай групай.
OH называюць функцыянальнай групай.
Агульная формула насычаных аднаатамных спіртоў СnH2n+1 ![]() OH.
OH.
У залежнасці ад таго, да якога атама вугляроду (першаснага, другаснага ці трацічнага) далучана група ![]() OH, адрозніваюць першасныя, другасныя або трацічныя спірты.
OH, адрозніваюць першасныя, другасныя або трацічныя спірты.
*Ненасычаныя і араматычныя спірты
Акрамя насычаных спіртоў, існуюць таксама ненасычаныя спірты. Трэба адзначыць, што спірты, у малекулах якіх гідраксільная група звязана з атамам вугляроду, які ўтварае двайную сувязь, вельмі няўстойлівыя. Таму гідратацыя алкінаў прыводзіць спачатку да няўстойлівых ненасычаных спіртоў, якія ізамерызуюцца ў выпадку ацэтылену ў воцатны альдэгід, а ў выпадку прапіну — у ацэтон (§ 18-1). У той жа час існуюць і ўстойлівыя ненасычаныя спірты, напрыклад алілавы спірт:
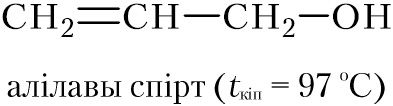
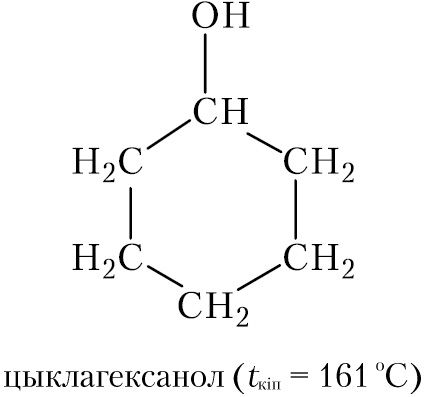
У малекулах спіртоў могуць мецца цыклы. Напрыклад, цыклагексанол:
Малекулы спіртоў могуць змяшчаць бензольнае кольца.
Такія спірты называюцца араматычнымі. Найпрасцейшы араматычны спірт — бензілавы спірт:
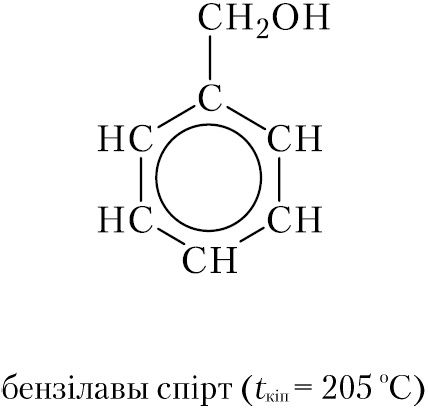
Неабходна адзначыць, што ў араматычных спіртах гідраксільная група не звязана непасрэдна з бензольным кольцам, а знаходзіцца ў бакавым ланцугу. Злучэнні, у малекулах якіх гідраксільная група непасрэдна звязана з бензольным кольцам, адносяцца да класса фенолаў. Уласцівасці фенолу мы будзем вывучаць пазней.
Пытанні і заданні
1. Напішыце агульную формулу гамалагічнага рада, да якога адносяцца метылавы і этылавы спірты. У чым заключаецца небяспека гэтых спіртоў для арганізма чалавека?
2. Адным з прадстаўнікоў класа простых эфіраў з’яўляецца дыэтылавы эфір С2Н5 ![]() О
О ![]() С2Н5. Дыэтылавы эфір — бясколерная вадкасць з характэрным пахам, мае тэмпературу кіпення, роўную 35 °С. Выкарыстоўваецца ў медыцыне для анестэзіі, прымяняецца ў якасці растваральніка. Прывядзіце формулы спіртоў, ізамерных дыэтылаваму эфіру.
С2Н5. Дыэтылавы эфір — бясколерная вадкасць з характэрным пахам, мае тэмпературу кіпення, роўную 35 °С. Выкарыстоўваецца ў медыцыне для анестэзіі, прымяняецца ў якасці растваральніка. Прывядзіце формулы спіртоў, ізамерных дыэтылаваму эфіру.
3. Прывядзіце назвы спіртоў, формулы якіх:
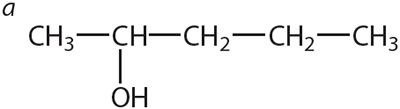
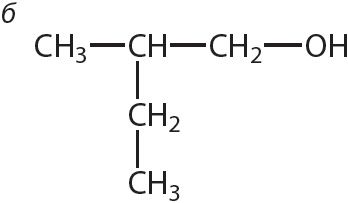
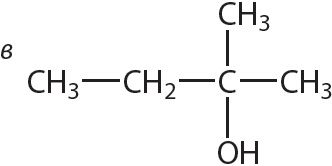
Знайдзіце сярод названых рэчываў першасны, другасны і трацічны спірты. Ці існуюць чацвярцічныя спірты?
4. Прывядзіце назвы спіртоў, шарастрыжнёвыя мадэлі малекул якіх:
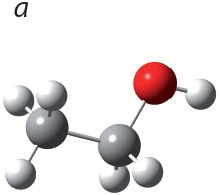
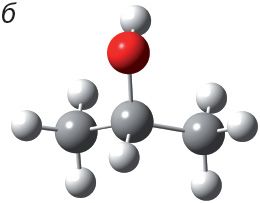
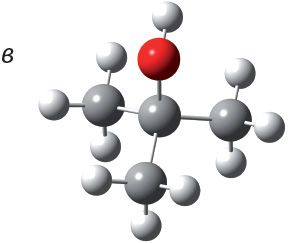
Знайдзіце сярод названых рэчываў першасны, другасны і трацічны спірты.
5. Напішыце структурныя формулы і назвы васьмі ізамерных спіртоў саставу С5H11OH. Аднясіце кожны з іх да першасных, другасных ці трацічных.
6*. Насычаныя аднаатамныя спірты і простыя эфіры з’яўляюцца міжкласавымі ізамерамі. Напішыце структурныя формулы спіртоў, ізамерных прапілэтылаваму эфіру, назавіце іх па наменклатуры ІЮПАК, укажыце першасныя, другасныя і трацічныя спірты.
