*§ 15-1. Далучэнне галагенавадародаў і вады да алкенаў. Правіла Маркоўнікава
Тлумачэнне правіла Маркоўнікава. Электронадонарныя і электронаакцэптарныя замяшчальнікі
Правіла Маркоўнікава тлумачыцца ўплывам замяшчальнікаў на электроны π-сувязі. Па гэтай прыкмеце ўсе замяшчальнікі можна падзяліць на дзве групы:
1. Замяшчальнікі, якія прыцягваюць электроны π-сувязі. Такія замяшчальнікі называюцца электронаакцэптарнымі (ад англ. to аccept — прымаць). Прыклады электронаакцэптарных замяшчальнікаў: карбаксільная група ![]() COOH і нітрагрупа
COOH і нітрагрупа ![]() NO2. Зрушэнне электронаў π-сувязі пад дзеяннем электронаакцэптарнага замяшчальніка паказана на малюнку 15-1.2:
NO2. Зрушэнне электронаў π-сувязі пад дзеяннем электронаакцэптарнага замяшчальніка паказана на малюнку 15-1.2:
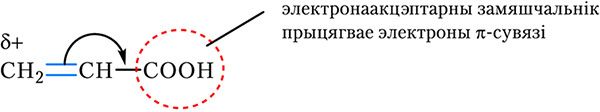
 С пад дзеяннем электронаакцэптарнага замяшчальніка
С пад дзеяннем электронаакцэптарнага замяшчальніка 2. Замяшчальнікі, якія адштурхваюць электроны π-сувязі (электронадонарныя замяшчальнікі). Да электронадонарных замяшчальнікаў адносяцца алкільныя радыкалы ![]() CH3,
CH3, ![]() C2H5 і інш., гідраксільная група
C2H5 і інш., гідраксільная група ![]() OH і амінагрупа
OH і амінагрупа ![]() NH2. Зрушэнне электронаў π-сувязі пад дзеяннем электронадонарнага замяшчальніка паказана на малюнку 15-1.3:
NH2. Зрушэнне электронаў π-сувязі пад дзеяннем электронадонарнага замяшчальніка паказана на малюнку 15-1.3:
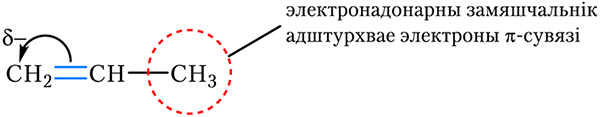
 С пад дзеяннем электронадонарнага замяшчальніка
С пад дзеяннем электронадонарнага замяшчальніка Разгледзім далучэнне хлоравадароду да прапену з улікам уплыву замяшчальнікаў на электроны π-сувязі:
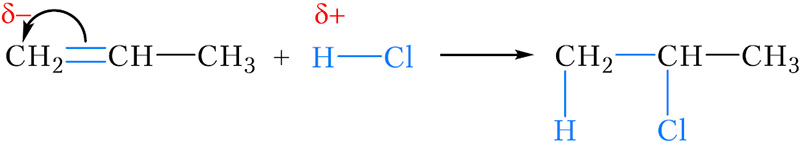
Дадатна зараджаны атам вадароду малекулы хлоравадароду далучаецца да атама вугляроду двайной сувязі, што нясе адмоўны зарад. Гэтым атамам вугляроду з’яўляецца больш гідрагенізаваны атам C(1), што адпавядае правілу Маркоўнікава.
Далучэнне галагенавадародаў і вады да несіметрычных алкенаў працякае па правілу Маркоўнікава — вадарод далучаеца да больш гідрагенізаванага атама вугляроду двайной сувязі.
Правіла Маркоўнікава тлумачыцца ўплывам замяшчальнікаў на электроны π-сувязі. Электронаакцэптарныя замяшчальнікі (![]() СООН,
СООН, ![]() NО2) прыцягваюць электроны π-сувязі, электронадонарныя (алкільныя радыкалы,
NО2) прыцягваюць электроны π-сувязі, электронадонарныя (алкільныя радыкалы, ![]() ОН,
ОН, ![]() NН2) — адштурхваюць.
NН2) — адштурхваюць.