*§ 15-1. Далучэнне галагенавадародаў і вады да алкенаў. Правіла Маркоўнікава
| Сайт: | Профильное обучение |
| Курс: | Хімія. 10 клас |
| Книга: | *§ 15-1. Далучэнне галагенавадародаў і вады да алкенаў. Правіла Маркоўнікава |
| Напечатано:: | Гость |
| Дата: | Среда, 2 Июль 2025, 20:06 |
Правіла Маркоўнікава
Рэакцыі далучэння галагенавадародаў і вады да гамолагаў этылену маюць некаторыя асаблівасці.
Далучэнне галагенавадародаў. Гідрагалагенаванне
Разгледзім рэакцыю далучэння хлоравадароду да прапену. У выніку гэтай рэакцыі, у прынцыпе, магчыма ўтварэнне двух прадуктаў — 2-хлорпрапану i 1-хлорпрапану:
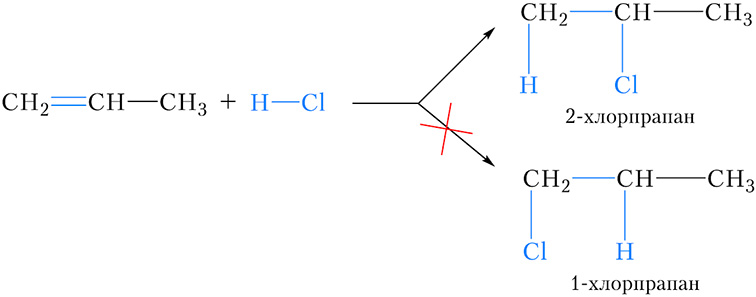
У рэчаіснасці, пераважным прадуктам гэтай рэакцыі з’яўляецца 2-хлорпрапан.
Тая самая з’ява (утварэнне аднаго з двух магчымых прадуктаў) назіраецца пры далучэнні хлоравадароду да метылпрапену:
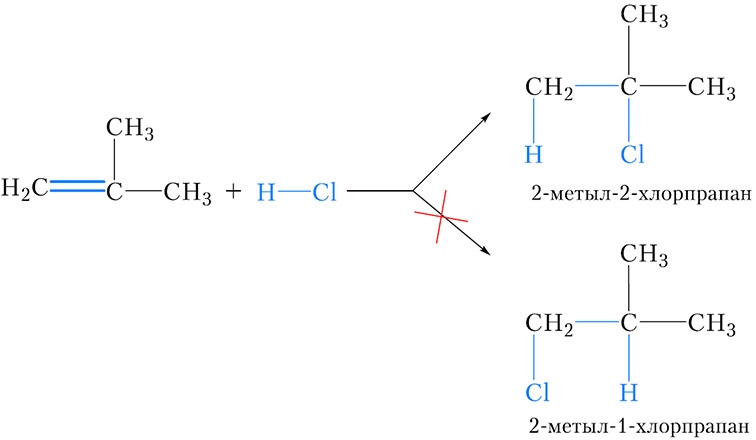
Можна заўважыць, што ў абодвух выпадках вадарод далучаецца да таго атама вугляроду двайной сувязі, з якім злучаны большы лік атамаў вадароду (больш гідрагенізаванаму атаму вугляроду). Гэта заканамернасць называецца правілам Маркоўнікава.
У якасці яшчэ адной ілюстрацыі правіла Маркоўнікава запішам ураўненне рэакцыі далучэння хлоравадароду да метылбутэну-2:
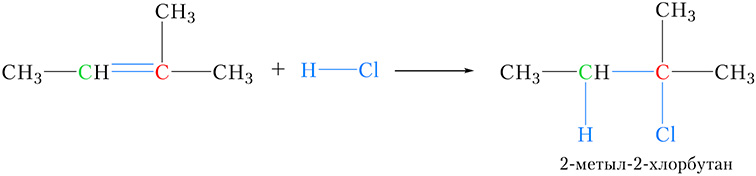
Атам вугляроду, выдзелены зялёным колерам, злучаны з адным атамам вадароду, у той час як у другога атама вугляроду двайной сувязі (выдзелены чырвоным колерам) атамы вадароду адсутнічаюць. У адпаведнасці з правілам Маркоўнікава вадарод далучаецца да больш гідрагенізаванага атама вугляроду.
Далучэнне вады. Гідратацыя
Далучэнне вады да прапену і іншых несіметрычных алкенаў таксама працякае ў адпаведнасці з правілам Маркоўнікава:
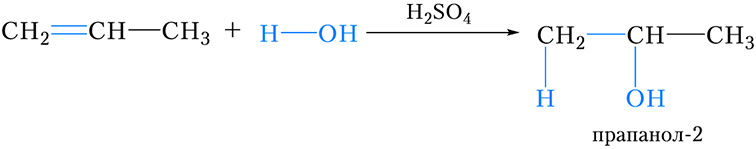
Правіла Маркоўнікава. Пры далучэнні галагенавадародаў і вады да алкенаў атам вадароду далучаецца да больш гідрагенізаванага атама вугляроду двайной сувязі.

Цікава ведаць
Правіла Маркоўнікава носіць імя яго першаадкрывальніка — рускага хіміка Уладзіміра Васільевіча Маркоўнікава, вучня А. М. Бутлерава. У. В. Маркоўнікаў зрабіў значны ўклад у развіццё палажэнняў тэорыі будовы арганічных злучэнняў, якія тычацца ізамерыі і ўзаемнага ўплыву атамаў у малекулах арганічных рэчываў. У. В. Маркоўнікаў адкрыў цыклаалканы ў саставе каўказскіх нафтаў, вядомы яго працы па даследаванні саставу саляных крыніц і саляных азёр Расіі.
Тлумачэнне правіла Маркоўнікава. Электронадонарныя і электронаакцэптарныя замяшчальнікі
Правіла Маркоўнікава тлумачыцца ўплывам замяшчальнікаў на электроны π-сувязі. Па гэтай прыкмеце ўсе замяшчальнікі можна падзяліць на дзве групы:
1. Замяшчальнікі, якія прыцягваюць электроны π-сувязі. Такія замяшчальнікі называюцца электронаакцэптарнымі (ад англ. to аccept — прымаць). Прыклады электронаакцэптарных замяшчальнікаў: карбаксільная група ![]() COOH і нітрагрупа
COOH і нітрагрупа ![]() NO2. Зрушэнне электронаў π-сувязі пад дзеяннем электронаакцэптарнага замяшчальніка паказана на малюнку 15-1.2:
NO2. Зрушэнне электронаў π-сувязі пад дзеяннем электронаакцэптарнага замяшчальніка паказана на малюнку 15-1.2:
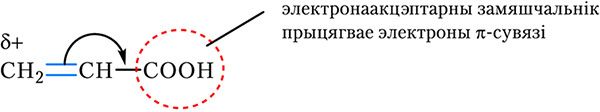
 С пад дзеяннем электронаакцэптарнага замяшчальніка
С пад дзеяннем электронаакцэптарнага замяшчальніка 2. Замяшчальнікі, якія адштурхваюць электроны π-сувязі (электронадонарныя замяшчальнікі). Да электронадонарных замяшчальнікаў адносяцца алкільныя радыкалы ![]() CH3,
CH3, ![]() C2H5 і інш., гідраксільная група
C2H5 і інш., гідраксільная група ![]() OH і амінагрупа
OH і амінагрупа ![]() NH2. Зрушэнне электронаў π-сувязі пад дзеяннем электронадонарнага замяшчальніка паказана на малюнку 15-1.3:
NH2. Зрушэнне электронаў π-сувязі пад дзеяннем электронадонарнага замяшчальніка паказана на малюнку 15-1.3:
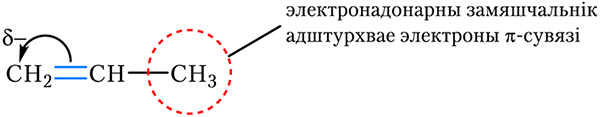
 С пад дзеяннем электронадонарнага замяшчальніка
С пад дзеяннем электронадонарнага замяшчальніка Разгледзім далучэнне хлоравадароду да прапену з улікам уплыву замяшчальнікаў на электроны π-сувязі:
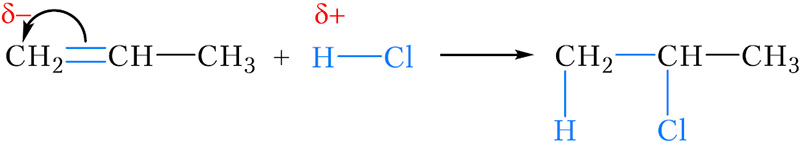
Дадатна зараджаны атам вадароду малекулы хлоравадароду далучаецца да атама вугляроду двайной сувязі, што нясе адмоўны зарад. Гэтым атамам вугляроду з’яўляецца больш гідрагенізаваны атам C(1), што адпавядае правілу Маркоўнікава.
Далучэнне галагенавадародаў і вады да несіметрычных алкенаў працякае па правілу Маркоўнікава — вадарод далучаеца да больш гідрагенізаванага атама вугляроду двайной сувязі.
Правіла Маркоўнікава тлумачыцца ўплывам замяшчальнікаў на электроны π-сувязі. Электронаакцэптарныя замяшчальнікі (![]() СООН,
СООН, ![]() NО2) прыцягваюць электроны π-сувязі, электронадонарныя (алкільныя радыкалы,
NО2) прыцягваюць электроны π-сувязі, электронадонарныя (алкільныя радыкалы, ![]() ОН,
ОН, ![]() NН2) — адштурхваюць.
NН2) — адштурхваюць.
Пытанні і заданні
1. Напішыце ўраўненне рэакцыі ўзаемадзеяння бутэну-1 з хлоравадародам. Чаму ў выніку гэтай рэакцыі ўтвараецца толькі адзін прадукт?
2. Напішыце ўраўненне рэакцыі гідратацыі 2-метылпрапену.
3. Напішыце ўраўненне рэакцыі далучэння бромавадароду да рэчыва, формула якога:
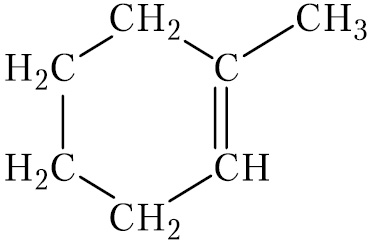
4. Прадкажыце прадукт наступнай рэакцыі:
CH2 ![]() CH
CH ![]() CH3 + ICl
CH3 + ICl ![]()
5. Прадкажыце прадукт наступнай рэакцыі:
CH2 ![]() CH
CH ![]() COOH + HCl
COOH + HCl ![]()