§ 4. Кавалентная сувязь
Кратнасць кавалентнай сувязі
На знешнім слоі атама фтору маецца адзін няспараны электрон, таму валентнасць фтору ў злучэннях роўная адзінцы.
![]()
Ад сімвала F у структурных формулах трэба маляваць адну рысачку: F ![]() F, H
F, H ![]() F.
F.
На малюнку 4.2 паказана схема ўтварэння кавалентнай сувязі ў малекуле фтору:

У малекуле фтору атамы звязвае адна агульная электронная пара. Такая сувязь называецца адзінарнай.
На знешнім слоі атама кіслароду маюцца два няспараныя электроны, таму валентнасць кіслароду ў злучэннях роўная двум.
![]()
Ад сімвала O ў структурных формулах трэба маляваць дзве рысачкі: O ![]() O, H
O, H ![]() O
O ![]() H.
H.
На малюнку 4.3 паказана схема ўтварэння кавалентнай сувязі ў малекуле кіслароду:

У малекуле кіслароду атамы звязваюць дзве электронныя пары. Такая сувязь называецца двайной. Двайная сувязь больш трывалая, чым адзінарная.
На знешнім слоі атама азоту маецца тры няспараныя электроны, таму валентнасць азоту ў злучэннях роўная тром.
![]()
Ад сімвала N у структурных формулах трэба маляваць тры рысачкі:
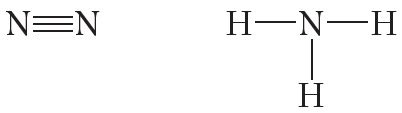
На малюнку 4.4 паказана схема ўтварэння кавалентнай сувязі ў малекуле азоту:

У малекуле азоту атамы звязваюць тры электронныя пары. Такая сувязь называецца трайной. Трайная сувязь больш трывалая, чым адзінарная і двайная.
Двайныя і трайныя сувязі маюць агульную назву кратныя.
У асноўным стане на знешнім слоі атама вугляроду маецца два няспараных электроны. Аднак атам вугляроду лёгка пераходзіць ва ўзбуджаны стан, у якім маецца чатыры няспараныя электроны:
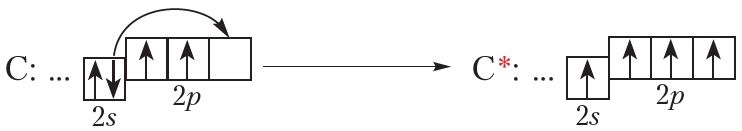
У сувязі з гэтым валентнасць вугляроду можа быць роўная чатыром. У большасці злучэнняў вуглярод чатырохвалентны. Таму ў структурных формулах ад сімвала C трэба маляваць чатыры рысачкі:
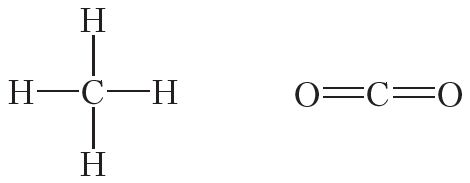
Атамы вугляроду могуць звязвацца паміж сабой як адзінарнымі, так і кратнымі сувязямі. Напрыклад, у малекуле этану, які мае састаў С2Н6, атамы вугляроду ўтвараюць толькі адзінарныя сувязі:
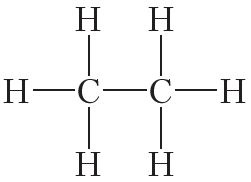
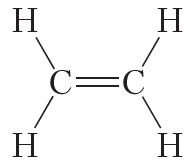
Двайной кавалентнай сувяззю атамы вугляроду злучаны паміж сабой у малекуле этылену (С2Н4):
Трайная сувязь паміж атамамі вугляроду маецца ў малекуле ацэтылену (С2Н2):
![]()