§ 10. Химические свойства, получение и применение алканов
Химические свойства, получение и применение алканов
Существует огромное число различных алканов. Их многообразие объясняется как возможностью образования углеродных цепей различной длины, так и изомерией. В связи с этим изучать химические свойства каждого алкана отдельно не представляется возможным. В то же время молекулы различных алканов имеют сходное строение: атомы углерода соединены между собой и атомами водорода одинарными ковалентными связями. Учитывая это, можно ожидать, что химические свойства различных алканов будут во многом сходными.
Все алканы характеризуются низкой химической активностью. Они не взаимодействуют с растворами кислот, оснований, солей. На них не действует такой сильный окислитель, как KMnO4, и такие сильные восстановители, как щелочные металлы. Вы знаете, что щелочные металлы очень активны и реагируют практически со всеми веществами, с которыми соприкасаются, в том числе легко окисляются кислородом воздуха. Чтобы уберечь щелочные металлы от окисления, их хранят под слоем керосина — смеси, состоящей в основном из насыщенных углеводородов. При этом алканы, входящие в состав керосина, не реагируют со щелочными металлами.
Из-за низкой химической активности алканов реакции с их участием протекают в жёстких условиях (при нагревании или облучении ультрафиолетовым излучением).
Мы изучим реакции алканов с галогенами (Cl2 и Br2) и кислородом (O2), а также превращения, которые они претерпевают при нагревании.
1. Галогенирование. Взаимодействие с галогенами
Взаимодействие алканов с галогенами — хлором и бромом — протекает при нагревании или облучении ультрафиолетовым излучением.
Если смесью газообразных метана и хлора заполнить стеклянный сосуд и поместить его в тёмное место, реакция протекать не будет. Однако при нагревании смеси или облучении её ультрафиолетовым излучением протекает химическая реакция замещения атомов водорода в молекуле метана на атомы хлора:
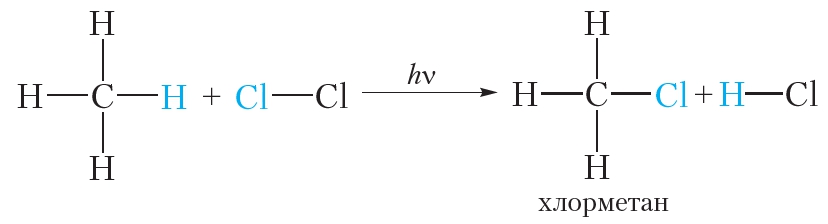
В уравнениях реакций, протекающих при облучении, над стрелкой записывают буквы hv. Данная реакция называется реакцией галогенирования и относится к реакциям замещения.
Если только один атом водорода в молекуле замещается на атом галогена, то реакцию называют моногалогенированием. Приведённая выше реакция является реакцией монохлорирования метана. В избытке хлора оставшиеся три атома водорода молекулы метана могут последовательно замещаться на галоген:
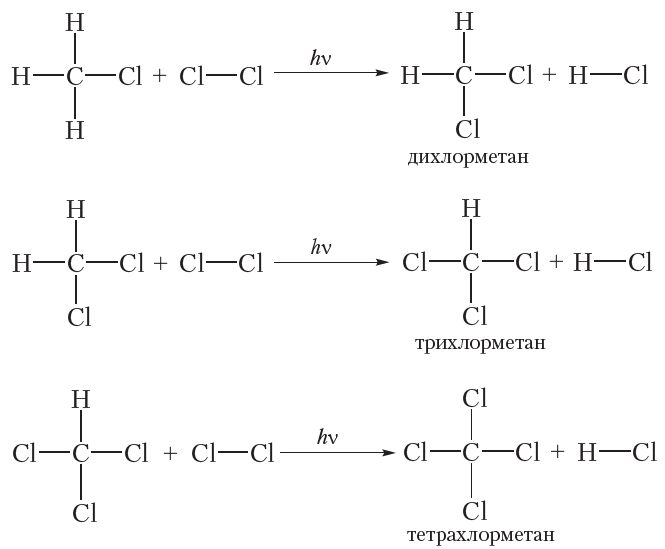
Приведём уравнения реакций всех четырёх стадий хлорирования метана с использованием молекулярных формул:
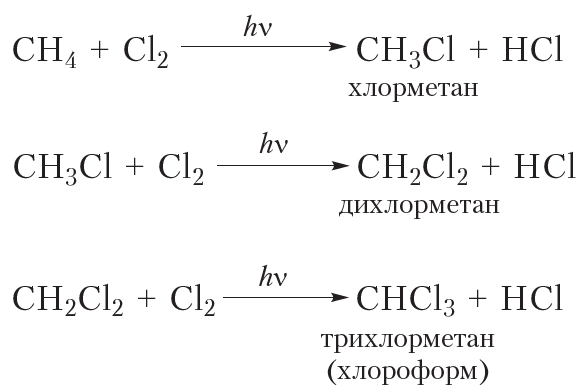
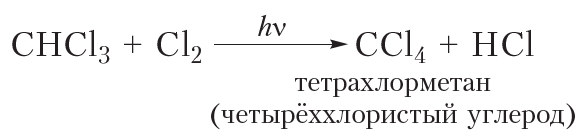
Рассмотрим реакции монохлорирования гомологов метана.
Монохлорирование этана
Для этана уравнение реакции следующее:
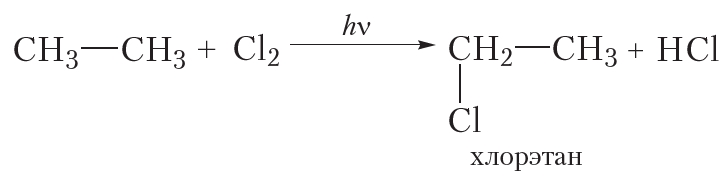
Отметим, что в названии «хлорэтан» нет необходимости указывать цифрой положение атома хлора. Это связано с тем, что при замещении любого атома водорода в молекуле этана на атом хлора образуется одно и то же вещество:

Таким образом, при монохлорировании этана так же, как и в случае метана, получается только одно органическое вещество — хлорэтан.
Монохлорирование пропана
При монохлорировании пропана образуется смесь двух органических веществ:
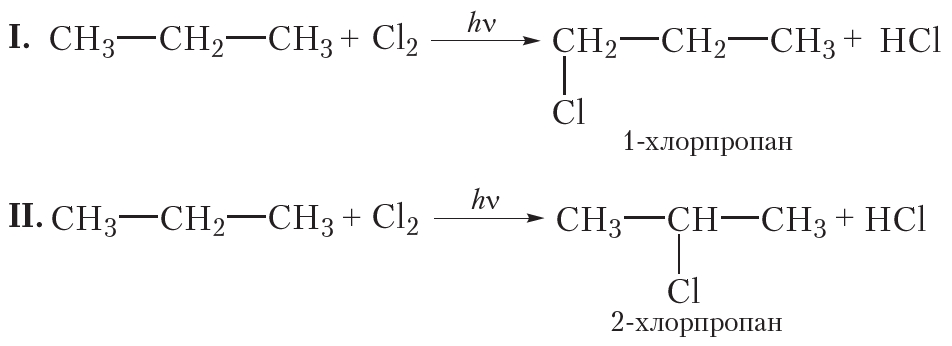
В случае I происходит замещение на галоген атома водорода при первом атоме углерода, продукт реакции 1-хлорпропан. В случае II замещается атом водорода при втором атоме углерода, продуктом реакции является 2-хлорпропан. Обратите внимание на то, что при построении названий нумерацию атомов углерода начинают с того конца углеродной цепи, к которому ближе расположен атом хлора.
В результате реакции монохлорирования пропана образуются два продукта: 1-хлорпропан и 2-хлорпропан, имеющие одинаковые молекулярные формулы C3H7Cl. Это неудивительно, ведь 1-хлорпропан и 2-хлорпропан — изомеры.
Если мы запишем уравнение реакции монохлорирования пропана с использованием молекулярных формул, оно будет выглядеть следующим образом:
![]()
Уравнение реакции, записанное в таком виде, не только не позволяет определить, какой именно продукт (1-хлорпропан или 2-хлорпропан) имеется в виду, но и приводит к распространённому заблуждению, что при монохлорировании пропана образуется только один органический продукт — C3H7Cl, хотя на самом деле их два. Поэтому в органической химии при записи уравнений реакций обычно используют структурные, а не молекулярные формулы веществ.
В результате хлорирования алканов происходит замещение одного или нескольких атомов водорода в молекуле алкана на атомы галогена. Поэтому получающиеся органические вещества называют галогенпроизводными алканов.
Пример. Замещение двух атомов водорода хлором в молекуле этана.
Реакция протекает в два этапа.
а) Первая стадия хлорирования этана. На первой стадии происходит замещение одного атома водорода. При этом образуется только одно органическое вещество — хлорэтан:

б) Вторая стадия хлорирования этана. На данной стадии происходит взаимодействие молекулы хлора с молекулой хлорэтана, образовавшегося на первой стадии. Очевидно, что при этом могут образоваться два органических вещества:
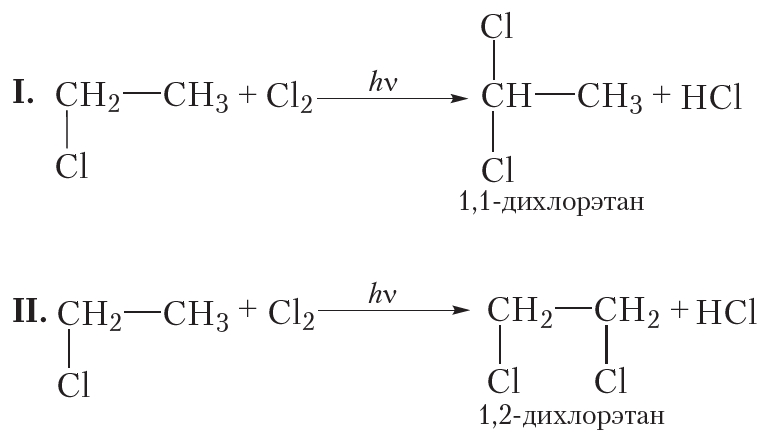
Действительно, в результате хлорирования этана можно получить смесь двух дихлорпроизводных.
Алканы вступают в реакции замещения также с бромом. Например:
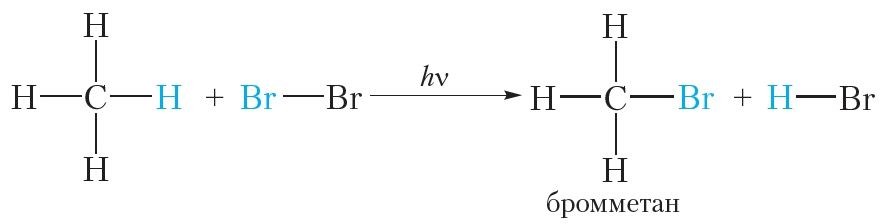
 В заключение ещё раз обратим внимание, что реакции алканов с хлором и бромом протекают в жёстких условиях: при облучении или нагревании.
В заключение ещё раз обратим внимание, что реакции алканов с хлором и бромом протекают в жёстких условиях: при облучении или нагревании.
С механизмом реакции галогенирования алканов вы можете познакомиться, перейдя по ссылке в QR-коде.
В реакциях галогенирования атомы водорода в молекуле алкана замещаются на атомы галогена, при этом углеродная цепь молекулы сохраняется. В других реакциях алканов их углеродный скелет изменяется или полностью разрушается. Рассмотрим такие реакции.
2. Пиролиз
При сильном нагревании алканов в их молекулах происходит разрыв связей ![]() и
и ![]() . В результате молекулы алканов могут быть полностью разрушены с образованием углерода и водорода. Разложение веществ при высоких температурах называют пиролизом (от греч. пиро — огонь, жар и лизис — разложение, распад). Например:
. В результате молекулы алканов могут быть полностью разрушены с образованием углерода и водорода. Разложение веществ при высоких температурах называют пиролизом (от греч. пиро — огонь, жар и лизис — разложение, распад). Например:
![]()
Общая схема реакции пиролиза алканов (n — число атомов углерода в молекуле алкана):
![]()
Эту реакцию используют в промышленности для получения сажи и водорода.
3. Изомеризация
Ещё одним химическим свойством алканов является изомеризация, то есть превращение одного изомера в другой. Это свойство возможно для алканов, начиная с бутана, так как метан, этан и пропан изомеров не имеют. Реакция изомеризации протекает при пропускании алкана через реактор, нагретый до высокой температуры, в присутствии катализатора. При этом молекулы алканов линейного строения превращаются в молекулы разветвлённого строения, например реакция изомеризации н-бутана:
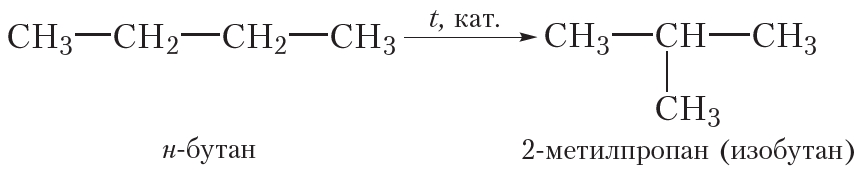
4. Горение. Взаимодействие с кислородом
Важнейшее свойство алканов — горение. Алканы воспламеняются при поджигании. Уравнение реакции горения метана:
![]()
Эта реакция вам хорошо знакома, она протекает при поджигании газа в кухонной газовой плите, ведь метан — основной компонент природного газа. Смесью пропана и изомерных бутанов наполняют газовые баллоны. Уравнения реакций горения этих алканов:
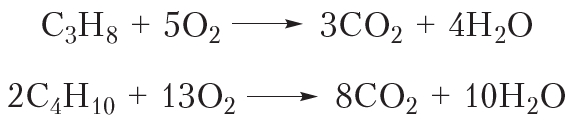
Последующие члены гомологического ряда алканов также горят при поджигании. Можно записать общее уравнение реакции горения:
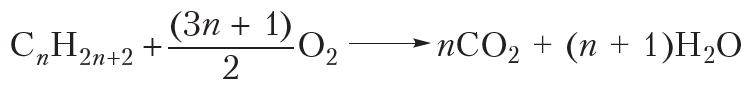
Видно, что при горении атомы водорода из молекулы алкана переходят в молекулы воды, а атомы углерода — в молекулы углекислого газа. Если горение алкана происходит в условиях недостатка кислорода, то, наряду с углекислым газом (СО2), может образоваться угарный газ (СО) или углерод (С) в виде сажи:
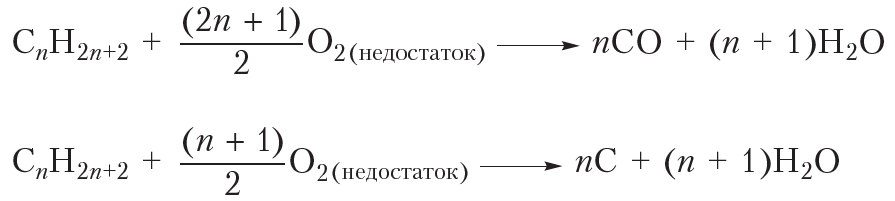
Отметим, что свойство гореть в кислороде присуще почти всем органическим соединениям. Поскольку все органические вещества содержат углерод, то при их горении могут образовываться оксиды углерода и сажа.
Образование угарного газа (CO) при неполном сгорании органического вещества смертельно опасно из-за высокой токсичности СО. Отравление угарным газом может произойти при неправильной эксплуатации печей и каминов.
Как видно, химические свойства алканов не отличаются большим разнообразием. Для них характерны в основном реакции окисления (в частности, горения), разложения и изомеризации при высокой температуре, а также реакции замещения, в результате которых получают галогенпроизводные алканов.