§ 25. Электралітычная дысацыяцыя рэчываў у растворах
Дысацыяцыя злучэнняў з іонным тыпам сувязі
Іонныя крышталі складаюцца з катыёнаў і аніёнаў, звязаных паміж сабой сіламі электрастатычнага ўзаемадзеяння ў спарадкаваную крышталічную структуру. Пад уздзеяннем палярных малекул вады адбываецца разбурэнне іонных крышталёў і іх растварэнне з утварэннем гідратаў іонаў (мал. 57).
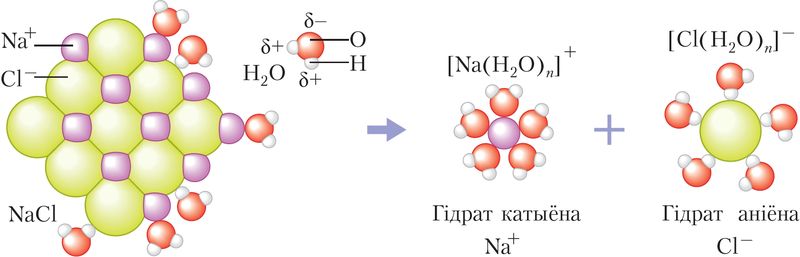
Разгледзьце малюнак 57 і звярніце ўвагу на адносны памер катыёнаў Na+, аніёнаў Cl–, малекул вады, а таксама знакі частковых зарадаў на атамах H і O ў малекуле вады. Звярніце ўвагу на тое, якім атамам малекула вады павернута да катыёнаў Na+, а якім — да аніёнаў Cl–. Чаму малекула вады арыентавана да катыёнаў Na+ атамам кіслароду, а да аніёнаў Cl– — атамам вадароду?
Асаблівасцю дысацыяцыі іонных злучэнняў (солей і шчолачаў) з’яўляецца тое, што гэтыя рэчывы ўжо складаюцца з іонаў і палярныя малекулы вады толькі падзяляюць катыёны і аніёны. Затрачаная на дысацыяцыю энергія кампенсуецца вылучэннем энергіі пры гідратацыі іонаў, і ў цэлым працэс працякае самаадвольна.
З’яўляючыся добра растваральнымі ў вадзе асновамі, шчолачы дысацыіруюць у водных растворах на гідраксід-аніёны і катыёны металу:
У выніку дысацыяцыі солей у вадзе іх іонныя крышталі распадаюцца на катыёны металаў (або амонію) і аніёны кіслотных астаткаў: