§ 38. Азотная кіслата
Нітраты
Солі азотнай кіслаты ўсе без выключэння добра растваральныя ў вадзе. Найважнейшая хімічная ўласцівасць нітратаў — іх здольнасць раскладацца пры награванні з утварэннем кіслароду. Састаў утвораных прадуктаў залежыць ад актыўнасці металу.
1. Нітраты шчолачных і шчолачназямельных металаў утвараюць нітрыт і кісларод:
.
2. Нітраты металаў, размешчаных у радзе актыўнасці ад магнію да медзі, раскладаюцца з утварэннем аксіду металу, аксіду азоту(IV) і кіслароду:
.
3. Нітраты металаў, размешчаных у радзе актыўнасці пасля медзі, пры раскладанні ўтвараюць метал, аксід азоту(IV) і кісларод:
.
Тэрмічнае раскладанне нітратаў можна паказаць схемай:
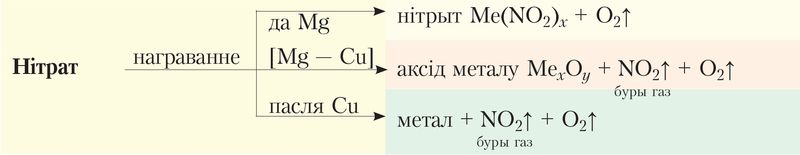
Вылучэнне кіслароду пры раскладанні дазваляе выявіць нітрат па «ўспышцы цвёрдай солі на распаленых вугольчыках» (Дадатак 3).
Варта адзначыць, што нітрат амонію, раскладаючыся пры тэмпературы не вышэйшай за 200 °С, кіслароду не ўтварае:
.
Выкарыстанне нітратаў. Нітраты натрыю, калію, кальцыю, амонію (NaNO3, KNO3, Са(NO3)2, NH4NO3) называюць салетрамі і выкарыстоўваюць у якасці ўгнаенняў. Яшчэ адзін важны напрамак выкарыстання нітратаў — піратэхніка: нітраты раскладаюцца пры награванні з вылучэннем кіслароду, які з’яўляецца моцным акісляльнікам, асабліва ў момант вылучэння. Кісларод пры гэтым служыць акісляльнікам іншых кампанентаў пораху.
Раскладанне нітрату натрыю можна выкарыстоўваць у лабараторыі для атрымання кіслароду:
(прадукты — кісларод і нітрыт натрыю — соль слабай азоцістай кіслаты).
Нітрат серабра(I) — складовую частку ляпісу — выкарыстоўваюць у медыцынскіх мэтах. У харчовай прамысловасці выкарыстоўваюць нітрат і нітрыт натрыю як кансерванты (Е251, Е250) для сыроў і каўбасных вырабаў. Мясным вырабам гэтыя солі надаюць яркі ружова-чырвоны колер. Гэтымі солямі карысталіся яшчэ старажытныя грэкі і егіпцяне.