§ 29.2. Пероксид водорода
Самоконтроль
1. Схема образования водородной связи между молекулами воды и пероксида водорода:
а) 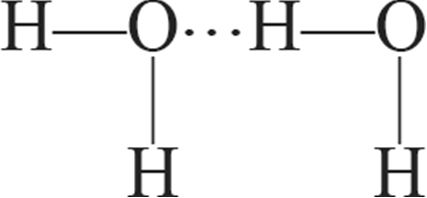
б) 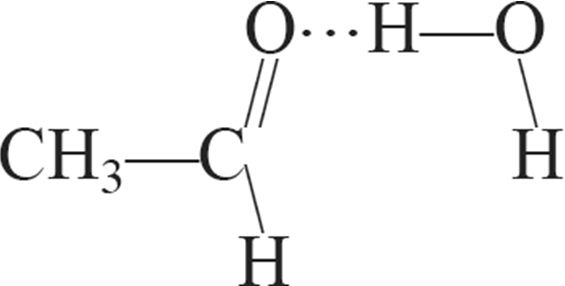

в) 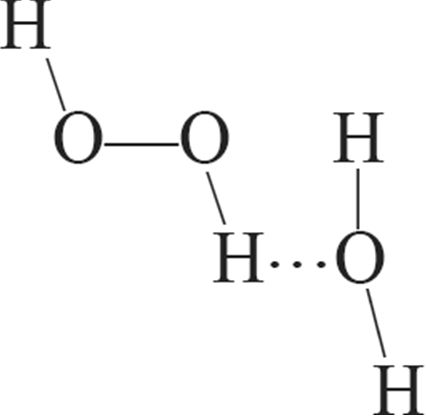

г)
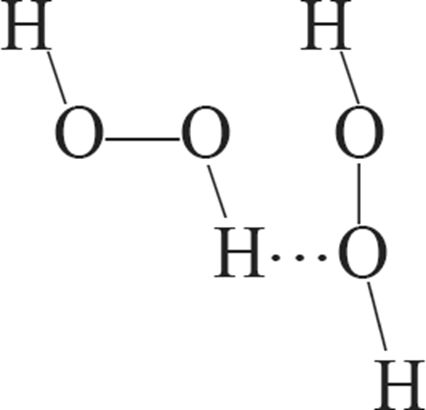
2. Сумма коэффициентов в уравнении реакции Н2О2 + PbS → H2O + PbSO4 равна:
- а) 6;
- б) 9;
- в) 10;
- г) 14.
3. Степень окисления –1 имеют атомы кислорода в соединениях:
- а) Na2О2;
- б) Н2О2;
- в) СаО2;
- г) K2О.
4. Пероксид водорода образуется в реакциях, схемы которых:
- а) ВаО2 + НCl →;
- б) ВаО2 + H2SO4 →;
- в) Н2О2 + KMnO4 →;
- г) Н2О2 + H2S →.
5. Относительно пероксида водорода верными являются утверждения:
- а) молекула Н2О2 линейна;
- б) в молекуле содержатся две полярные и одна неполярная ковалентная связь;
- в) проявляет окислительные свойства по отношению к NaI;
- г) можно использовать для получения кислорода в лаборатории.