§ 29.2. Пероксид водорода
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 29.2. Пероксид водорода |
| Напечатано:: | Гость |
| Дата: | Wednesday, 10 June 2026, 01:10 |

Пероксид водорода Н2О2 — вещество молекулярного строения, структурная формула которого Н—О—О—Н. Строение молекулы показано на рисунке 67.2.
Энергия связи Н—О составляет 468 кДж/моль и почти в два раза выше энергии связи О—О (210 кДж/моль). Молекула несимметрична и полярна. Между молекулами существуют водородные связи.
Физические свойства
При комнатной температуре пероксид водорода — бледно-голубая сиропообразная жидкость. По сравнению с водой она имеет более высокие температуры кипения и плавления: tкип. = 150,2 °С, tпл. = 0,41 °С. Смешивается с водой в любых соотношениях, чему способствует образование водородных связей с молекулами воды. Раствор с массовой долей H2O2 30 % называют пергидролем. В быту обычно используют 3%-ный раствор.
Химические свойства
Пероксид водорода проявляет слабо выраженные кислотные свойства, а также вступает в окислительно-восстановительные реакции. В окислительно-восстановительных реакциях кислород, имея промежуточную степень окисления –1, может её либо понижать до –2, играя роль окислителя, либо повышать до 0, выступая восстановителем.
1. Раствор пероксида водорода имеет кислую реакцию среды, что объясняется образованием ионов водорода Н+ (гидроксония (Н3О+):
или
Пероксид водорода — очень слабая кислота. Как кислота H2O2 реагирует с некоторыми щелочами (например, Ba(OH)2):
Н2О2 + Ва(ОН)2 = ВаО2 + 2Н2О (пероксид бария).
2. При хранении на свету, а также нагревании, в присутствии катализаторов (например, MnO2) H2O2 разлагается на кислород и воду:
,
поэтому пероксид водорода и его растворы хранят в тёмной посуде на холоде, для стабилизации добавляют ингибиторы.
3. В реакциях с восстановителями (например, ) атомы кислорода понижают степень окисления:
;
.
4. В реакциях с сильными окислителями (например, KMnO4) атомы кислорода повышают степень окисления:
Получение. Пероксид водорода в лаборатории можно получить действием серной кислоты на пероксиды металлов:
BaО2 + H2SO4 = BaSO4↓ + Н2О2.
Применение. Водные растворы пероксида водорода используют как антисептик в медицине, как окислитель ракетного топлива, для отбеливания тканей, в косметических средствах для окраски волос. Его действие обусловлено разложением под действием теплоты, света, а также некоторых других веществ с выделением кислорода. Из пероксида водорода получают другие пероксиды.
Пероксид водорода Н2О2 проявляет слабо выраженные кислотные свойства. В окислительно-восстановительных реакциях пероксид водорода выступает как восстановитель и как окислитель.
Вопросы, задания, задачи
1. Выпишите формулы пероксидов: Н2О, Н2О2, Na2О2, OF2, BaО2, CO2.
2. Составьте электронную и структурную формулы пероксида водорода.
3. Дайте характеристику химических связей в молекуле пероксида водорода.
4. Запишите уравнение реакции разложения пероксида водорода в присутствии оксида марганца(IV). Охарактеризуйте реакцию с точки зрения процессов окисления и восстановления.
5. К раствору пероксида водорода массой 75 г добавили небольшую порцию оксида марганца(IV). В результате полного разложения пероксида водорода выделился газ объёмом 0,5 дм3. Какова массовая доля пероксида в исходном растворе?
6. Расставьте коэффициенты методом электронного баланса:
KMnO4 + Н2О2 → MnO2 + KOH + Н2О + O2↑.
7. Предложите продукты реакций между пероксидом водорода и: а) гидроксидом железа(II), б) йодидом натрия. Составьте уравнения реакций и укажите переход электронов.
8. Предложите молекулярную и структурную формулы дисульфана — водородного соединения серы, являющегося аналогом пероксида водорода (по составу и строению). Составьте уравнение реакции его разложения на сероводород и серу.
9. Определите вещества X, Y, Z в схеме:
, если
.
Составьте уравнения соответствующих реакций.
10. Рассчитайте объём раствора пероксида водорода с массовой долей 3 % (плотность 1,01 г/см3), который можно приготовить, имея 1 дм3 пергидроля (плотность 1,112 г/см3, массовая доля Н2O2 30 %).
Самоконтроль
1. Схема образования водородной связи между молекулами воды и пероксида водорода:
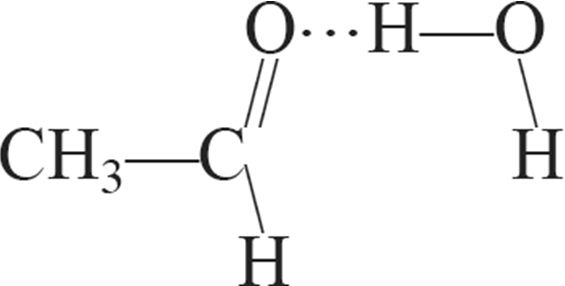
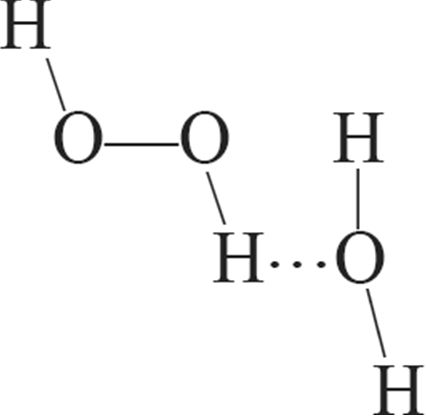
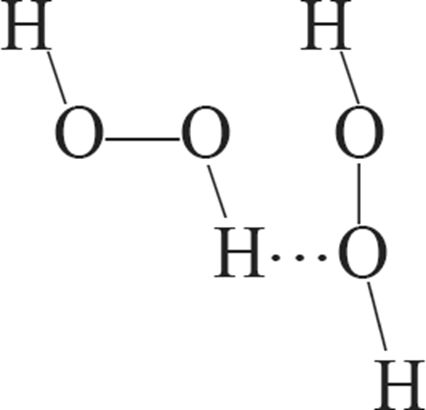
2. Сумма коэффициентов в уравнении реакции Н2О2 + PbS → H2O + PbSO4 равна:
- а) 6;
- б) 9;
- в) 10;
- г) 14.
3. Степень окисления –1 имеют атомы кислорода в соединениях:
- а) Na2О2;
- б) Н2О2;
- в) СаО2;
- г) K2О.
4. Пероксид водорода образуется в реакциях, схемы которых:
- а) ВаО2 + НCl →;
- б) ВаО2 + H2SO4 →;
- в) Н2О2 + KMnO4 →;
- г) Н2О2 + H2S →.
5. Относительно пероксида водорода верными являются утверждения:
- а) молекула Н2О2 линейна;
- б) в молекуле содержатся две полярные и одна неполярная ковалентная связь;
- в) проявляет окислительные свойства по отношению к NaI;
- г) можно использовать для получения кислорода в лаборатории.