§ 25. Электролитическая диссоциация веществ в растворах
*Отличие химических свойств ионов от свойств атомов и молекул
Атомы и молекулы являются электронейтральными частицами. Катионы металлов, например K+, как вам известно, образуются в результате того, что атомы металлов отдают электроны. Анионы неметаллов, например Br–, образуются в результате присоединения электронов к атомам неметаллов.
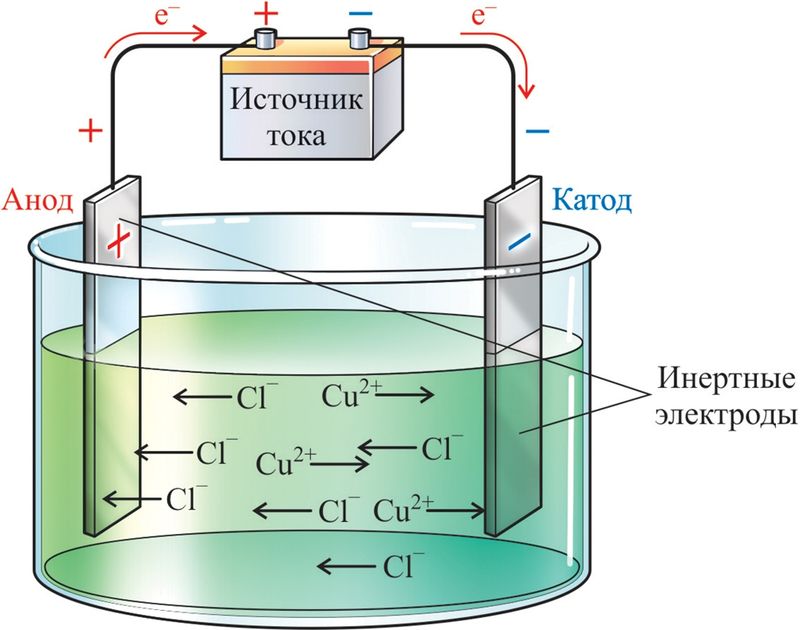
Свойства катионов и анионов отличаются от свойств соответствующих электронейтральных атомов. Так, в электрическом поле, которое создаётся электродами, происходит упорядоченное движение катионов и анионов электролита — электрический ток. Положительные ионы — катионы металлов, H+, и др. перемещаются к отрицательному электроду (катоду).
Отрицательные ионы — анионы кислотных остатков и OH– движутся к положительному электроду (аноду) (рис. 58.1).
В отличие от нейтральных атомов (в частности, атомов металлов) катионы, например Cu2+, Fe3+ и др., имеют меньшее число электронов на внешних электронных уровнях и меньший размер, всегда могут выступать в качестве окислителя и принимать электроны:
CuSO4 + Zn = ZnSO4 + Cu↓
или Cu2+ + Zn = Zn2+ + Cu↓.
В сравнении с нейтральными атомами (I, S, O) простые анионы, например, I–, S2– , O2– и др., имеют большее число электронов на внешних электронных уровнях и больший размер, могут выступать в качестве восстановителя и отдавать электроны:
2NaI + Cl2 = 2NaCl + I2
или 2I– + Cl2 = 2Cl– + I2.