§ 25. Электролитическая диссоциация веществ в растворах
Диссоциация соединений с ковалентным полярным типом связи
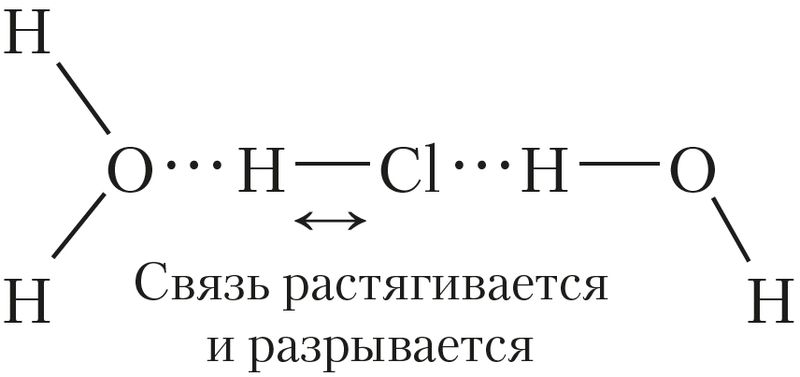
между молекулами H2O и HCl
Большинство органических и неорганических кислот растворимы в воде и являются электролитами. В кислотах атомы водорода связаны ковалентными полярными связями с атомами кислотных остатков. В полярных молекулах готовых ионов нет. Рассмотрим процесс диссоциации кислот на примере молекулы .
Вначале полярные молекулы кислоты притягиваются к полярным молекулам воды и ещё больше поляризуются.
Образуются водородные связи между молекулами кислоты и воды (рис. 58).
Затем ковалентная полярная связь удлиняется и становится менее прочной. В результате она разрывается, то есть происходит образование ионов:
Получившийся при диссоциации кислоты катион H+ присоединяется к молекуле воды с образованием катиона гидроксония H3O+ по донорно-акцепторному механизму, с которым вы познакомились, изучая материал § 13. Образовавшийся при ионизации ион хлора также оказывается гидратированным, что показано на рисунке 57.
Для упрощения уравнений реакций в ионной форме обычно записывают гидратированный катион водорода в виде Н+.
Аналогичным образом под действием полярных молекул воды происходит диссоциация и других соединений с ковалентным полярным типом связи.
Диссоциация включает процессы гидратации исходных молекул, их поляризации, разрушения связей в молекулах и их распада с образованием гидратированных ионов.
Молекулы кислот при диссоциации в водных растворах полностью или частично диссоциируют на катионы водорода и анионы кислотных остатков: