§ 14. Свойства химических связей
Свойства ионной и металлической связей
Длина и энергия ионных связей зависят от размера и заряда взаимодействующих ионов. Как правило, чем меньше размер и больше заряд ионов, тем прочнее связь. Значения её энергии находятся в пределах 300–700 кДж/моль.
В отличие от ковалентной связи ионная связь ненаправленная и ненасыщаемая, поскольку ион может притягивать к себе ионы противоположного знака в любом направлении. Расположение и число соседних ионов определяется их размерами, силами притяжения и отталкивания между ионами разных знаков. Поэтому ионы располагаются в определённом порядке, образуя кристаллическую решётку.
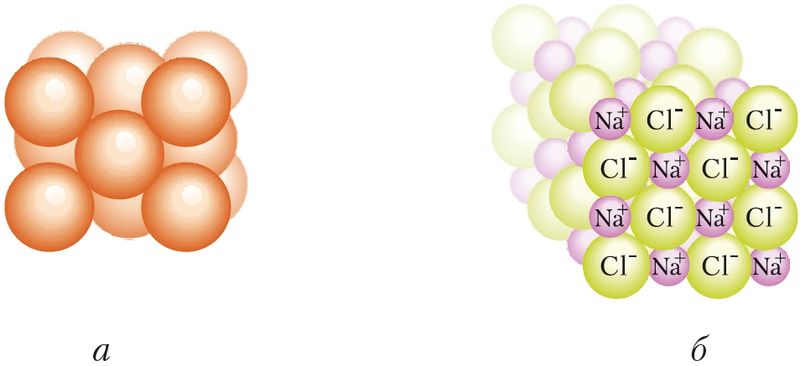
Металлическая связь также ненаправленная и ненасыщаемая. Её энергия изменяется в широких пределах: от десятков до нескольких сотен кДж/моль. В кристаллах металлов атомы имеют большое число ближайших соседей, что обеспечивает очень плотную упаковку атомов. Так, в кристаллах у атома меди 12 ближайших соседей, а у иона натрия в NaCl — шесть соседних ионов Cl–. Строение кристаллов можно представить в виде плотно упакованных шаров (рис. 34).