§ 13. Природа и типы химической связи
Ионная связь
Ионная связь — это химическая связь, которая образуется в результате электростатического притяжения противоположно заряженных ионов.
В случае ковалентной связи валентные электроны, участвующие в её образовании, локализованы между двумя связанными атомами. При образовании ионной связи электроны, напротив, считаются полностью перешедшими от одного атома к другому. В результате такого перехода электронов образуются ионы.
Образование ионов в кристаллах хлорида натрия представим, исходя из электронной конфигурации атомов натрия и хлора, следующим образом:
11Na 1s22s22p63s1 – e– → 11Na+ 1s22s22p6 (или Na – e– → Na+),
в сокращённом виде [Ne]3s1 – e– → [Ne];
17Cl 1s22s22p63s23p5 + e– → 17Cl– 1s22s22p63s23p6 (или Cl + e– → Cl–),
в сокращённом виде [Ne]3s23p5 + e– → [Ar].
Образующиеся ионы приобретают конфигурацию ближайшего благородного газа с октетом электронов на внешнем слое ns2nр6.
Переход электронов можно показать и с помощью электронных формул:
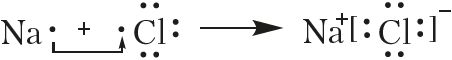
Из приведённых схем следует, что валентный электрон атома натрия полностью переходит на валентную оболочку атома хлора. Это приводит к возникновению ионов с противоположными зарядами.
Отметим, что для ионных соединений структурные формулы не составляют.
Возникает вопрос: почему в случае HCl образуется ковалентная, а в случае NaCl — ионная связь? Это объясняется различием в значениях электроотрицательности взаимодействующих атомов. Разность между значениями электроотрицательности атомов H и Cl значительно меньше, чем разность между значениями электроотрицательности Na и Cl. Это означает, что хлор гораздо сильнее притягивает к себе электрон натрия, чем электрон водорода. В результате происходит полный переход электрона от атома натрия к атому хлора.
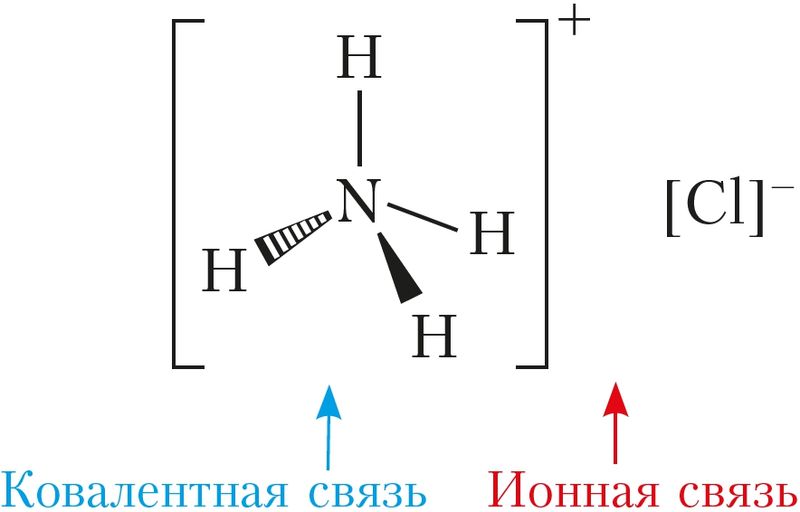
Ионная связь главным образом образуется в галогенидах, гидроксидах и оксидах щелочных и щёлочноземельных металлов. К этому типу также относят связь между катионом и анионом сложного состава, например в солях кислородсодержащих кислот (Na2SO4, NaNO3, (NH4)2SO4). В таких веществах существует два типа связей: ионная — между катионом и анионом, и ковалентная — между атомами неметаллов внутри катиона или иона сложного состава (рис. 25).