§ 13. Природа и типы химической связи
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 13. Природа и типы химической связи |
| Напечатано:: | Гость |
| Дата: | Monday, 13 October 2025, 20:01 |
Любое химическое соединение — молекулу (CO2), кристалл (NaCl), сложный ион () — с точки зрения электронного строения можно представить в виде системы, состоящей из атомных ядер и связывающих их электронов. Взаимодействие, которое делает эту систему устойчивой, называют химической связью.
Химическая связь — это взаимодействие, в результате которого отдельные атомы объединяются в более сложные системы (молекулы, кристаллы, ионы и др.).
Химическая связь обусловлена действием сил притяжения и отталкивания между положительно заряженными ядрами и отрицательно заряженными электронами, то есть имеет электростатическую природу.
Электроны, которые принимают участие в образовании химических связей, называют валентными. Это электроны внешних электронных оболочек атомов.
Рассмотрим, как и почему образуется химическая связь.
Основным условием образования химической связи является понижение полной энергии системы ядер и электронов по сравнению с энергией изолированных атомов.
Уменьшение полной энергии системы ядер и электронов достигается в результате совместного использования электронов разными атомами. В зависимости от того, как в результате распределена электронная плотность, различают три типа химической связи: ковалентную, ионную и металлическую.
Механизмы образования этих связей вы уже рассматривали при изучении химии в 8–10-х классах. Здесь мы дополним понятие химической связи представлениями о состоянии электронов в атоме.
Ковалентная связь
Ковалентная связь — это химическая связь, образованная общими (связывающими) электронными парами. Её называют локализованной, так как общая пара электронов размещается (локализуется) между двумя ядрами. Это заставляет положительно заряженные ядра притягиваться к паре электронов, расположенной между ядрами. Такая связь возникает между атомами с одинаковыми или близкими значениями электроотрицательности. Как правило, это атомы неметаллов.
Появление пары электронов, связывающей соседние атомы, можно представить двумя способами, то есть существует два механизма образования ковалентной связи — обменный и донорно-акцепторный.
Обменный механизм объясняет образование общей электронной пары из неспаренных валентных электронов, принадлежащих разным атомам. При этом электроны, образующие общую пару, должны иметь противоположные (антипараллельные) спины. Перекрывание двух электронных облаков приводит к увеличению электронной плотности между ядрами:
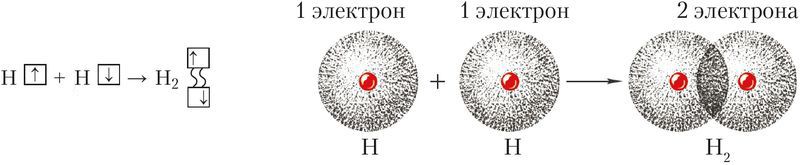
В образовании ковалентной связи могут участвовать s-, p- и d-электронные облака. Например, в связывании атомов хлора и водорода в молекуле H—Сl участвуют 1s-электрон атома водорода и неспаренный 3p-электрон атома хлора (рис. 24).
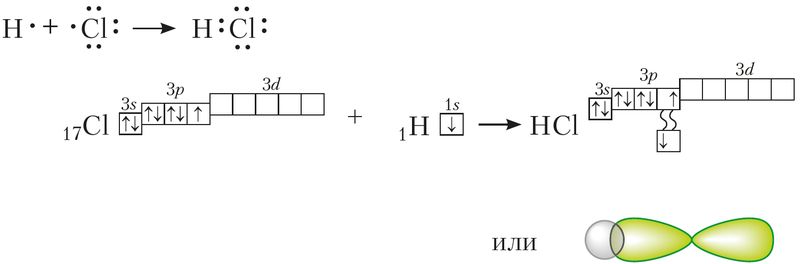
Каждый из связанных в общую электронную пару атомов приобретает электронную конфигурацию благородного газа: водород — гелия 1s2, а хлор — аргона 1s22s22р63s23р6. В результате оба атома достигают наиболее устойчивой электронной конфигурации.
Ещё один пример — образование связей в молекуле аммиака NH3. У атома азота согласно электронно-графической схеме есть три неспаренных электрона: 7N 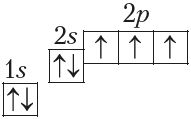 , у атома водорода — один
, у атома водорода — один . Эти электроны участвуют в образовании трёх ковалентных связей по обменному механизму с атомами водорода:
![]() или
или ![]()
Отметим, что одновременно с этим у азота на 2s-орбитали остаётся неподелённая электронная пара — пара электронов, не принимающая участия в образовании химических связей.
Обменным механизмом объясняют образование ковалентной связи в подавляющем большинстве молекул органических и неорганических веществ, в атомных кристаллах алмаза C, красного фосфора P, карборунда SiC, кварца SiO2 и др.
Донорно-акцепторный механизм образования ковалентной связи предполагает образование общей пары электронов за счёт передачи неподелённой электронной пары от одного атома (донора) на вакантную атомную орбиталь другого (акцептора). В качестве примера рассмотрим образование химической связи в катионе аммония при протекании реакции:
(хлорид аммония)
или в ионном виде:
(ион аммония).
Это взаимодействие можно представить электронными формулами:
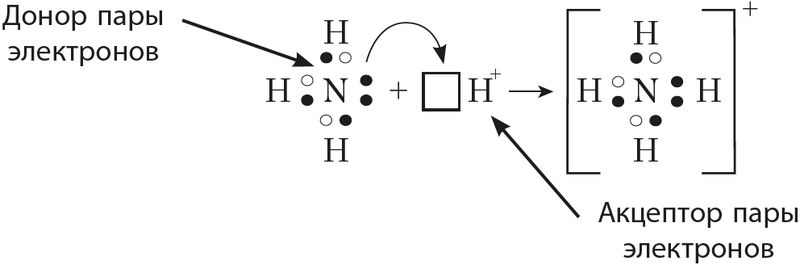
При взаимодействии молекулы 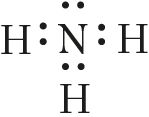 с катионом водорода
с катионом водорода , у которого на 1s-орбитали нет электронов, неподелённая пара электронов азота размещается на свободной 1s-орбитали
иона водорода. В результате образуется катион аммония
с четырьмя ковалентными связями:
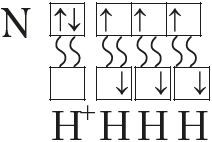
Так как молекула аммиака электронейтральна, а присоединённый к ней ион имеет заряд «+», то образовавшийся катион аммония также имеет положительный заряд. Этот заряд принадлежит целому иону, а не отдельному атому, поэтому в структурной формуле знак заряда иона ставят за квадратной скобкой: 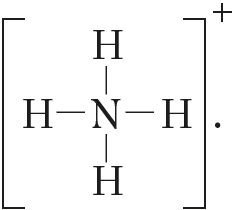 Если мы хотим подчеркнуть механизм образования связи, то можно стрелкой указать направление смещения электронной пары от донора к акцептору:
Если мы хотим подчеркнуть механизм образования связи, то можно стрелкой указать направление смещения электронной пары от донора к акцептору: 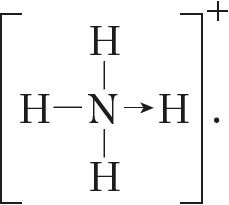 Но делать это необязательно, так как все связи в молекуле, независимо от механизма их образования, являются равноценными.
Но делать это необязательно, так как все связи в молекуле, независимо от механизма их образования, являются равноценными.
Аналогичным образом можно представить образование химической связи в катионе гидроксония H3O+: в результате гидратации иона водорода в водных растворах неподелённая электронная пара атома кислорода в молекуле воды размещается на свободной 1s-орбитали иона водорода.
Донорно-акцепторным механизмом объясняют образование ковалентной связи в молекулах угарного газа ![]() , азотной кислоты
, азотной кислоты 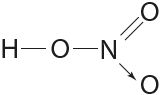 и др.
и др.
Ионная связь
Ионная связь — это химическая связь, которая образуется в результате электростатического притяжения противоположно заряженных ионов.
В случае ковалентной связи валентные электроны, участвующие в её образовании, локализованы между двумя связанными атомами. При образовании ионной связи электроны, напротив, считаются полностью перешедшими от одного атома к другому. В результате такого перехода электронов образуются ионы.
Образование ионов в кристаллах хлорида натрия представим, исходя из электронной конфигурации атомов натрия и хлора, следующим образом:
11Na 1s22s22p63s1 – e– → 11Na+ 1s22s22p6 (или Na – e– → Na+),
в сокращённом виде [Ne]3s1 – e– → [Ne];
17Cl 1s22s22p63s23p5 + e– → 17Cl– 1s22s22p63s23p6 (или Cl + e– → Cl–),
в сокращённом виде [Ne]3s23p5 + e– → [Ar].
Образующиеся ионы приобретают конфигурацию ближайшего благородного газа с октетом электронов на внешнем слое ns2nр6.
Переход электронов можно показать и с помощью электронных формул:
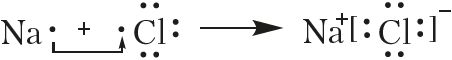
Из приведённых схем следует, что валентный электрон атома натрия полностью переходит на валентную оболочку атома хлора. Это приводит к возникновению ионов с противоположными зарядами.
Отметим, что для ионных соединений структурные формулы не составляют.
Возникает вопрос: почему в случае HCl образуется ковалентная, а в случае NaCl — ионная связь? Это объясняется различием в значениях электроотрицательности взаимодействующих атомов. Разность между значениями электроотрицательности атомов H и Cl значительно меньше, чем разность между значениями электроотрицательности Na и Cl. Это означает, что хлор гораздо сильнее притягивает к себе электрон натрия, чем электрон водорода. В результате происходит полный переход электрона от атома натрия к атому хлора.
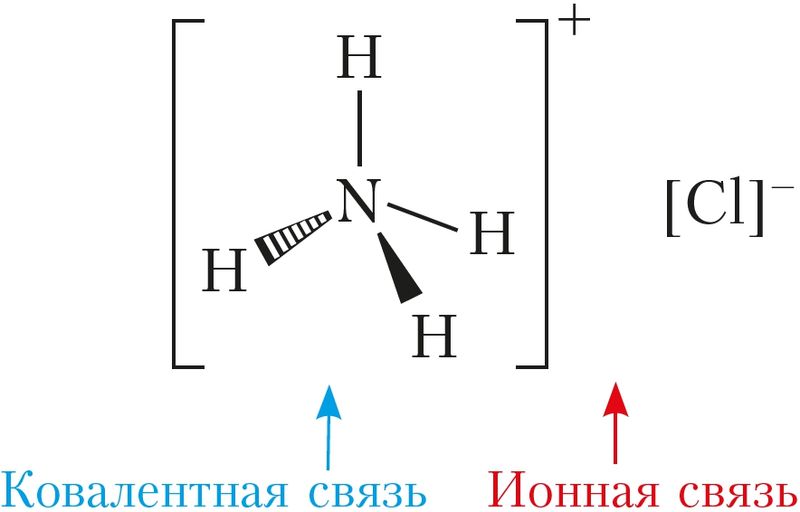
Ионная связь главным образом образуется в галогенидах, гидроксидах и оксидах щелочных и щёлочноземельных металлов. К этому типу также относят связь между катионом и анионом сложного состава, например в солях кислородсодержащих кислот (Na2SO4, NaNO3, (NH4)2SO4). В таких веществах существует два типа связей: ионная — между катионом и анионом, и ковалентная — между атомами неметаллов внутри катиона или иона сложного состава (рис. 25).
Металлическая связь
Металлическая связь образуется в кристаллах металлов и металлических сплавов за счёт обобществления всеми атомами их валентных электронов.

состоящий из регулярно
расположенных катионов металла
и свободно перемещающихся
электронов
Передача атомами металлов своих валентных электронов в коллективное пользование, наличие в металлах свободных электронов — причина электрической проводимости. Образование металлической связи можно описать следующим образом. В атомах металлов на внешнем энергетическом уровне содержится небольшое количество валентных электронов. В любом периоде периодической системы атомы металлов имеют по сравнению с атомами неметаллов больший радиус, меньшее количество валентных электронов и самый малый заряд ядра. Поэтому валентные электроны относительно слабо связаны с ядрами атомов и могут легко перемещаться по всему кристаллу металла. В результате кристалл состоит из положительно заряженных ионов, между которыми перемещаются свободные электроны, так называемый электронный газ (рис. 26).
В таблице 11 суммированы сведения о механизмах образования химических связей и распределении электронной плотности между химически связанными атомами.
Таблица 11. Образование ковалентной, ионной и металлической связей
| Тип связи | Характер обмена электронами между атомами | Условия взаимодействия между атомами |
| Ковалентная связь | Локализация связывающих электронных пар валентных электронов между положительно заряженными ядрами атомов. Возникает преимущественно между атомами неметаллов в молекулах и атомных кристаллах |
 электронных пар |
| Ионная связь | Передача электронов от одного атома другому и образование кристалла из катионов и анионов. Возникает между атомами типичных металлов и неметаллов, в солях, многих оксидах, гидроксидах |
 взаимодействие между образовавшимися ионами |
| Металлическая связь | Обобществление валентных электронов и их равномерное распределение в пространстве между всеми атомными ядрами. Возникает в металлах и сплавах |
 валентных электронов |
Химическая связь — это взаимодействие, в результате которого отдельные атомы объединяются в более устойчивые сложные системы (молекулы, кристаллы, ионы и др.).
Химическая связь имеет электростатическую природу.
При образовании химической связи полная энергия системы ядер и электронов понижается.
Выделяют три основных типа химической связи: ковалентная, ионная и металлическая, отличающиеся характером распределения электронной плотности между взаимодействующими атомами.
Существует два механизма образования ковалентной связи — обменный и донорно-акцепторный.
Вопросы, задания, задачи
1. Определите тип химической связи, представленный электронными схемами:
| а) | в) | ||
| б) | г) |
2. Составьте электронные формулы молекул водорода, хлора, хлороводорода, воды, аммиака и укажите число связывающих и неподелённых электронных пар в каждой из них.
3. Укажите тип химической связи между атомами в следующих соединениях:
- а) СaCl2, BaO, S8, CaF2, CCl4, сплав Fe—C;
- б) I2, SiO2, Na2S, О3, C2H5OH, сплав Au—Cu.
4. Сравните электронные схемы и электронные конфигурации:
- а) атома Li и иона Li+ в бромиде лития;
- б) атома Сl и иона Сl– в хлориде калия;
- в) атома S и атома серы в молекуле сероводорода.
5. Назовите механизм образования связи между атомами, имеющими следующие электронно-графические схемы внешних электронных оболочек:
- а)
и

- б)
 и
и 
- в)
и

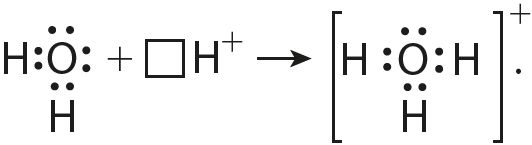
6. Согласно приведённой схеме объясните механизм образования ковалентной связи в ионе гидроксония при взаимодействии молекулы воды и иона водорода:
7. Используя значения электроотрицательности элементов (табл. 7), дайте обоснование типу химической связи в веществах и частицах: ,
,
,
,
,
.
| Химическая формула вещества или частицы | Электроотрицательность атомов | Разность электроотрицательностей ∆χ |
Тип химической связи | |
| χ1 | χ2 | |||
8. Укажите соединения, имеющие как ковалентную, так и ионную связь: НСООН, CH3COONa, MgF2, MgSO4, NH4NO3, HNO3, KNO3, CaSO4, NH3.
9. Рассчитайте число электронов, участвующих в образовании ковалентных связей в ионах аммония количеством 3 моль.
10. При образовании метана из атомов углерода и водорода выделяется 1662 кДж/моль энергии. Вычислите среднюю энергию связи С—Н (кДж/моль).
*Самоконтроль
1. Верными являются утверждения:
- а) химическая связь имеет электростатическую природу;
- б) энергия двух отдельных атомов Сl меньше энергии двух связанных атомов Cl;
- в) атом углерода имеет четыре валентных электрона;
- г) разрыв химической связи сопровождается поглощением энергии.
2. За счёт общих электронных пар образуются связи:
- а) ковалентная полярная;
- б) ионная;
- в) металлическая;
- г) ковалентная неполярная.
3. Ионная связь существует в веществах:
- а) О2;
- б) СsCl;
- в) Mg(NO3)2;
- г) Н2О.
4. Азот выступил донором электронной пары в соединениях:
- а) NН3;
- б) NH4NO3;
- в) NCl3;
- г) (NH4)2SO4.
5. Электронную конфигурацию, сходную с конфигурацией атома аргона, имеют ионы:
- а) Ca2+;
- б) F–;
- в) Na+;
- г) S2–.