§ 3. Арганічныя рэчывы. Амінакіслоты. Алігапептыды
Амінакіслоты — манамеры бялковых малекул. Амінакіслоты — арганічныя злучэнні, якія змяшчаюць адначасова амінагрупу (—NН2), што валодае асноўнымі ўласцівасцямі, і карбаксільную групу (—СООН), што праяўляе кіслотныя ўласцівасці. У саставе жывых арганізмаў выяўлены сотні амінакіслот, але ва ўтварэнні бялкоў удзельнічае толькі 20 з іх. Такія амінакіслоты называюць бялокутваральнымі, іх поўныя і скарочаныя назвы паказаны ў табліцы 3 (не для запамінання).
Табліца 3. Бялокутваральныя амінакіслоты
|
Амінакіслата |
Скарочаная назва |
Амінакіслата |
Скарочаная назва |
|
Аланін |
Ала |
Лейцын |
Лей |
|
Аргінін |
Арг |
Лізін |
Ліз |
|
Аспарагін |
Асн |
Метыянін |
Мет |
|
Аспарагінавая кіслата |
Асп |
Пралін |
Пра |
|
Валін |
Вал |
Серын |
Сер |
|
Гістыдзін |
Гіс |
Тыразін |
Тыр |
|
Гліцын |
Глі |
Трэанін |
Трэ |
|
Глутамін |
Глн |
Трыптафан |
Трп |
|
Глутамінавая кіслата |
Глу |
Фенілаланін |
Фен |
|
Ізалейцын |
Іле |
Цыстэін |
Цыс |
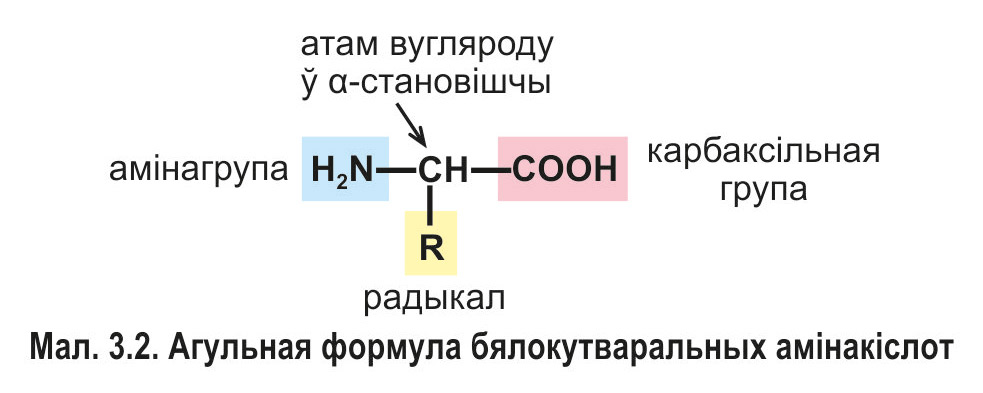
У малекулах бялокутваральных амінакіслот амінагрупа і карбаксільная група далучаны да аднаго і таго ж атама вугляроду (г. зн. усе яны з’яўляюцца a-амінакіслотамі). З гэтым жа атамам вугляроду злучаны радыкал (R), які ў кожнай амінакіслаты мае асаблівую будову і вызначае яе спецыфічныя ўласцівасці (мал. 3.2).
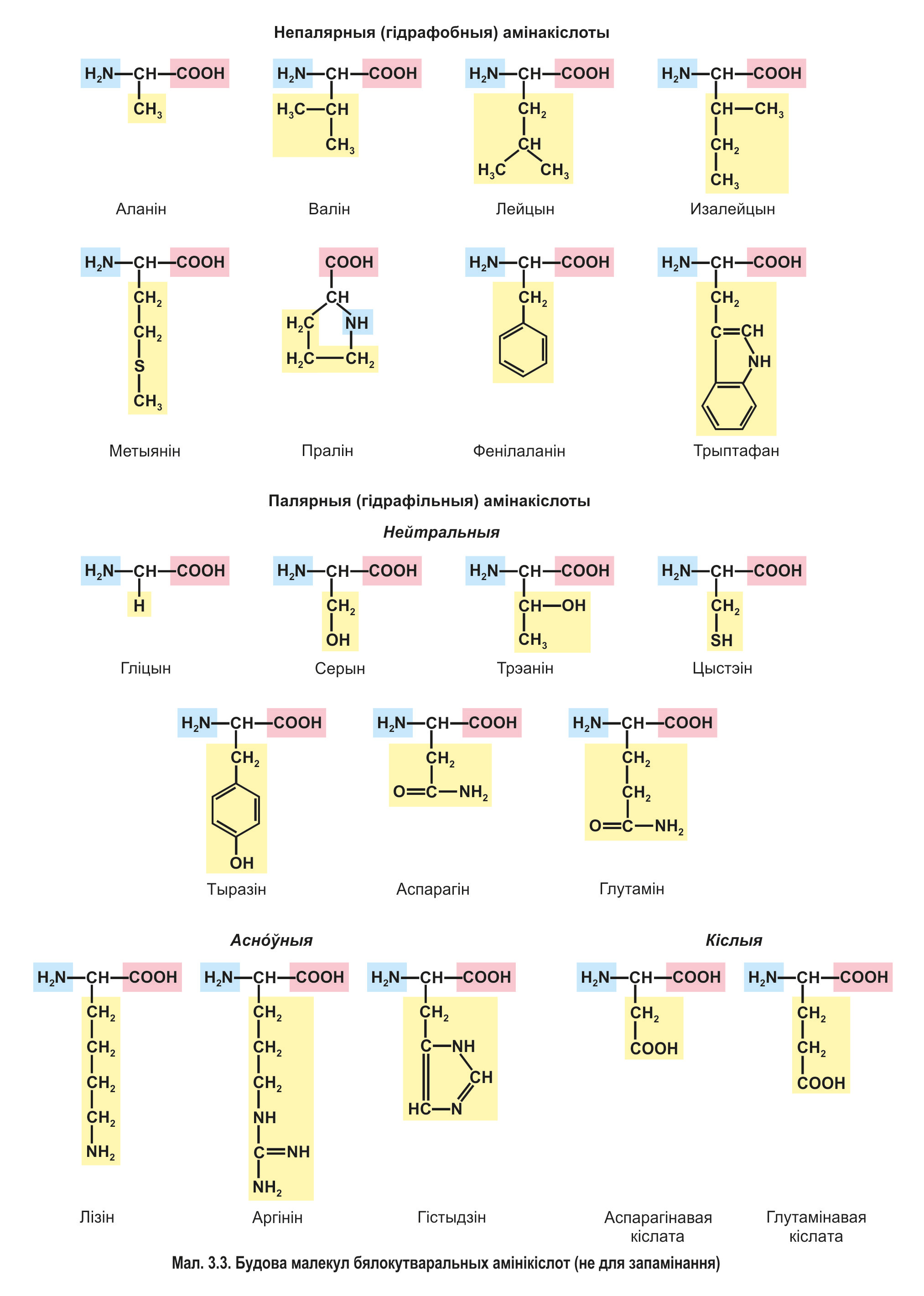
Радыкалы амінакіслот могуць быць непалярнымі (гідрафобнымі) ці палярнымі (гідрафільнымі), змяшчаць розныя функцыянальныя групы. Напрыклад, радыкал серыну змяшчае гідраксільную групу (—ОН), радыкал цыстэіну — серазмяшчальную групу (—SH). Некаторыя амінакіслоты маюць цыклічныя радыкалы (мал. 3.3). Усё гэта адыгрывае важную ролю ў фарміраванні прасторавай структуры бялкоў.
Малекулы большасці бялокутваральных амінакіслот змяшчаюць адну амінагрупу і адну карбаксільную групу — гэта нейтральныя амінакіслоты. Некаторыя амінакіслоты маюць дадатковыя аміна- ці карбаксільныя групы ў саставе радыкала. Такія амінакіслоты адпаведна называюцца асноўнымі або кіслымі (гл. мал. 3.2).
Аўтатрофныя арганізмы сінтэзуюць усе неабходныя ім амінакіслоты з прадуктаў фотасінтэзу і азотазмяшчальных неарганічных злучэнняў. Для гетэратрофных арганізмаў крыніцай амінакіслот з’яўляецца ежа. У арганізме чалавека і жывёл некаторыя амінакіслоты могуць сінтэзавацца з прадуктаў абмену рэчываў (у першую чаргу — з іншых амінакіслот). Такія амінакіслоты называюцца замяняльнымі. Іншыя ж, так званыя незамяняльныя амінакіслоты, не могуць быць сінтэзаваны ў арганізме і таму павінны пастаянна паступаць у яго ў саставе бялкоў ежы.
*Паўнацэнныя харчовыя бялкі змяшчаюць астаткі ўсіх незамяняльных амінакіслот. Бялкі ежы, у саставе якіх адсутнічаюць астаткі якіх-небудзь незамяняльных амінакіслот, называюць непаўнацэннымі.*
Для чалавека незамяняльнымі амінакіслотамі з’яўляюцца: трыптафан, валін, лізін, ізалейцын, трэанін, фенілаланін, метыянін і лейцын. Запамінаць іх пералік неабавязкова, але пры жаданні можаце выкарыстаць мнеманічныя правілы. Напрыклад: «ТРы Падлеткі — ВАЛя, ЛІЗа І ЛЕнка ТРЭніраваліся з ФЕНам і МЕТалічнай ЛЕЙкай».
*Часткова замяняльныя амінакіслоты — аргінін і гістыдзін — сінтэзуюцца ў чалавека ў невялікай колькасці, недастатковай для нармальнага функцыянавання арганізма, асабліва ў дзіцячым узросце. Таму яны павінны дадаткова паступаць у складзе харчовых бялкоў.*
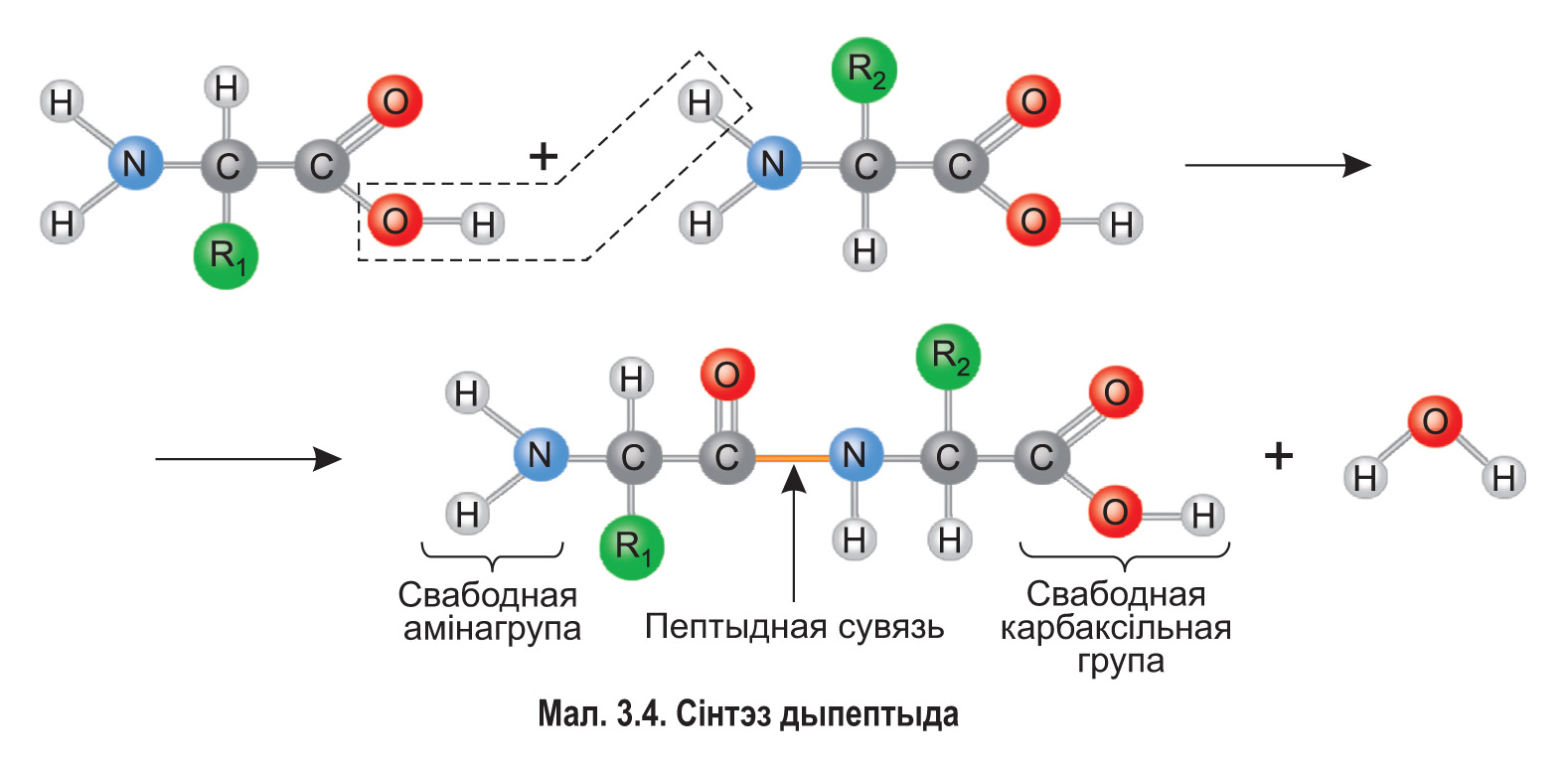
Наяўнасць адначасова амінагрупы і карбаксільнай групы абумоўлівае амфатэрнасць амінакіслот і іх высокую рэакцыйную здольнасць. Як вы памятаеце з курса хіміі, карбаксільная група (—СООН) адной амінакіслаты можа ўзаемадзейнічаць з амінагрупай (—NH2) другой амінакіслаты. Пры гэтым ад карбаксільнай групы адшчапляецца група —ОН, а ад амінагрупы — атам вадароду. У выніку вылучаецца малекула вады, а паміж атамам вугляроду карбаксільнай групы і атамам азоту амінагрупы ўзнікае кавалентная сувязь, якая называецца пептыднай сувяззю (мал. 3.4).
Так утвараецца дыпептыд, які мае на адным канцы свабодную амінагрупу, а на другім — свабодную карбаксільную групу. Дзякуючы любой з іх дыпептыд можа ўзаемадзейнічаць з наступнай амінакіслатой, утвараючы трыпептыд і г. д. Калі такім чынам злучаецца больш за 10 астаткаў амінакіслот, то ўтвараецца поліпептыд.
*Структуру аліга- і поліпептыдаў прынята запісваць злева направа ў напрамку ад канца, які змяшчае свабодную амінагрупу (так званы N-канец), да канца, які мае свабодную карбаксільную групу (С-канец). Напрыклад, дыпептыды Глу—Ала і Ала—Глу маюць розную структуру: у першага астатак глутамінавай кіслаты мае свабодную групу –NH2, а астатак аланіну — групу –СООН, а ў другога — наадварот.*