§ 9. Выпарэнне і кандэнсацыя. Насычаная пара
Чаму ў шчыльна закрытай пасудзіне гарачая вада астывае павольней, чым у адкрытай? Чаму зімой на дрэвах часам з’яўляецца іней? Чым ідэальны газ адрозніваецца ад пары?
Выпарэнне і кандэнсацыя. З паўсядзённага досведу мы ведаем, што вадкасці, напрыклад вада, знаходзячыся ў адкрытых пасудзінах, з цягам часу пераходзяць у газападобны стан — выпарваюцца. Прычым хуткасць выпарэння залежыць ад роду вадкасці, яе тэмпературы, плошчы свабоднай паверхні і ад прытоку паветра. У выніку выпарэння вады з паверхні вадзяной абалонкі Зямлі (гідрасферы), з паверхні глебы і расліннага покрыва ў паветры заўсёды знаходзіцца вадзяная пара, якая можа кандэнсавацца, утвараць воблакі, вяртацца на зямлю ў выглядзе ападкаў. Працэсы выпарэння і кандэнсацыі распаўсюджаны ў прыродзе і тэхніцы, і вывучэнне іх асаблівасцей мае вялікае практычнае значэнне.
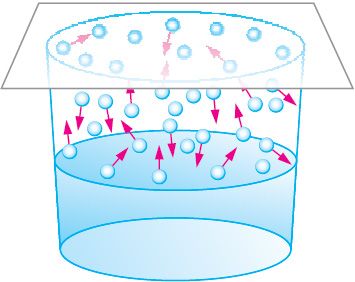
Разгледзім шчыльна закрытую пасудзіну, у якой вада займае ніжнюю частку, а астатняя прастора запоўнена парай. Малекулы ў вадзе і пары знаходзяцца ў бесперапынным руху і могуць як пераходзіць з вады ў пару, так і вяртацца з пары ў ваду. Такім чынам, у пасудзіне адначасова адбываюцца два процілегла накіраваныя працэсы — пераход вады ў газападобны стан (выпарэнне) і пераход вадзяной пары ў вадкасць (кандэнсацыя) (мал. 58).
Пасля герметызацыі пасудзіны на працягу некаторага прамежку часу выпарэнне вадкасці пераважае над кандэнсацыяй яе пары. Калі пры гэтым з навакольнага асяроддзя да сістэмы «вадкасць — пара» не паступае энергія, то вадкасць ахалоджваецца. Гэта адбываецца ў выніку таго, што паверхневы слой вадкасці пакідаюць малекулы, якія валодаюць найбольшай скорасцю. Такія малекулы маюць і найбольшую кінетычную энергію цеплавога руху, што дазваляе ім пераадолець сілы прыцяжэння, якія дзейнічаюць у паверхневым слоі вадкасці. Работа сіл прыцяжэння ўплывае такім чынам, што скорасць кожнай малекулы, якая вылятае з вадкасці, памяншаецца, а скорасць кожнай малекулы, якая ўлятае ў яе, наадварот, павялічваецца. Такое змяненне скорасці, а значыць, і кінетычнай энергіі малекул, якія перасякаюць паверхню вадкасці, дазваляе сістэме «вадкасць — пара» дасягнуць стану цеплавой раўнавагі, пры якой тэмпературы вадкасці і яе пары аднолькавыя.
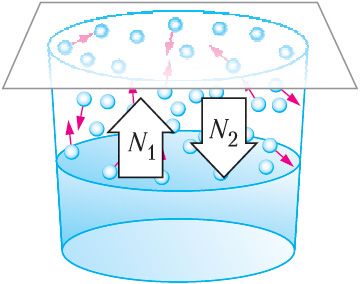
Пры выпарэнні вадкасці ў добра закрытай посудзіне шчыльнасць пары над ёй павялічваецца, і адначасова расце колькасць малекул, што ўлятаюць назад у вадкасць. Канцэнтрацыя малекул пары ўзрастае да таго часу, пакуль колькасць N1 малекул, якія пакідаюць вадкасць (мал. 59), не стане роўнай колькасці N2 малекул, якія вяртаюцца ў яе за той самы прамежак часу: N1 = N2. Узровень вадкасці ў пасудзіне пры гэтым не змяняецца з цягам часу. Паміж вадкасцю і яе парай устанаўліваецца стан дынамічнай раўнавагі. Ён будзе існаваць да таго часу, пакуль не зменіцца тэмпература ці аб’ём сістэмы.
1. Звычайна пры выпарэнні вадкасць ахалоджваецца. У якім выпадку магчыма выпарэнне вадкасці пры пастаяннай тэмпературы?
2. Калі пасудзіну з вадой шчыльна закрыць, то спачатку колькасць вады паменшыцца, а затым будзе заставацца пастаяннай. Чаму?