§ 9. Испарение и конденсация. Насыщенный пар
Почему в плотно закрытом сосуде горячая вода остывает медленнее, чем в открытом? Почему зимой на деревьях иногда появляется иней? Чем идеальный газ отличается от пара?
Испарение и конденсация. Из повседневного опыта мы знаем, что жидкости, например вода, находясь в открытых сосудах, с течением времени переходят в газообразное состояние — испаряются. Причём скорость испарения зависит от рода жидкости, её температуры, площади свободной поверхности и от притока воздуха. Вследствие испарения воды с поверхности водяной оболочки Земли (гидросферы), с поверхности почвы и растительного покрова в воздухе всегда находятся водяные пары, которые могут конденсироваться, образовывать облака, выпадать в виде осадков. Процессы испарения и конденсации распространены в природе и технике, и изучение их особенностей имеет большое практическое значение.
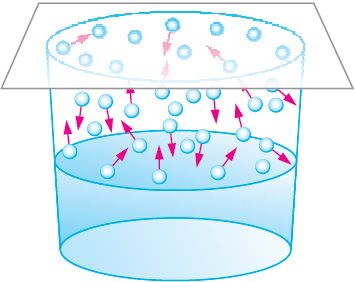
Рассмотрим плотно закрытый сосуд, в котором вода занимает нижнюю часть, а остальное пространство заполнено паром. Молекулы в воде и паре находятся в непрерывном движении и могут как вылетать из воды в пар, так и из пара возвращаться в воду. Таким образом, в сосуде одновременно протекают два противоположно направленных процесса — переход воды в газообразное состояние (испарение) и переход водяного пара в жидкость (конденсация) (рис. 58).
После герметизации сосуда в течение некоторого промежутка времени испарение жидкости преобладает над конденсацией её пара. Если при этом из окружающей среды к системе «жидкость — пар» не поступает энергия, то жидкость охлаждается. Это происходит вследствие того, что поверхностный слой жидкости покидают молекулы, обладающие наибольшей скоростью. Такие молекулы имеют и наибольшую кинетическую энергию теплового движения, что позволяет им преодолеть силы притяжения, действующие в поверхностном слое жидкости. Работа сил притяжения обеспечивает то, что скорость каждой вылетающей из жидкости молекулы уменьшается, а скорость каждой влетающей в неё молекулы, наоборот, увеличивается. Такие изменения скорости, а значит, и кинетической энергии молекул, пересекающих поверхность жидкости, позволяют системе «жидкость — пар» достичь состояния теплового равновесия, при котором температуры жидкости и её пара одинаковы.
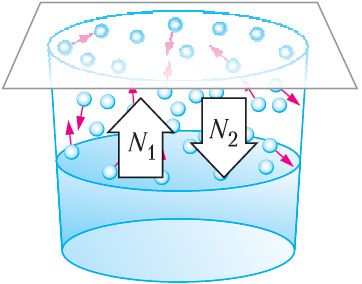
При испарении жидкости в плотно закрытом сосуде плотность пара над ней увеличивается, и одновременно растёт число молекул, влетающих обратно в жидкость. Концентрация молекул пара возрастает до тех пор, пока число N1 молекул, покидающих жидкость (рис. 59), не станет равным числу N2 молекул, возвращающихся в неё за тот же промежуток времени: N1 = N2. Уровень жидкости в сосуде при этом не изменяется с течением времени. Между жидкостью и её паром устанавливается состояние динамического равновесия. Оно будет существовать до тех пор, пока не изменится температура или объём системы.
1. Обычно при испарении жидкость охлаждается. Когда возможно испарение жидкости при постоянной температуре?
2. Если сосуд с водой плотно закрыть, то сначала количество воды уменьшится, а затем будет оставаться постоянным. Почему?