§ 39. Жиры
Химические свойства
1. Гидрирование
Жидкие жиры можно превратить в твёрдые, осуществив реакцию присоединения водорода по двойным связям C ![]() C остатков ненасыщенных кислот. Этот процесс, который называется гидрированием жиров, широко используется в промышленности для получения твёрдых жиров — исходных веществ для синтеза моющих средств и маргарина.
C остатков ненасыщенных кислот. Этот процесс, который называется гидрированием жиров, широко используется в промышленности для получения твёрдых жиров — исходных веществ для синтеза моющих средств и маргарина.
В качестве примера приведём уравнение реакции гидрирования триглицерида олеиновой кислоты до триглицерида стеариновой кислоты:
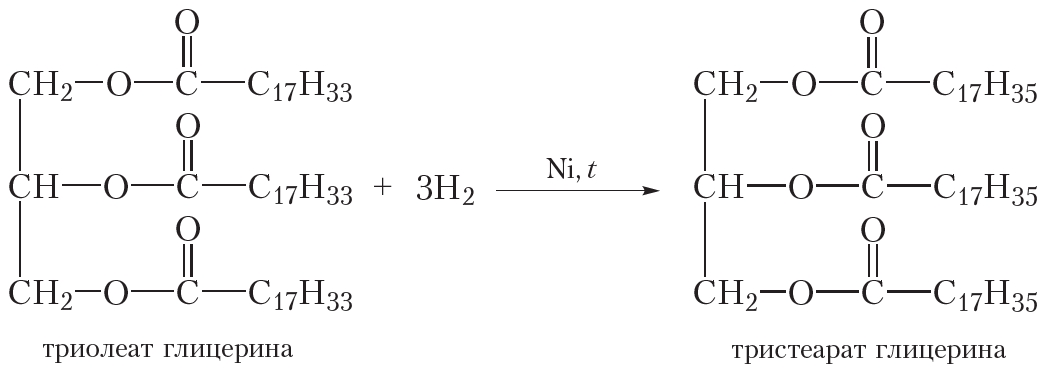
2. Гидролиз
Так как триглицериды являются сложными эфирами, они подвергаются кислотному и щелочному гидролизу.
Кислотный гидролиз
При нагревании в присутствии кислот жиры гидролизуются до глицерина и соответствующих карбоновых кислот. Приведём уравнение реакции кислотного гидролиза на примере триглицерида пальмитиновой кислоты: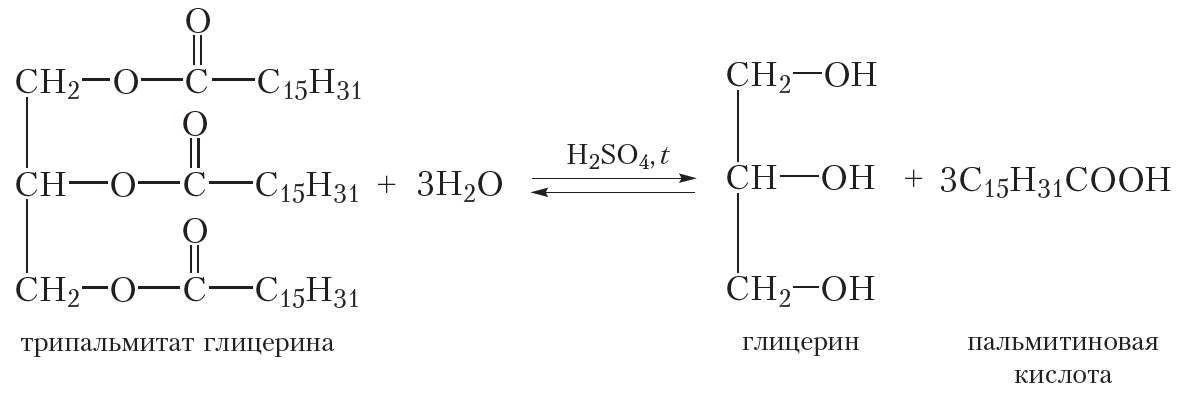
Так как жир является смесью триглицеридов, то при гидролизе жира образуется смесь карбоновых кислот и глицерин.
Щелочной гидролиз
Процесс щелочного гидролиза имеет особое значение, потому что в результате наряду с глицерином образуются соли карбоновых кислот. Например, при гидролизе триглицерида стеариновой кислоты раствором гидроксида натрия образуется натриевая соль стеариновой кислоты — стеарат натрия:
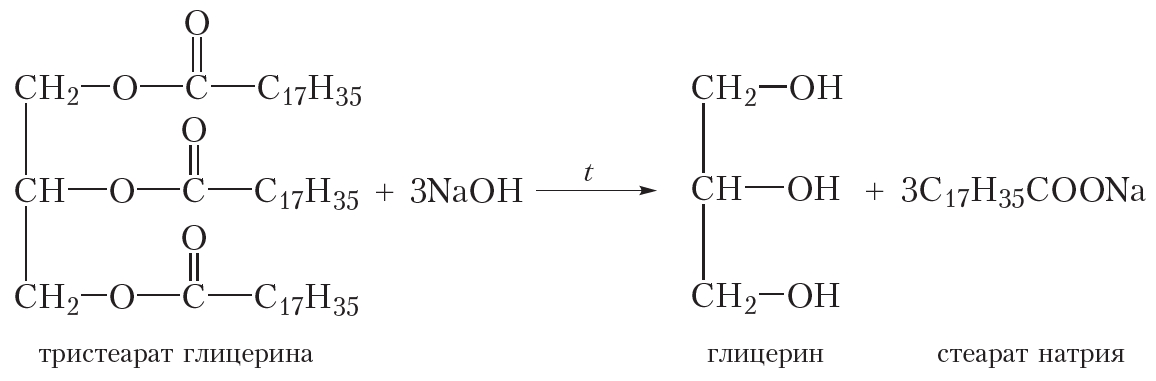
Натриевые и калиевые соли высших жирных кислот являются основой мыла. В связи с этим реакцию щелочного гидролиза иногда называют омылением.
Из реакционной смеси, образовавшейся в результате щелочного гидролиза жира, соли высших карбоновых кислот извлекают путём добавления хлорида натрия при перемешивании. По мере насыщения раствора хлоридом натрия растворимость солей высших карбоновых кислот уменьшается, раствор начинает мутнеть и, наконец, соли высших жирных кислот всплывают над прозрачной жидкостью в виде творожистых хлопьев, которые отделяют, промывают водой, добавляют красители, отдушки и прессуют в обычные куски мыла.