§ 8. Гомологический ряд и физические свойства алканов
Гомологический ряд и физические свойства алканов
Из материала предыдущих параграфов вы познакомились с органическими соединениями, относящимися к классу алканов. Алканы называют также предельными углеводородами. Название предельные углеводороды обусловлено тем, что молекулы алканов содержат предельно возможное число атомов водорода.
Атомы углерода в молекулах алканов соединены только одинарными связями. Такие вещества называют насыщенными. В отличие от насыщенных углеводородов, в молекулах ненасыщенных соединений имеются атомы углерода, связанные двойными или тройными связями. Примеры ненасыщенных углеводородов:
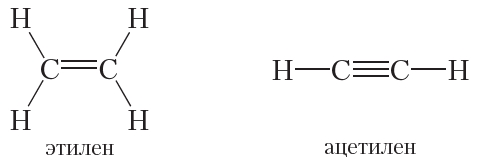
Ненасыщенные углеводороды будем изучать позднее, пока сосредоточим внимание на насыщенных углеводородах — алканах.
Мы пока познакомились лишь с несколькими представителями алканов, однако очевидно, что соединений этого класса может быть огромное число как за счёт возможности образования углеродных цепей различной длины, так и за счёт изомерии. Состав всех алканов описывается общей формулой CnH2n+2.
Легко видеть, что состав молекулы этана отличается от состава молекулы метана на один атом углерода и два атома водорода — СН2. Такую же разницу в составе имеют молекулы пропана и этана, н-бутана и пропана:
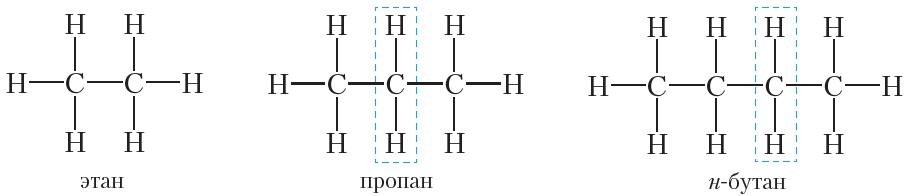
В то же время состав н-бутана и этана различается на две группы СН2. Таким образом, молекулы алканов по составу отличаются друг от друга на одну или несколько групп CH2. При этом молекулы алканов имеют сходное строение: связи между атомами углерода одинарные, остальные cвязи углерод образует с водородом. Поэтому разные алканы имеют похожие химические свойства.
| Вещества, сходные по строению и химическим свойствам и отличающиеся по составу молекул на одну или несколько групп СН2, называются гомологами и образуют гомологический ряд. |
Например, метан, этан и пропан являются гомологами.
Понятие «гомологический ряд» является важным в органической химии. По причине огромного множества органических соединений, изучение химических свойств каждого органического вещества не представляется возможным, поэтому сходные по строению вещества объединяют в гомологические ряды и изучают общие свойства представителей данного гомологического ряда. Мы не будем рассматривать отдельно химические свойства метана, затем свойства этана и т. д. Вместо этого изучим свойства, присущие всем алканам.
Рассмотрим физические свойства алканов. В таблице 8.1 приведены температуры кипения неразветвлённых алканов, молекулы которых содержат от одного до десяти атомов углерода.
Таблица 8.1. Температуры кипения неразветвлённых алканов
|
Молекулярная формула |
Структурная формула |
Температура кипения (tкип, °С) |
|
СН4 |
СН4 |
–162 |
|
С2Н6 |
|
–89 |
|
С3Н8 |
–42 | |
|
С4Н10 |
–0,5 | |
|
С5Н12 |
36 | |
|
С6Н14 |
69 | |
|
С7Н16 |
98 | |
|
С8Н18 |
126 | |
|
С9Н20 |
151 | |
|
С10Н22 |
174 |
Из данных таблицы видно, что температуры кипения метана, этана, пропана и бутана ниже 0 °С, следовательно, эти вещества при нормальных условиях должны быть газообразными. Действительно, метан, этан, пропан и н-бутан при комнатной температуре являются бесцветными газами. Алканы с бо́льшим числом атомов углерода в молекуле (от 5 до 15) представляют собой жидкости со специфическим запахом. Эти алканы входят в состав бензина, керосина, многих растворителей. Алканы с ещё бо́льшим числом атомов углерода в молекуле (от 16 и более) представляют собой твёрдые вещества. Они хорошо знакомы вам — из твёрдых алканов изготавливают парафиновые свечи. Название парафины (от лат. parum — мало и affinis — имеющий сродство) — ещё одно название алканов. Это название указывает на низкую химическую активность алканов, химические свойства которых будут рассмотрены в дальнейшем.
Алканы нерастворимы в воде, но хорошо растворяются в органических растворителях. Вспомните правило, известное вам из курса неорганической химии, «подобное растворяется в подобном». Это значит, что обычно хорошо смешиваются между собой вещества, имеющие сходное строение. Например, вода, молекулы которой являются полярными, хорошо растворяет вещества с ионными и ковалентными полярными связями — кислоты, щёлочи, соли. Напротив, вещества, молекулы которых образованы ковалентными неполярными либо малополярными связями, не растворяются в воде, зато растворяются в жидкостях, состоящих из неполярных молекул. Приведём пример: пятно от машинного масла на ткани практически невозможно удалить с помощью воды, но оно может быть с успехом удалено бензином, поскольку машинное масло и бензин состоят из веществ сходного строения, углеводородов.
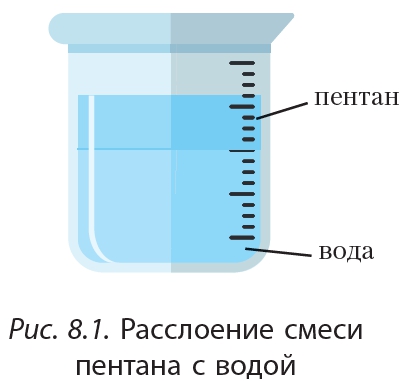 Жидкие и твёрдые алканы имеют плотность менее 1 г/см3, то есть меньше плотности воды. Если поместить в химический стакан воду, а затем добавить пентан, то полученная смесь разделится на два слоя, причём пентан соберётся в верхней части, а снизу будет вода (рис. 8.1).
Жидкие и твёрдые алканы имеют плотность менее 1 г/см3, то есть меньше плотности воды. Если поместить в химический стакан воду, а затем добавить пентан, то полученная смесь разделится на два слоя, причём пентан соберётся в верхней части, а снизу будет вода (рис. 8.1).
Такой же эффект наблюдается при попадании нефти в воду. При этом на поверхности воды образуется плёнка из нефти, что наносит огромный ущерб живым организмам. Поэтому аварии, связанные с разливом нефти, особенно опасны для окружающей среды.
|
Углеводороды, в молекулах которых атомы углерода соединены только одинарными связями, называются насыщенными. Алканы являются насыщенными углеводородами. Алканы называют также предельными углеводородами, поскольку молекулы алканов содержат предельно возможное число атомов водорода. Молекулы алканов имеют сходное строение и по составу отличаются друг от друга на одну или несколько групп CH2. Вещества, сходные по строению и химическим свойствам, отличающиеся по составу молекул на одну или несколько групп СН2, называются гомологами и образуют гомологический ряд. В гомологическом ряду алканов по мере увеличения числа атомов углерода в молекуле растут температуры кипения. Алканы не растворяются в воде, но растворяются в органических растворителях. |