§ 14. Першы закон тэрмадынамікі. Прымяненне першага закона тэрмадынамікі да ізапрацэсаў змянення стану ідэальнага газу
![]()
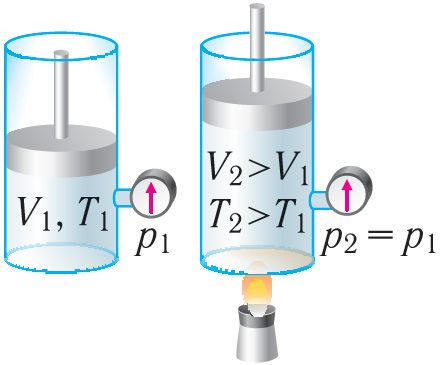
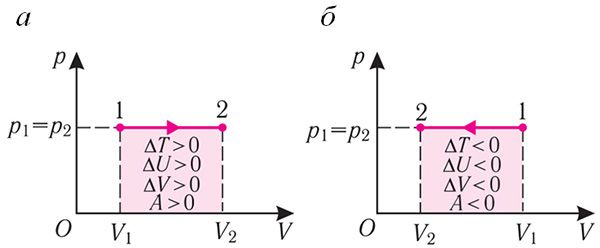
Ізабарны працэс. Няхай газ знаходзіцца ў цыліндрычнай пасудзіне, закрытай поршнем, які можа свабодна або пад пастаяннай нагрузкай перамяшчацца (мал. 80). Нагрэем газ, перадаўшы яму некаторую колькасць цеплаты (Q > 0). Паводле першага закона тэрмадынамікі перададзеная газу колькасць цеплаты часткова расходуецца на павелічэнне ўнутранай энергіі (ΔU > 0) сістэмы і часткова ідзе на выкананне работы сілай ціску газу пры яго расшырэнні (А > 0, мал. 80.1, а): Q = ΔU + A.
Пры ізабарным працэсе работа расшырэння (сціскання) газу A = pΔV ≠ 0, і першы закон тэрмадынамікі прымае выгляд
Q = ΔU+ pΔV.
Пры ізабарным сцісканні газу знешнія сілы выконваюць работу A' > 0. Каб ціск газу пры гэтым заставаўся пастаянным, газ неабходна ахалоджваць, гэта значыць ён павінен аддаваць у навакольнае асяроддзе некаторую колькасць цеплаты (Q < 0). Паніжэнне тэмпературы газу пры ізабарным сцісканні прыводзіць да памяншэння яго ўнутранай энергіі (ΔU < 0). Работа сілы ціску газу пры сцісканні А < 0 (мал. 80.1, б).
Сіла ціску ідэальнага газу падчас ізабарнага расшырэння выканала работу А = 320 Дж. Пры гэтым газ атрымаў колькасць цеплаты Q = 680 Дж. Вызначце прырашчэнне ўнутранай энергіі ідэальнага газу.
![]()
Удзельная цеплаёмістасць рэчыва залежыць не толькі ад яго ўласцівасцей, але і ад характару ажыццяўлення працэсу цеплаабмену. Сапраўды, з формулы Q = cmΔT вынікае, што ўдзельная цеплаёмістасць .
Тады згодна з першым законам тэрмадынамікі пры ізахорным працэсе ўдзельная цеплаёмістасць ідэальнага газу , а пры ізабарным —
. Такім чынам, для аднолькавага павелічэння тэмпературы пры ізабарным награванні адзінцы масы газу неабходна перадаць большую колькасць цеплаты, чым пры ізахорным награванні, гэта значыць cp > cV. Гэта тлумачыцца тым, што пры пастаянным ціску частка перададзенай энергіі расходуецца на выкананне сілай ціску газу работы пры расшырэнні.
Расшырэнне вадкіх і цвёрдых цел пры награванні пры пастаянным ціску значна меншае, чым газаў, таму для іх АΔU і іх удзельныя цеплаёмістасці мала залежаць ад характару працэсу (ср ≈ сV).