§ 6. Ізатэрмічны, ізабарны і ізахорны працэсы
Ізабарны працэс. Працэс змянення стану газу пры пастаянным ціску (p = const) называюць ізабарным.
У 1802 г. французскі вучоны Жозэф Гей-Люсак (1778–1850) разгледзеў гэты працэс для паветра, вадароду, кіслароду і азоту.
Калі пры пераходзе з пачатковага стану ў канчатковы маса і малярная маса газу не змяняюцца, то аб’ём газу, як вынікае з ураўнення Клапейрона — Мендзялеева:
, або
, гэта значыць
.
(6.2)
Аб’ём дадзенай масы газу пры пастаянных малярнай масе і ціску прама прапарцыянальны абсалютнай тэмпературы.
Гэтае сцвярджэнне называюць законам Гей-Люсака.
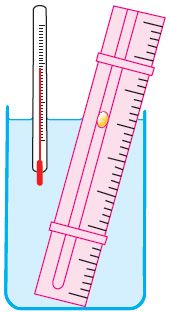
Праўдзівасць закона Гей-Люсака можна праверыць эксперыментальна, выкарыстоўваючы прыладу, паказаную на малюнку 23. Вадкасць у пасудзіне знаходзіцца ў цеплавой раўнавазе з тонкай трубкай, запоўненай паветрам, якое закрыта кропелькай алею. Пры павелічэнні тэмпературы вадкасці аб’ём паветра, што знаходзіцца ў трубцы пад кропелькай алею, узрастае і кропелька рухаецца ўверх. Пры памяншэнні тэмпературы аб’ём паветра памяншаецца — і кропелька рухаецца ўніз.
Ці можна лічыць расшырэнне газу пры павольным награванні яго ў цыліндры з рухомым поршнем ізабарным працэсам?
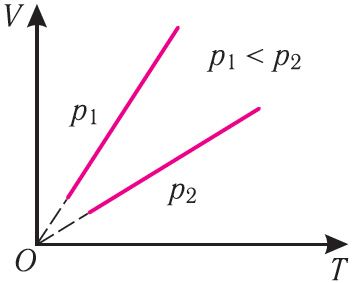
Паколькі V ~ T, то ў каардынатах (V, T) графік ізабарнага працэсу для ідэальнага газу ўяўляе з сябе прамую лінію, працяг якой праходзіць праз пачатак каардынат (мал. 24). Гэтую лінію называюць ізабарай.
Ізабара рэальных газаў не можа быць працягнутая да нулявога значэння тэмпературы (на графіку пункцірная лінія), бо пры нізкіх тэмпературах усе газы істотна адрозніваюцца ад мадэлі «ідэальны газ» і пры далейшым паніжэнні тэмпературы ператвараюцца ў вадкасці.
У адных і тых каардынатах (V, T) можна пабудаваць некалькі ізабар, якія будуць адпавядаць розным ціскам дадзенай масы ідэальнага газу пры нязменнай малярнай масе. Аналіз суадносін (6.2) дазваляе зрабіць выснову, што большаму ціску адпавядае меншы нахіл ізабары да восі тэмператур (гл. мал. 24).
Пабудуйце графікі ізабарнага працэсу ў каардынатах (p, V) і (p, T).