§ 2. Маса і памеры малекул. Колькасць рэчыва
Практыкаванне 1
1. Вызначце малярныя масы і масы малекул: а) вады H2O; б) вуглякіслага газу CO2; в) аміяку NH3; г) азотнай кіслаты HNO3.
2. У шклянку наліта вада H2O масай m = 0,20 кг. Вызначце колькасць рэчыва і колькасць малекул вады ў шклянцы.
3. Вызначце масу N = 4,5 · 1022 малекул серавадароду H2S.
4. Параўнайце колькасць часціц рэчыва ў алюмініевым і медным кубіках аднолькавага аб’ёму. Шчыльнасць алюмінію , шчыльнасць медзі
.
5. У сярэбранай пласцінцы N = 1,0 · 1024 атамаў. Вызначце аб’ём пласцінкі, калі шчыльнасць серабра ρ = 10,5 · 103 .
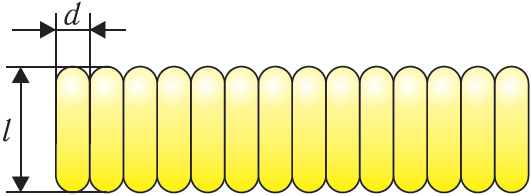
6. Англійскі фізік Джон Уільям Стрэт, лорд Рэлей (1842–1919), прапанаваў такі спосаб ацэнкі памераў малекул: на паверхню вады ў шырокай пасудзіне ён капнуў кроплю аліўкавага алею аб’ёмам V = 8,9 · 10–10 м3 і шчыльнасцю ρ = 9,0 · 102 . Кропля расцяклася, утварыўшы плёнку плошчай S = 0,55 м2. Вызначце па гэтых даных масу і дыяметр малекулы аліўкавага алею, палічыўшы таўшчыню плёнкі роўнай даўжыні цыліндрычных па форме малекул алею (мал. 13). Малярную масу аліўкавага алею палічыце роўнай M = 0,28
.
7. Вада ў адкрытай пасудзіне выпарылася за прамежак часу Δt = 6,0 сутак. Вызначце масу вады, якая знаходзілася ў пасудзіне, калі з яе паверхні кожную секунду вылятала ў сярэднім = 5,0 · 1018 малекул.
![]()
8. Маса газу, малекулы якога складаюцца з атамаў вадароду і вугляроду, m = 80 г. Вызначце масы ўсіх атамаў вадароду і вугляроду, калі лік малекул газу N = 3,01 · 1024.
9. Кропелька духоў, якая ўтрымлівае араматычнае рэчыва масай m = 2,0 · 10–4 г, выпарылася ў пакоі ўмяшчальнасцю V1 = 52 м3. Малярная маса араматычнага рэчыва . Вызначце сярэднюю колькасць
малекул гэтага рэчыва, якія трапляюць пры кожным удыху ў лёгкія чалавека, калі аб’ём паветра, якое ён удыхнуў, V2 = 2,2 л.