§ 2. Маса і памеры малекул. Колькасць рэчыва
| Сайт: | Профильное обучение |
| Курс: | Фізіка. 10 клас |
| Книга: | § 2. Маса і памеры малекул. Колькасць рэчыва |
| Напечатано:: | Гость |
| Дата: | Воскресенье, 6 Июль 2025, 08:43 |
У 1,0 см3 любога газу, які знаходзіцца пры нармальных умовах (тэмпература t0 = 0,0 °С, ціск р0 = 1,0 · 105 Па), змяшчаецца 2,7 · 1019 малекул. Каб уявіць, наколькі вялікі гэты лік, дапусцім, што з адтуліны ў ампуле ўмяшчальнасцю V = 1,0 см3 кожную секунду вылятае 100 малекул. Тады для таго, каб усе малекулы вылецелі з ампулы, спатрэбіцца 8,6 млрд гадоў, гэта значыць прамежак часу, параўнальны з узростам Сусвету (12–15 млрд гадоў). Такая велізарная колькасць малекул у рэчыве сведчыць пра тое, што іх памеры вельмі малыя. Якія ж памеры і маса часціц рэчыва? Як можна вызначыць колькасць атамаў у любым макраскапічным целе?
Малекулярна-кінетычная тэорыя дае магчымасць ацаніць масу і памеры часціц, якія ўтвараюць макраскапічныя целы. Малекулы, як і атамы, не маюць выразных межаў. Калі ўявіць малекулу ў выглядзе шарыка, то яе радыус мае значэнне ад 0,1 нм у самых простых да 100 нм у складаных малекул, якія змяшчаюць некалькіх тысяч атамаў. Напрыклад, ацэначны дыяметр малекулы вадароду складае 0,2 нм, а дыяметр малекулы вады — 0,3 нм. Пры такіх памерах колькасць часціц у рэчыве надзвычай вялікая. Напрыклад, у адным граме вады ўтрымліваецца 3,3 · 1022 малекул.
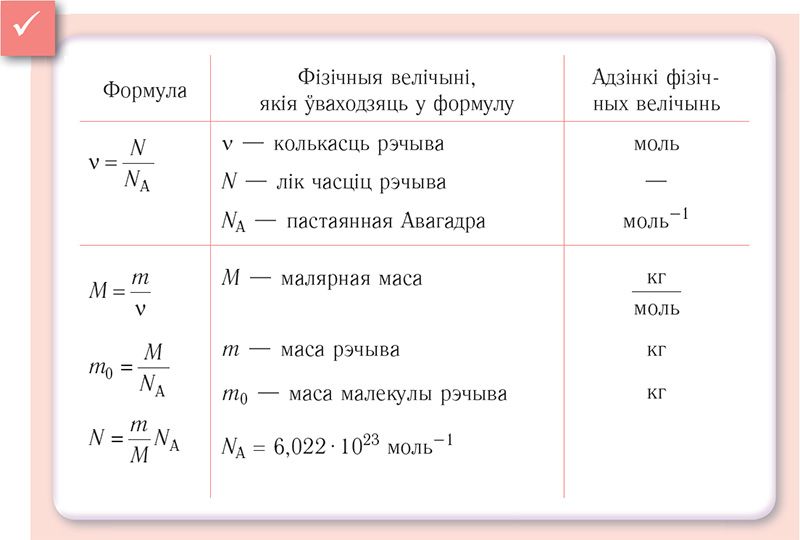
Памеры і маса малекулы ўзрастаюць з павелічэннем колькасці атамаў, з якіх яна складаецца. Атамы і малекулы (акрамя шмататамных малекул арганічных рэчываў) маюць масу прыкладна 10–26 кг. З прычыны малых значэнняў выражаць масы атамаў і малекул у кілаграмах (кг) нязручна. Таму для вымярэн ня мас атамаў і малекул у хіміі і фізіцы выкарыстоўваюць атамную адзінку масы (а. а. м.). Атамную адзінку масы выражаюць праз масу ізатопу вугляроду :
Масу малекулы (або атама), выражаную ў атамных адзінках масы, называюць адноснай малекулярнай масай Mr (або адноснай атамнай масай Ar). Адносная малекулярная (або атамная) маса Mr паказвае, у колькі разоў маса m0 малекулы (або атама) большая за атамную адзінку масы:
У Перыядычнай сістэме хімічных элементаў Д. І. Мендзялеева (гл. форзац 2) каля сімвалаў элементаў пазначаны і іх адносныя атамныя масы. У большасці выпадкаў пры правядзенні разлікаў значэнне адноснай атамнай масы акругляюць да цэлага ліку, выкарыстоўваючы правілы набліжаных вылічэнняў. Так, напрыклад, адносная атамная маса вадароду роўная 1, кіслароду — 16, азоту — 14.
Колькасць рэчыва, якая змяшчаецца ў макраскапічным целе, вызначаюць колькасцю часціц у ім. Прыведзеныя вышэй прыклады паказваюць, наколькі вялікі гэты лік. Таму пры разліках прынята выкарыстоўваць не абсалютную колькасць часціц рэчыва, а адносную:
гэта значыць колькасць рэчыва ν вызначаюць адносінамі ліку часціц N гэтага рэчыва да пастаяннай Авагадра NA.
Асноўнай адзінкай колькасці рэчыва ў СІ з’яўляецца моль. 1 моль роўны колькасці рэчыва, якая змяшчае столькі часціц, колькі атамаў утрымліваецца ў 0,012 кг ізатопу вугляроду . Значыць, у адным молі любога рэчыва знаходзіцца аднолькавая колькасць атамаў або малекул. Гэтую колькасць часціц абазначылі NA і назвалі пастаяннай Авагадра ў гонар італьянскага вучонага Амедэа Авагадра (1776–1856). Пастаянная Авагадра з’яўляецца адной з фундаментальных фізічных пастаянных, яе значэнне
NA = 6,022 · 1023 моль–1.
У малекулярна-кінетычнай тэорыі разам з адноснай малекулярнай (або атамнай) масай выкарыстоўваюць малярную масу M — масу рэчыва, узятага ў колькасці ν = 1 моль. Малярную масу M вызначаюць адносінамі масы m рэчыва да яго колькасці ν:
Асноўнай адзінкай малярнай масы ў СІ з’яўляецца кілаграм на моль . Малярная маса рэчыва звязана з яго адноснай малекулярнай масай наступнымі суадносінамі:
M = Mr · 10–3 .
Малярную масу рэчыва таксама можна вылічыць па формуле
M = m0NA.
З улікам таго, што , атрымаем формулу для разліку колькасці малекул у дадзеным рэчыве:
1. У колькі разоў лік малекул вадароду, узятага ў колькасці νв = 8 моль, большы за лік малекул азоту, колькасць рэчыва якога νа = 4 моль?
2. Выкарыстоўваючы выраз , разлічыце колькасць малекул у адным граме вады і пераканайцеся ў правільнасці прыведзенага ў пачатку параграфа значэння.
1. У якіх адзінках вымяраюць масы атамаў і малекул?
2. Што такое колькасць рэчыва? Назавіце адзінку гэтай фізічнай велічыні.
3. Што такое пастаянная Авагадра?
4. Што называюць малярнай масай рэчыва?
5. Растлумачце, чаму колькасць рэчыва ν, яго маса m і малярная маса М звязаны суадносінамі .
6. Дакажыце, што малярную масу М можна звязаць з адноснай малекулярнай (атамнай) масай Мr рэчыва суадносінамі .
7. Дакажыце, што канцэнтрацыю часціц рэчыва можна вызначыць па формуле , дзе m0 — маса адной малекулы, ρ — шчыльнасць рэчыва.
1. Прапануйце спосаб вызначэння прыкладнай колькасці малекул, якія выпарыліся з кожнага квадратнага сантыметра паверхні вады, налітай у шклянку, за прамежак часу Δt = 1 с.
Абсталяванне: шклянка з вадой, электронныя вагі (з як мага большай дакладнасцю вымярэння), секундамер, лінейка.
2. Прапануйце спосаб вызначэння колькасці часціц у кавалачку крэйды (СаСО3).
Абсталяванне: кавалачак крэйды, электронныя вагі.
Прыклад 1. Вызначце малярную масу і масу адной малекулы сульфату медзі(II) CuSO4.
Рашэнне. Каб вылічыць малярную масу М любога рэчыва, неабходна па хімічнай формуле знайсці адносную малекулярную масу Mr гэтага рэчыва і атрыманае значэнне памножыць на . Паколькі хімічная формула сульфату медзі(II) мае выгляд CuSO4, то
Тады малярная маса
Для вызначэння масы малекулы CuSO4 выкарыстаем формулу *:
Адказ:
Прыклад 2. Вызначце колькасць рэчыва і колькасць атамаў, якія змяшчаюцца ў жалезным бруску аб’ёмам V = 100 см3. Шчыльнасць жалеза .
N — ?
Рашэнне. Колькасць рэчыва можна вызначыць, выкарыстаўшы формулу , где m — маса жалезнага бруска, а
— малярная масcа жалеза. Паколькі
, то
.
Колькасць атамаў у дадзеным жалезным бруску .
Адказ: ν = 14 моль, N = 8,4 · 1024.
* Пры рашэнні задач постаянную Авагадра прыняць роўнай NA = 6,02 · 1023 моль–1 ↑
Практыкаванне 1
1. Вызначце малярныя масы і масы малекул: а) вады H2O; б) вуглякіслага газу CO2; в) аміяку NH3; г) азотнай кіслаты HNO3.
2. У шклянку наліта вада H2O масай m = 0,20 кг. Вызначце колькасць рэчыва і колькасць малекул вады ў шклянцы.
3. Вызначце масу N = 4,5 · 1022 малекул серавадароду H2S.
4. Параўнайце колькасць часціц рэчыва ў алюмініевым і медным кубіках аднолькавага аб’ёму. Шчыльнасць алюмінію , шчыльнасць медзі
.
5. У сярэбранай пласцінцы N = 1,0 · 1024 атамаў. Вызначце аб’ём пласцінкі, калі шчыльнасць серабра ρ = 10,5 · 103 .
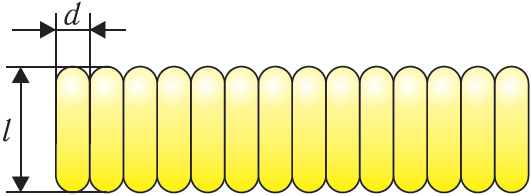
6. Англійскі фізік Джон Уільям Стрэт, лорд Рэлей (1842–1919), прапанаваў такі спосаб ацэнкі памераў малекул: на паверхню вады ў шырокай пасудзіне ён капнуў кроплю аліўкавага алею аб’ёмам V = 8,9 · 10–10 м3 і шчыльнасцю ρ = 9,0 · 102 . Кропля расцяклася, утварыўшы плёнку плошчай S = 0,55 м2. Вызначце па гэтых даных масу і дыяметр малекулы аліўкавага алею, палічыўшы таўшчыню плёнкі роўнай даўжыні цыліндрычных па форме малекул алею (мал. 13). Малярную масу аліўкавага алею палічыце роўнай M = 0,28
.
7. Вада ў адкрытай пасудзіне выпарылася за прамежак часу Δt = 6,0 сутак. Вызначце масу вады, якая знаходзілася ў пасудзіне, калі з яе паверхні кожную секунду вылятала ў сярэднім = 5,0 · 1018 малекул.
![]()
8. Маса газу, малекулы якога складаюцца з атамаў вадароду і вугляроду, m = 80 г. Вызначце масы ўсіх атамаў вадароду і вугляроду, калі лік малекул газу N = 3,01 · 1024.
9. Кропелька духоў, якая ўтрымлівае араматычнае рэчыва масай m = 2,0 · 10–4 г, выпарылася ў пакоі ўмяшчальнасцю V1 = 52 м3. Малярная маса араматычнага рэчыва . Вызначце сярэднюю колькасць
малекул гэтага рэчыва, якія трапляюць пры кожным удыху ў лёгкія чалавека, калі аб’ём паветра, якое ён удыхнуў, V2 = 2,2 л.