§ 37.1. Аксіды азоту(II) і (IV)
Аксід азоту(IV). Атрыманне і хімічныя ўласцівасці
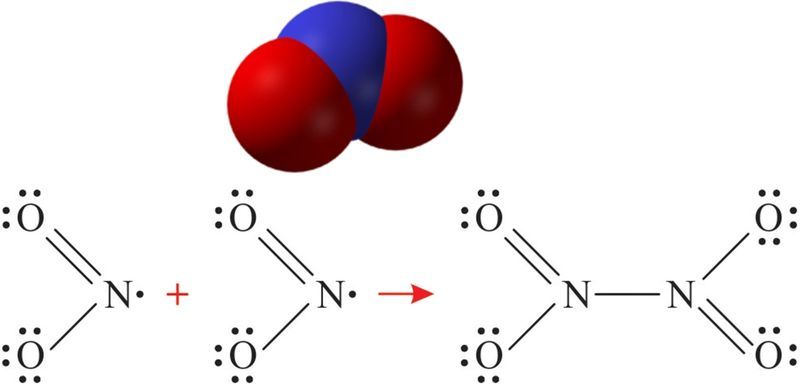
Малекула NO2 мае вуглавую форму (мал. 94.1). Мяркуецца, што атам азоту знаходзіцца ў стане sp2-гібрыдызацыі, даўжыня сувязі N—O роўная 0,119 нм, што адпавядае паўтарачнай сувязі.
Аксід азоту(IV) NO2, дыаксід азоту — газ бурага колеру (Тпл. −11,2 °С, Tкіп. 21 °С), у вадкім і цвёрдым стане бясколерны і складаецца з малекул N2O4 у выніку дымерызацыі:
2NO2 N2O4 + Q.
Дымерызацыя лёгка адбываецца з-за наяўнасці няспаранага электрона. У газападобным стане аксід азоту(IV) дымерызаваны часткова.
У лабараторыі звычайна яго атрымліваюць вядомай вам рэакцыяй канцэнтраванай азотнай кіслаты з меддзю:
Cu + 4HNO3(канц) = Cu(NO3)2 + 2NO2↑ + 2H2O
або раскладаннем некаторых нітратаў (§ 38).
Аксід азоту(IV) узаемадзейнічае з вадой. У залежнасці ад умоваў утвараюцца розныя прадукты. Так, пры пакаёвай тэмпературы ўтвараюцца азотная і азоцістая кіслоты:
.
Пры растварэнні NO2 у вадзе пры павышанай тэмпературы ў лішку кіслароду ўтвараецца азотная кіслата:
.
Раўнавагу гэтай абарачальнай рэакцыі пры прамысловым атрыманні азотнай кіслаты зрушваюць управа, павялічваючы ціск.
Пры растварэнні NO2 у шчолачах утвараюцца нітраты разам з нітрытамі:
Недастатковая ачыстка газаў, што вылучаюцца ў навакольнае асяроддзе прадпрыемствамі, якія вырабляюць азотную кіслату, катламі электрастанцый, газатурбіннымі ўстаноўкамі, рухавікамі аўтамабіляў і самалётаў, прыводзіць да забруджвання атмасферы аксідамі азоту. Пад дзеяннем кіслароду NO ператвараецца ў NO2. У вільготнай атмасферы ўтвараецца азотная кіслата, і на зямлю выпадаюць кіслотныя дажджы, шкодныя не толькі для чалавека і жывёл, але і для раслін. Пад дзеяннем кіслотных дажджоў разбураюцца збудаванні.
Газападобны аксід азоту(I) N2O пры ўдыханні прыводзіць да зніжэння болевай адчувальнасці, таму яго часам ужываюць у сумесі з кіслародам для наркозу.
Аксід N2O3 устойлівы толькі пры нізкіх тэмпературах (Тпл. −102 °С, Ткіп. 4 °С, Траскл. 4,5 °С) і ўяўляе сабой вадкасць блакітнага колеру. Пры ўзаемадзеянні з вадой утварае азоцістую кіслату:
.
Аксід азоту(V) N2O5 — цвёрдае рэчыва белага колеру. Рэагуючы з вадой, утварае азотную кіслату:
.