§ 30. Галагены
*Атрыманне хлору ў лабараторыі і прамысловасці
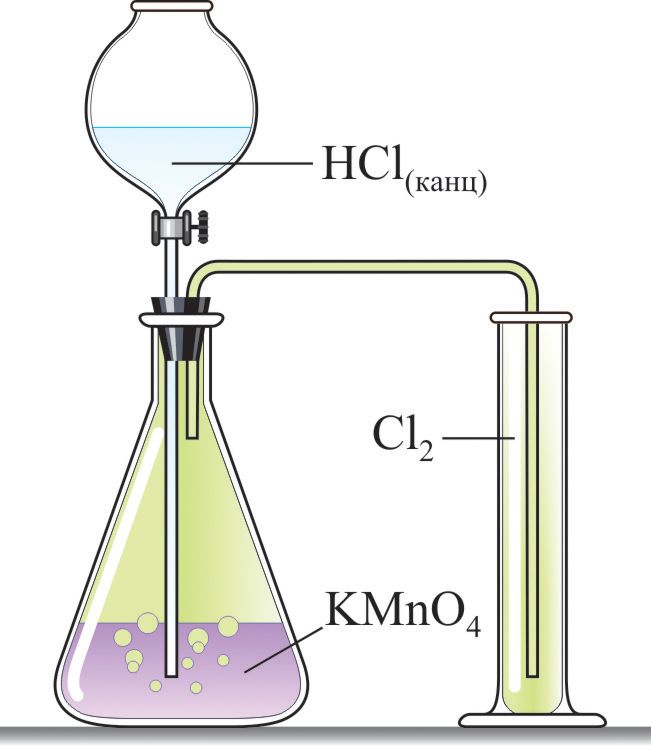
Для атрымання хлору ў лабараторыі выкарыстоўваюць рэакцыю канцэнтраванай салянай кіслаты з моцнымі акісляльнікамі (МnO2, KМnO4, KClO3) (мал. 69.1):
;
.
Каб выдаліць следавыя колькасці хлоравадароду, атрыманы газ прапускаюць праз ваду, а для выдалення пароў вады — праз канцэнтраваную серную кіслату.
Упершыню хлор атрымаў шведскі хімік Карл Вільгельм Шэеле (1742–1786) пры ўзаемадзеянні мінералу піралюзіту, г. зн. аксіду марганцу(IV), і салянай кіслаты ў 1774 годзе. Вучонаму належыць гонар адкрыцця мноства неарганічных і арганічных рэчываў.
У прамысловасці хлор атрымліваюць у асноўным электролізам воднага раствору хларыду натрыю. Пры гэтым на анодзе вылучаецца хлор, а на катодзе — вадарод.
Хлор таксама ўтвараецца пры электролізе расплаву хларыду натрыю:
2NaCl(расплаў) 2Na + Cl2↑.
Больш падрабязна працэсы электролізу вы разгледзіце ў раздзеле «Металы».