§ 30. Галагены
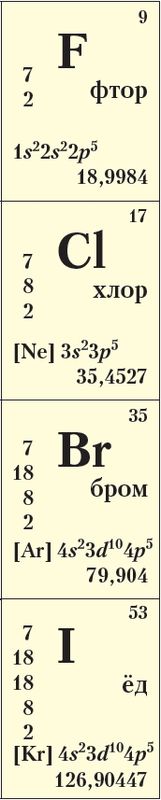
Галагены як хімічныя элементы
Да галагенаў адносяць пяць элементаў VIIА-групы перыядычнай сістэмы: фтор F, хлор Сl, бром Вr, ёд I і астат At.
Атамы галагенаў утрымліваюць па 7 электронаў на знешнім электронным слоі, агульная электронная канфігурацыя якога ns2np5, гэта значыць галагены з’яўляюцца р-элементамі (Дадатак 1). Электроннаграфічныя схемы знешняга электроннага слоя атамаў фтору і хлору выглядаюць наступным чынам:
Пры гэтым на знешнім электронным слоі ў атама фтору чатыры арбіталі, а атамы астатніх галагенаў змяшчаюць яшчэ пяць незапоўненых d-арбіталей.
Фтор як самы электраадмоўны элемент у злучэннях праяўляе толькі адмоўную ступень акіслення –1. Характэрныя для іншых элементаў ступені акіслення (–1, +1, +3, +5, +7) можна растлумачыць магчымасцю распарвання электронаў знешняга электроннага слоя. У выпадку атамаў хлору гэта выглядае так:
Ступені акіслення +1, –1, 0
Ступень акіслення +5
Ступень акіслення +3
Ступень акіслення +7
Прыкладамі злучэнняў з рознымі ступенямі акіслення хлору могуць служыць вядомыя вам рэчывы: (галіт),
(берталетава соль),
(хлорная кіслата).
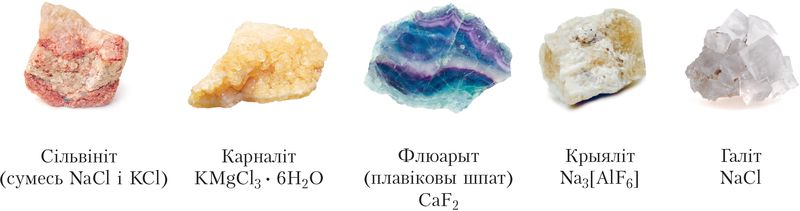
У прыродзе галагены існуюць у выглядзе злучэнняў з іншымі элементамі (табл. 21, мал. 68). Фтор і хлор належаць да дваццаці самых распаўсюджаных элементаў у зямной кары.
Табліца 21. Хімічныя элементы галагены
| Элемент | Радыус атама, нм | χ | Ступені акіслення | Прыродныя злучэнні |
| Фтор 9F | 0,071 | 4,0 | –1, 0 | CaF2 (флюарыт, плавіковы шпат); Na3[AlF6] (крыяліт);); Са5[РО4]3F (фторапатыт)) |
| Хлор 17Cl | 0,099 | 3,0 | –1, 0, +1, +3, +5, +7 | NaCl (каменная соль, галіт); KCl (сільвін);); Смесь NaCl и KCl (сільвініт); KMgCl3 · 6H2O (карналіт) |
| Бром 35Br | 0,114 | 2,8 | –1, 0, +1, +3, +5, +7 | NaBr, KBr, MgBr2 — у адкладах хларыдаў; у марской вадзе ў выглядзе брамід-іонаў |
| Ёд 53I | 0,133 | 2,5 | –1, 0, +1, +3, +5, +7 | KIO3 (ёдат калію) — у адкладах чылійскай салетры, у падземных буравых водах, у марскіх водарасцях |