§ 49. Железо и его соединения
Коррозия железа
Изделия из железа в технике, быту, природе подвергаются коррозии. Коррозия — разрушение металла в результате взаимодействия с веществами из окружающей среды.
Причины коррозии. Условно процесс коррозии железа во влажной атмосфере можно представить уравнением:
.
Образующийся Fe(OH)3 подвергается частичной дегидратации — удалению воды — и поэтому состав ржавчины выражают формулой Fe2O3 · xH2O.
При высоких температурах может происходить окисление сухим кислородом с образованием Fe3O4:
.
В окружающей среде в присутствии иных окислителей, например кислот и кислотных оксидов, образуются соли железа.
Во всех этих процессах железо окисляется и разрушается, компоненты окружающей среды восстанавливаются. Продукты окисления железа образуются в виде рыхлых слоёв, не защищающих металл от дальнейшей коррозии (§ 20, рис. 47, б).
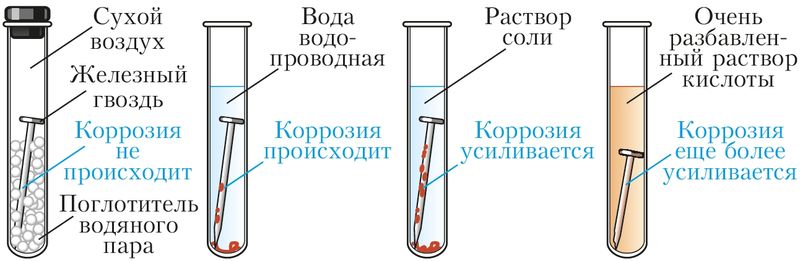
Скорость коррозии, как и в случае других окислительно-восстановительных процессов, зависит от химической природы и площади соприкосновения реагентов, их концентрации, температуры. Коррозию ускоряют растворы солей и кислот (рис. 113). Коррозию замедляют, полируя поверхность металла, сохраняя металл в сухом воздухе. Коррозия железа замедлена в растворах щелочей или при контакте с более активным, чем железо, металлом (рис. 114).
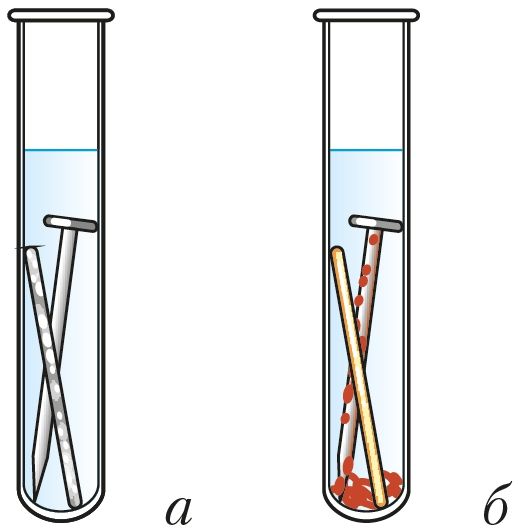
Из курса химии 9-го класса вам известно, что скорость коррозии увеличивается при контакте железа с менее активным металлом (рис. 114).
Знание факторов, влияющих на скорость коррозии, позволило предложить ряд способов защиты от коррозии.
1. Защитные покрытия. В качестве материалов для металлических покрытий применяют цинк, никель, медь, хром, серебро, бронзу, латунь и др. (рис. 115). Так, оцинкованное железо используют в качестве кровельного материала, в изготовлении кузовов автомобилей, шурупов. В этом случае железо не будет разрушаться до тех пор, пока не прореагирует всё покрытие из цинка. Покрытия из менее активных металлов, чем железо, защищают его от коррозии лишь в случае, если в них отсутствуют поры, трещины, царапины.

К неметаллическим покрытиям относят лакокрасочные и полимерные материалы, смазочные масла.
Защитные покрытия также получают путём оксидирования (создание слоя окалины Fe3O4) и фосфатирования (нанесение слоя фосфатов) поверхности металла.
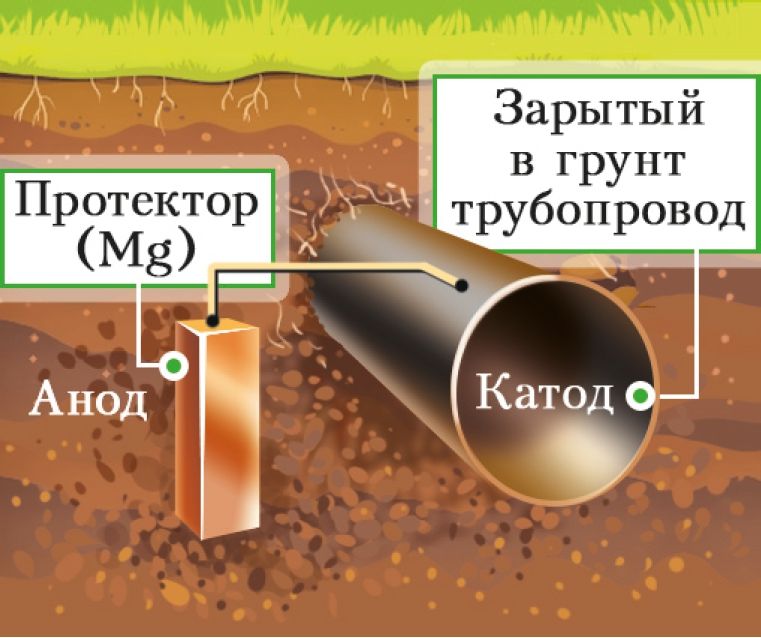
2. Электрохимическая защита осуществляется подключением защищаемой конструкции к отрицательному полюсу внешнего источника постоянного тока (катодная защита) или приведением защищаемого металла в контакт с более активным металлом (рис. 116).
3. Легирование металлов. В расплав металла при его производстве добавляют легирующие добавки — хром, никель, молибден и др., снижающие активность металла. Таким образом получают, например, нержавеющую сталь.
4. Изменение состава и свойств коррозионной среды. Коррозионную среду можно изменить добавлением в неё ингибиторов (веществ, которые значительно уменьшают скорость коррозии металла, например нитрита, фосфата или хромата натрия и ряда других).

Применение железа и его сплавов. До 95 % всего добываемого железа производится в виде его сплавов — чугуна и сталей. С составом, свойствами и сферами применения этих сплавов вы уже ознакомились, изучая материал § 43, а с методами получения — в § 45. Напомним, что содержание углерода в сталях ниже 2 %, то есть гораздо меньше, чем в чугуне, поэтому сталь — более ковкий, прочный и менее хрупкий сплав по сравнению с чугуном. Она легко подвергается механической обработке (режется, шлифуется, прокатывается, куётся).
Чугун — более дешёвый сплав с хорошими литейными свойствами, но более хрупкий. Изделия из чугуна более коррозионноустойчивы, чем из нелегированной стали (рис. 117). Различие в свойствах определило и разные области использования сплавов железа.
Чистое железо используется как катализатор, например в синтезе аммиака, бромировании бензола.