§ 14. Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам изменения состояния идеального газа
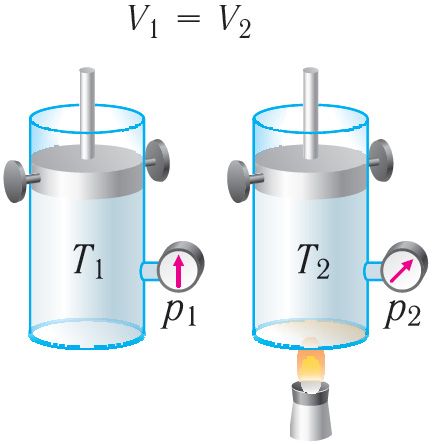
Изохорный процесс. Пусть идеальный одноатомный газ находится в цилиндрическом сосуде, закрытом неподвижным поршнем (V = const). Нагреем цилиндр с газом. Объём газа остаётся практически постоянным (тепловым расширением сосуда пренебрегаем) (рис. 78), следовательно, работа силы давления газа A = 0. Тогда первый закон термодинамики примет вид
![]()
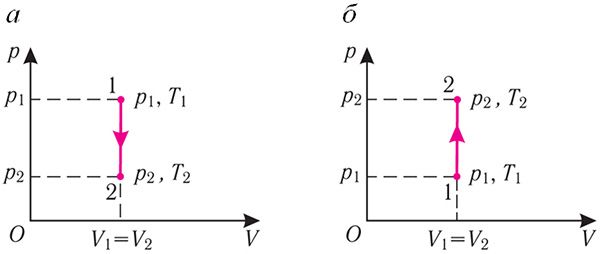
Это означает, что всё передаваемое газу количество теплоты идёт на увеличение его внутренней энергии. При этом приращение внутренней энергии газа (рис. 78.1, а). Если же газ при изохорном процессе отдаёт количество теплоты, то его внутренняя энергия убывает:
(рис. 78.1, б).
1. Каково приращение внутренней энергии идеального газа, если при изохорном процессе от него было отведено количество теплоты Q = –560 Дж?
![]()
2. Как изменяются внутренняя энергия и давление определённой массы идеального газа при изохорном повышении температуры?