§ 11. Термодинамическая система. Внутренняя энергия. Внутренняя энергия идеального одноатомного газа
Пример 1. При изобарном охлаждении внутренняя энергия идеального одноатомного газа изменилась на ΔU = –6,0 · 102 Дж. Определите давление газа, если его объём изменился на ΔV = –1,0 · 102 см3.
ΔU = –6,0 · 102 Дж
ΔV = –1,0 · 102 см3 = –1,0 · 10–4 м3
Решение: Приращение внутренней энергии некоторого количества идеального одноатомного газа
(1)
Используя уравнение Клапейрона–Менделеева, можно осуществить замену:
(2)
Решая совместно уравнения (1) и (2), получим: .
.
Ответ: .
![]()
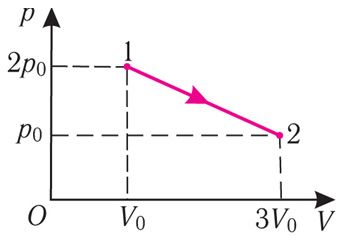
Пример 2. На рисунке 65.1 в координатах (p, V) изображён процесс перехода определённой массы идеального одноатомного газа из состояния 1 в состояние 2. Определите изменение внутренней энергии газа, если его давление в конечном состоянии p0 = 1,5 МПа, а объём в начальном состоянии V0 = 2,0 л.
p0 = 1,5 МПа = 1,5 · 106 Па
V0 = 2,0 л = 2,0 · 10–3 м3
Решение: Приращение внутренней энергии идеального одноатомного газа . Используя уравнение Клапейрона‒Менделеева для состояний 1 и 2, можно определить значение выражения
. Анализируя рисунок 65.1, следует сделать вывод, что в состоянии 1 давление газа 2p0, а его объём V0, а в состоянии 2 — p0 и 3V0. Тогда уравнение Клапейрона‒Менделеева для состояний газа 1 и 2 примет вид:
,
.
Вычтем из уравнения (2) уравнение (1): и получим, что
. Тогда
.
Ответ: ΔU = 4,5 кДж.