§ 11. Термодинамическая система. Внутренняя энергия. Внутренняя энергия идеального одноатомного газа
Внутренняя энергия идеального одноатомного газа. Определим внутреннюю энергию идеального одноатомного газа, т. е. газа, образованного атомами. Например, одноатомными газами являются инертные газы — гелий, неон, аргон и др.
Из определения понятия «идеальный газ» следует, что его внутренняя энергия является суммой кинетических энергий хаотического движения всех атомов (или молекул) (потенциальная энергия взаимодействия между частицами отсутствует). Следовательно, внутренняя энергия идеального одноатомного газа равна произведению средней кинетической энергии теплового движения частиц на их число
, т. е.
. Поскольку
,
где — масса газа, а
, то
.
С учётом того, что произведение постоянной Больцмана и постоянной Авогадро , где
— универсальная газовая постоянная, получим:
,
(11.1)
или
.
Из формулы (11.1) следует, что внутренняя энергия данной массы идеального одноатомного газа пропорциональна его абсолютной температуре. Она не зависит от других макроскопических параметров состояния — давления и объёма. Следовательно, изменение внутренней энергии данной массы одноатомного идеального газа происходит только при изменении его температуры:
1. Воздух при комнатной температуре и нормальном атмосферном давлении можно описывать моделью идеального газа. Как показывают расчёты, внутренняя энергия двухатомного газа больше внутренней энергии одинакового количества одноатомного газа, находящегося при такой же температуре, в раза. Учитывая, что воздух состоит в основном из двухатомных молекул, оцените внутреннюю энергию воздуха в комнате, длина которой
, ширина
, высота
.
Сравните полученный результат с кинетической энергией грузового автомобиля массой , движущегося со скоростью, модуль которой
. Сделайте вывод.
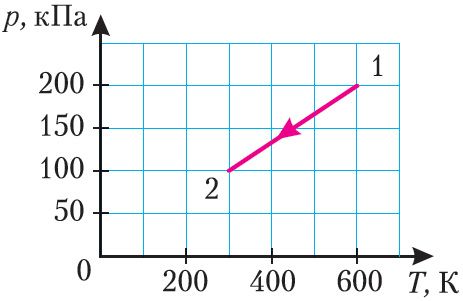
2. Идеальный одноатомный газ, количество вещества которого , перевели из состояния 1 в состояние 2 (рис. 64). Как и на сколько изменилась внутренняя энергия газа?
При определении внутренней энергии реальных газов, жидкостей и твёрдых тел необходимо учитывать потенциальную энергию взаимодействия частиц, которая зависит от расстояния между ними. Поэтому в общем случае внутренняя энергия макроскопических тел зависит не только от абсолютной температуры, но и от объёма.
Изменить внутреннюю энергию термодинамической системы можно двумя способами: используя теплообмен и совершая работу. Процесс теплообмена и совершение работы характеризуют соответственно физическими величинами — количеством теплоты Q и работой А, которые являются мерами изменения внутренней энергии системы.

1. Что называют термодинамической системой?
2. Что понимают под внутренней энергией макроскопического тела? Термодинамической системы?
3. Что представляет собой внутренняя энергия идеального газа? От чего зависит её значение?
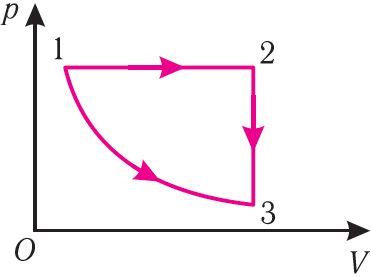
4. Идеальный газ переводят из состояния 1 в состояние 3 двумя различными способами: изотермически (1 3) и осуществляя сначала изобарное расширение, а затем изохорное охлаждение (1
2
3) (рис. 65). Зависит ли приращение внутренней энергии газа от способа его перехода из состояния 1 в состояние 3?
5. От каких параметров зависят значения внутренней энергии идеального газа и внутренней энергии реальных газов?