§ 5. Предмет органической химии. Теория строения органических веществ
Теория строения органических веществ
Теория строения органических веществ сформировалась во второй половине XIX века. К этому времени были получены и исследованы многие органические соединения, установлен их качественный и количественный состав, описаны свойства.
Так, в конце XVIII — начале XIX века были выделены важнейшие углеводороды (органические вещества, состоящие только из углерода и водорода) и установлены их молекулярные формулы. Однако оказалось, что знания молекулярных формул, отражающих только состав вещества, явно недостаточно для понимания строения и свойств органических соединений. Приведём примеры некоторых противоречий, заводивших в тупик учёных первой половины XIX века.
Пример 1. Молекулярные формулы простейших углеводородов метана, этана и пропана — CH4, C2H6 и C3H8 соответственно.
К середине XIX века Э. Франкландом уже было предложено понятие валентности атомов, а А. Кекуле предположил, что атомы углерода четырёхвалентны. Если исходить из того, что водород одновалентен, то, рассматривая приведённые молекулярные формулы, можно ошибочно предположить, что только в метане CH4 углерод имеет валентность, равную четырём, валентность углерода в этане C2H6 должна равняться трём, а в пропане C3H8 углерод должен иметь дробную валентность.
 Пример 2. Одинаковую формулу C4H10 имеют два различных вещества.
Пример 2. Одинаковую формулу C4H10 имеют два различных вещества.
Температура кипения одного из этих веществ равна –0,5 °С, тогда как температура кипения второго более чем на 11 °С ниже и составляет –12 °С. Накопление подобных необъяснимых на тот момент фактов стало предпосылкой создания новой теории — теории строения органических соединений. Её основные положения в середине XIX века сформулировал А. М. Бутлеров.
К тому времени было известно, что молекулы состоят из атомов, но учёные ещё не придавали значения тому, как атомы располагаются в молекуле, и считали, что познать это невозможно. А. М. Бутлеров высказал предположение о том, что атомы в молекуле соединены в определённой последовательности, которую можно установить химическими методами и отразить в структурной формуле.
Сформулируем важнейшие положения теории строения органических соединений А. М. Бутлерова:
- Атомы, входящие в состав органических соединений, связаны друг с другом в определённой последовательности в соответствии с их валентностью.
- Свойства вещества зависят не только от того, атомы каких элементов и в каком количестве входят в состав молекул, но и от последовательности соединения атомов в молекулах.
Данная теория открыла путь к широкому распространению структурных формул для отображения строения органических веществ.
Используем положения теории А. М. Бутлерова для объяснения противоречий, описанных в примерах 1 и 2.
Сначала объясним строение молекул простейших углеводородов. Учитывая, что валентность углерода равна четырём, а валентность водорода — единице, структурная формула метана CH4 следующая:
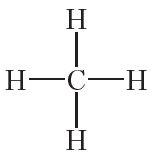
В молекуле этана C2H6 все атомы углерода и водорода входят в состав одной частицы. Для этого два атома углерода должны образовать друг с другом химическую связь. Оставшиеся три единицы валентности каждый атом углерода использует для соединения с тремя атомами водорода. Тогда структурная формула этана:
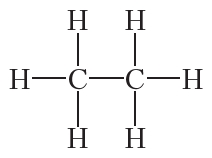
Аналогичные рассуждения для пропана C3H8 приводят к структурной формуле:
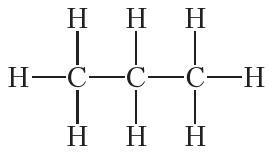
Как видно, во всех этих углеводородах углерод четырёхвалентен. Рассмотрим теперь, какое влияние на свойства веществ оказывает последовательность связывания атомов в молекуле на примере соединения с молекулярной формулой C4H10. Можно составить две цепи из четырёх атомов углерода: линейную и разветвлённую:

Таким образом, молекулярную формулу C4H10 имеют два вещества:
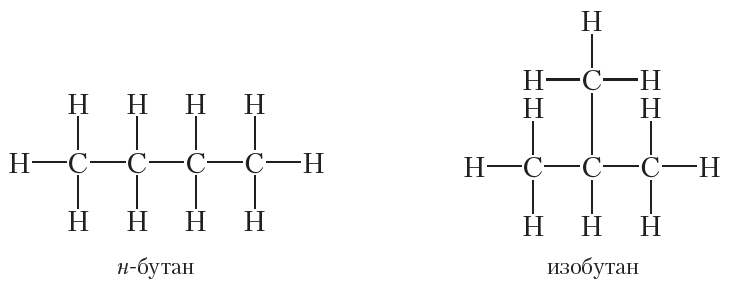
Так как н-бутан (н — сокращённое от нормальный) и изобутан являются разными веществами, они должны иметь различные свойства. Действительно, температура кипения н-бутана равна –0,5 °С, тогда как температура кипения изобутана равна –12 °С. Таким образом, теория Бутлерова позволила объяснить, почему соединения, имеющие совершенно одинаковый состав, могут обладать различными свойствами. Вещества, молекулы которых имеют одинаковый качественный и количественный состав, но разное строение, называются изомерами.
Дальнейшее развитие науки только дополняло и совершенствовало теорию А. М. Бутлерова, показало её справедливость не только для органических, но и для неорганических соединений. Структурные формулы, впервые предложенные А. М. Бутлеровым, и сегодня с успехом используются для отображения строения молекул как органических, так и неорганических соединений.
Значение теории состоит в систематизации огромного фактического материала, что дало возможность целенаправленного синтеза новых веществ с заданными свойствами.
|
Органическая химия — химия соединений углерода. Органические соединения являются основой живых организмов. В основе теории строения органических соединений А. М. Бутлерова лежат представления о том, что свойства веществ определяются не только их составом, но и последовательностью соединения атомов в молекуле. Молекулы различных веществ могут иметь одинаковый состав, но разную последовательность соединения атомов в молекуле. |