§ 42. Угольная и кремниевая кислоты, их соли
Кремниевая кислота и её соли
Кремниевая кислота H2SiO3 является двухосновной и более слабой, чем угольная кислота. Её получают взаимодействием силикатов (Na2SiO3 или K2SiO3) с более сильными кислотами, например H2SO4, HCl:
Кремниевая кислота при этом выделяется в виде студенистого осадка, состав которого часто выражают формулой nSiO2 · mH2O. В действительности кремниевая кислота имеет полимерную природу:
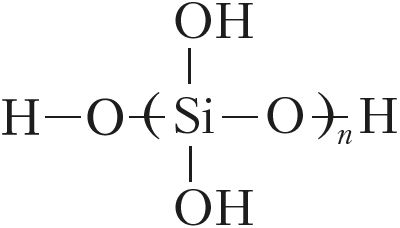
Уже при незначительном нагревании или длительном хранении кислота разлагается на оксид и воду:
.
Образующийся оксид SiO2 имеет пористую структуру и большую площадь поверхности (до 1000 м2/г), что позволяет ему адсорбировать молекулы различных веществ, в том числе и воду. Именно благодаря адсорбционным свойствам оксид SiO2 под названием «силикагель» используется как осушитель воздуха в упаковках с электроникой и обувью, а под названием «Белый уголь» — как адсорбент в медицине (рис. 101).
