§ 3.5. Узаемасувязь паміж класамі неарганічных злучэнняў
| Сайт: | Профильное обучение |
| Курс: | Хімія. 11 клас |
| Книга: | § 3.5. Узаемасувязь паміж класамі неарганічных злучэнняў |
| Напечатано:: | Гость |
| Дата: | Воскресенье, 17 Август 2025, 09:37 |
Разнастайнасць неарганічных злучэнняў найбольш лагічна адлюстроўваюць так званыя генетычныя рады, што ўтрымліваюць злучэнні аднаго элемента, якія належаць розным класам. Як правіла, такі рад прадстаўлены элементам, яго аксідам, гідраксідам і адпаведнай соллю. Напрыклад, генетычны рад тыповага металу і генетычны рад неметалу выглядаюць так:
| Метал | → | асноўны аксід | → | гідраксід (аснова) | → | соль |
| Са | → | СаО | → | Са(ОН)2 | → | Са(NO3)2 |
| Неметал | → | кіслотны аксід | → | гідраксід (кіслата) | → | соль |
| S | → | SO2 | → | Н2SO3 | → | Na2SO3 |
Стрэлка (→) у дадзеных схемах азначае «адпавядае». Так, тыповаму металу адпавядаюць асноўны аксід, гідраксід, соль, у прыватнасці Са — аксід СаО, гідраксід Са(ОН)2, соль Са(NO3)2.
Уласцівасці злучэнняў металаў і неметалаў па сваёй сутнасці процілеглыя, таму рэчывы розных генетычных радоў могуць узаемадзейнічаць адно з адным, утвараючы пераважна солі. Некаторыя варыянты такіх парных узаемадзеянняў могуць быць паказаны схемамі на аснове генетычных радоў, з якіх відаць, што прадуктамі ўзаемадзеяння рэчываў розных генетычных радоў з’яўляюцца, галоўным чынам, солі (мал. 6.5, 6.6).
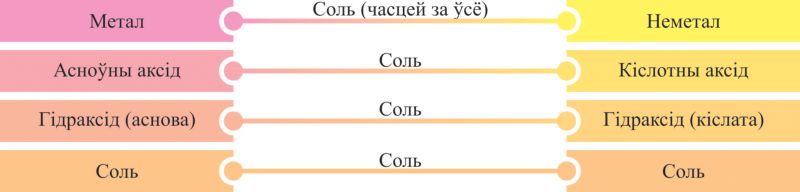
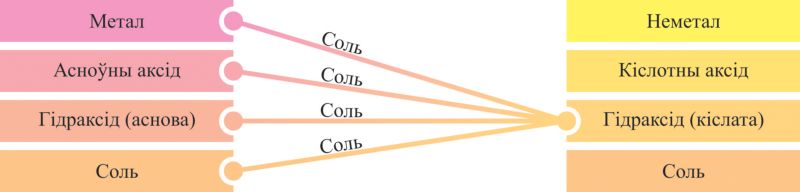
Пры ўзаемадзеянні металаў і неметалаў утвараюцца як солі (галагеніды, сульфіды — NaCl, Al2S3), так і бінарныя злучэнні, якія не адносяцца да класа солей (нітрыды, фасфіды, карбіды, гідрыды, аксіды — Li3N, Ca3P2, Al4C3, NaH, CaO).
Генетычныя рады ў арганічнай хіміі ўтвараюць злучэнні, якія ўтрымліваюць аднолькавы лік атамаў вугляроду:
С3Н8 → С3Н7Сl → С3Н7ОН → C2H5СНО → C2H5СОOH → CH3CH(Cl)СОOH → CH3CH(NH2)СОOH → NH—CH(CH3)CO
Веданне асаблівасцей кожнага віду ўзаемадзеянняў неабходна пры выкананні розных заданняў і рашэнні эксперыментальных задач. У практычнай дзейнасці хімікі атрымліваюць новыя рэчывы з наяўных у іх распараджэнні: напрыклад, серную кіслату — з сернага калчадану, аміяк — з азоту, азотную кіслату — з аміяку, цынк — з цынкавай падманкі і г. д. Пры гэтым, як правіла, неабходна правесці серыю рэакцый, каб атрымаць патрэбны прадукт. Напрыклад, адзін з варыянтаў атрымання цынку з прыроднага мінералу ZnS можна паказаць схемай ператварэнняў:
ZnS → ZnO → Zn,
для ажыццяўлення якіх неабходны рэакцыі:
1) акіслення сульфіду цынку кіслародам (абпал):
2ZnS + 3O2 = 2ZnO + 2SO2;
2) аднаўлення металу з аксіду:
ZnO + С = СО + Zn.
На выбар шляху ператварэнняў і распрацоўку тэхналагічных працэсаў уплываюць веданне ўласцівасцей рэчываў, улік даступнасці рэагентаў, бяспекі працэсаў і многія іншыя фактары.
У якасці прыкладу разгледзім ператварэнне рэчываў аднаго генетычнага раду — асноўнага аксіду ў гідраксід.
Прыклад 1. Складзіце ўраўненне рэакцыі, якая дазваляе атрымаць шчолач з асноўнага аксіду: СаО → Са(ОН)2.
Рашэнне
Паколькі кальцый — актыўны метал, то яго аксід рэагуе з вадой, утвараючы шчолач:
CaO + H2O = Ca(OH)2 (узаемадзеянне актыўнага металу з вадой).
Прыклад 2. Складзіце ўраўненні рэакцый, якія дазваляюць атрымаць нерастваральную аснову з асноўнага аксіду: FeO → Fe(OH)2.
Рашэнне
Паколькі Fe(OH)2 — нерастваральная аснова, то яе можна атрымаць толькі з раствору солі. Значыць, зыходны аксід FeO неабходна першапачаткова перавесці ў растваральную соль:
FeO + Н2SO4 = FeSO4 + H2O (растварэнне аксіду ў кіслаце, атрыманне растваральнай солі
Потым да раствору солі неабходна дадаць раствор шчолачы:
FeSO4 + 2NaOH → Fe(OH)2↓ + NaSO4 (атрыманне нерастваральнай асновы ўзаемадзеяннем раствораў солі і шчолачы).
Такім чынам, выбар рэагентаў залежыць ад таго, чым з’яўляецца прадукт ператварэння — гідраксід металу: шчолаччу або нерастваральнай асновай. Для атрымання шчолачы з аксіду дастаткова мець ваду, а нерастваральную аснову можна атрымаць толькі з раствору солі. Таму аксід неабходна папярэдне ператварыць у растваральную соль, а потым дадаць раствор шчолачы.
Пытанні, заданні, задачы
1. Выпішыце хімічныя формулы рэчываў, якія ўтвараюць генетычны рад магнію: МnO, Mn(OH)2, Mg(OH)2, MgO, K2SO4, MgSO4, Mg, Mn, MnSO4.
2. Запоўніце табліцу, выкарыстоўваючы формулы рэчываў: Fe(ОН)2, СаО, Н2SO4, SО3, СО2, NaOH, Na2SO4, НСl, Н2SO3, K3PO4, Ba(ОН)2, КСl.
| Оксиды | Кислоты | Основания | Соли |
3. Складзіце генетычныя рады металаў:
- а) … → … → … → хларыд магнію;
- б) … → … → … → сульфат цынку;
- в) … → аксід натрыю → … → …;
- г) … → … → гідраксід калію → ….
4. Складзіце ўраўненні рэакцый паводле малюнка 6 на прыкладзе сернай кіслаты.
5. Складзіце ўраўненні рэакцый для двух ператварэнняў:
- а) ВаО → Ba(ОH)2 и Al2O3 → Al(ОH)3;
- б) Li2О → LiОH и Fe2O3 → Fe(ОH)3.
Чаму вам спатрэбілася скласці розную колькасць ураўненняў рэакцый у прапанаваных ператварэннях?
6. Складзіце генетычны рад натрыю і генетычны рад вугляроду. У чым іх прынцыповае адрозненне? Напішыце ўраўненні рэакцый, якія дазваляюць ажыццявіць паслядоўнае атрыманне рэчываў у кожным радзе.
7. Разлічыце масу цынку, атрыманага ў выніку ператварэнняў: Zn → ZnO → Zn, калі маса зыходнага сульфіду цынку роўная 29,1 г, а страты склалі 5 %.
8. Складзіце ўраўненні рэакцый згодна са схемай:
- a) Вa
ВаО
Вa(OH)2
ВаСl2
ВaCO3
…;
- б) С
СО2
Н2СO3
Na2СO3
CaCO3
….
9. Вызначце простае рэчыва Х у генетычным радзе і складзіце ўраўненні адпаведных рэакцый:
Х Х2О5
Н3ХO4
K3ХO4,
калі масавая доля кіслароду ў злучэнні K3ХO4 роўная 30,19 %.
10. Вызначце простае рэчыва Х у генетычным радзе і складзіце ўраўненні адпаведных рэакцый:
ХХО2
Н2ХO3
NaНХO3,
калі масавая доля элемента Х у злучэнні NaНХO3 роўная 30,77 %.
Самакантроль
1. Не з’яўляецца злучэннем генетычнага раду магнію:
- а) МnO;
- б) Мg(OH)2;
- в) MgSO4;
- г) MgO.
2. Дзеяннем вады можна ажыццявіць ператварэнні:
- а) СаO → Сa(OH)2;
- б) Р2О5 → Н3РO4;
- в) SiO2 → H2SiO3;
- г) ZnO → Zn(OH)2.
3. Прадуктамі ўзаемадзеяння металу і неметалу з’яўляюцца злучэнні:
- а) К2S;
- б) AlCl3;
- в) SO3;
- г) MgBr2.
4. Прадукт ператварэння SO3 утварае солі, рэагуючы з рэчывамі:
- а) МgO;
- б) Fe(OH)2;
- в) S;
- г) Na2SiO3.
5. Масавая доля кіслароду ў сульфаце, атрыманым у ператварэнні Х → ВаО → Ba(ОH)2 → ХSO4, роўная:
- а) 6,9 %;
- б) 13,7 %;
- в) 27,5 %;
- г) 72,5 %.