§ 48. Алюминий и его соединения
Алюминий как химический элемент

Алюминий — элемент 3-го периода, IIIA-группы. Электронная схема, формула электронной конфигурации и электронно-графическая схема его атома имеют вид:
13Al ![]() или 13Аl 2е–, 8е–, 3е–;
или 13Аl 2е–, 8е–, 3е–;
13Аl 1s22s22p63s23p1 или 13Аl [Ne]3s23p1;
13Al 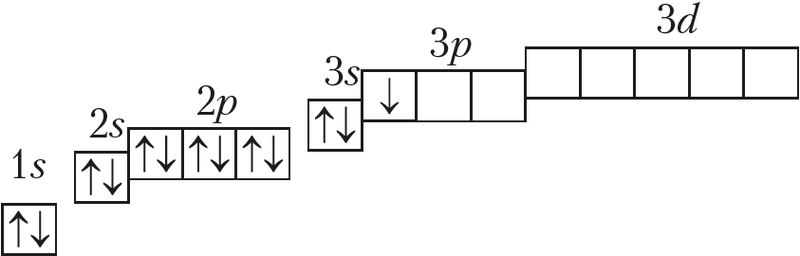
На внешнем электронном слое у атомов алюминия имеется 3 электрона, конфигурация валентного слоя 3s23p1, то есть алюминий относится к р-элементам. Он имеет низкое значение электроотрицательности χ(Al) = 1,6 и проявляет в соединениях степень окисления только +3.
Алюминий — самый распространённый металл земной коры (ω(Al) = 7,5 %, (§ 43, рис. 102)). В природе он представлен единственным нуклидом .
Вследствие значительной химической активности алюминий в природных условиях находится преимущественно в виде химических соединений — минералов, представляющих собой оксиды, гидроксиды, силикаты или алюмосиликаты. Например, продукт разрушения горных пород — глина (каолинит), продукты дальнейшего разрушения глины — бокситы Al2O3 · xH2O. Наибольшее практическое значение для получения алюминия имеют бокситы и криолит Na3[AlF6].