§ 39. Кислородсодержащие соединения фосфора
| Сайт: | Профильное обучение |
| Курс: | Химия. 11 класс |
| Книга: | § 39. Кислородсодержащие соединения фосфора |
| Напечатано:: | Гость |
| Дата: | Суббота, 19 Июль 2025, 02:41 |
К наиболее значимым кислородсодержащим соединениям фосфора относят оксид фосфора(V), фосфорную кислоту и её соли.
Оксиды фосфора
Взаимодействие кислорода с фосфором приводит к образованию оксидов, состав которых зависит от условий проведения реакции.
При сжигании фосфора в чистом кислороде, как указано на с. 201, получается оксид фосфора(V) P2O5, а при недостатке кислорода — оксид фосфора(III) P2O3.
Белый фосфор являлся одним из первых дымообразующих веществ, при сжигании которого во время военных действий образовывалась дымовая завеса из частиц P2O5. Дым — дисперсная система, состоящая из твёрдых взвешенных частиц в газовой среде.
Оксид фосфора(V) считают самым эффективным осушителем. Причём осушителем является и образующаяся при этом кислота. Обращаться с P2O5 следует крайне осторожно, так как при попадании на кожу оксид вызывает сильнейшие ожоги, одна из причин — обезвоживание тканей.
Оксид фосфора(V) — высший оксид фосфора, и ему соответствует гидроксид
— фосфорная (или ортофосфорная) кислота.
P2O5 — белое твёрдое вещество (Tпл. = 420 °С). Является типичным кислотным оксидом: реагирует с водой (1), основными оксидами (2) и щелочами (3), широко используется в органическом синтезе. Рассмотрим особенности этих реакций:
1. Конечным продуктом реакции оксида фосфора(V) с водой является фосфорная кислота H3PO4:
3H2O + P2O5 = 2H3PO4.
Оксид фосфора(V) не только растворяется в воде, но и «жадно» поглощает пары воды из воздуха, то есть гигроскопичен, используется в качестве осушителя.
2. Взаимодействие с основными и амфотерными оксидами приводит к образованию солей:
3СаО + P2O5 = Са3(РО4)2;
3ZnО + P2O5 = Zn3(РО4)2.
3. При растворении P2O5 в щелочах могут образовываться как средние, так и кислые соли (в зависимости от соотношения реагентов). Например, при взаимодействии с гидроксидом натрия могут образоваться Na3PO4, Na2HPO4 или NaH2PO4:
P2O5 + 6NaOH = 2Na3PO4 + 3H2O;
P2O5 + 4NaOH = 2Na2HPO4 + H2O;
P2O5 + 2NaOH + H2O = 2NaH2PO4.
Фосфорная кислота
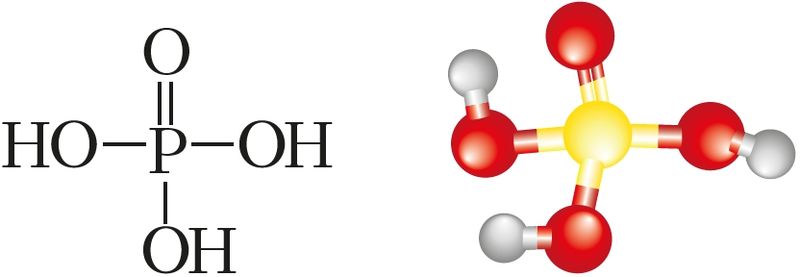
Химические и физические свойства. Фосфор образует несколько кислот, однако самой устойчивой является фосфорная кислота H3PO4 (рис. 96). Из структурной формулы её молекулы видно, что кислота трёхосновна. H3PO4 — вещество, температура плавления которого 42,35 °С. Это означает, что при комнатной температуре фосфорная кислота — твёрдое вещество. Фосфорная кислота хорошо растворима в воде. В водном растворе диссоциирует ступенчато:
Фосфорная кислота — слабый электролит, диссоциирует преимущественно по первой ступени. В растворах она проявляет общие свойства кислот: меняет цвет индикаторов и образует соли в реакциях с металлами, находящимися в ряду активности до водорода (1), основными и амфотерными оксидами (2), гидроксидами металлов и аммиаком (3), другими солями (4); она не является окислителем за счёт аниона:
Отметим, что фосфорная кислота образует как средние соли (фосфаты), так и кислые (гидрофосфаты и дигидрофосфаты), в зависимости от соотношения исходных веществ. Например:
3КOH + H3PO4 = К3PO4 + 3H2O (фосфат калия) (3 : 1);
2КOH + H3PO4 = К2HPO4 + 2H2O (гидрофосфат калия) (2 : 1);
КOH + H3PO4 = КН2PO4 + H2O (дигидрофосфат калия) (1 : 1).
При составлении уравнений реакций в ионной форме фосфорную кислоту представляют в виде молекул как преобладающих частиц в её растворе. Например:
Применение и получение. Фосфорную кислоту применяют в производстве удобрений и кормовых средств, для формирования антикоррозионных покрытий на металлах, а также в пищевой промышленности для придания кисловатого вкуса безалкогольным напиткам, для осветления сахара.
Получают H3PO4 взаимодействием природных фосфатов с серной кислотой при 60‒80 °С с последующим отфильтровыванием осадка СаSO4. При этом фосфорная кислота образуется в виде сиропообразного раствора с массовой долей вещества 85 %. Второй способ — сжигание фосфора, полученного прокаливанием природного фосфата с песком и углём, и последующее растворение оксида в воде:
Сa3(PO4)2 → Р → P2O5 → H3PO4.
Соли фосфорной кислоты. Фосфаты, как правило, нерастворимы, за исключением солей натрия, калия и аммония. Кислые соли более растворимы, чем средние, а дигидрофосфаты имеют большую растворимость, чем гидрофосфаты. Например, фосфат Ca3(PO4)2 нерастворим, гидрофосфат CaHPO4 — мало растворим, а дигидрофосфат Ca(H2PO4)2 — хорошо растворим в воде.
Большинство фосфатов обладает высокой термической устойчивостью — не разрушаются при нагревании до температуры плавления. Характерной особенностью фосфатов (средних солей) является образование осадка жёлтого цвета при действии раствора нитрата серебра(I) (Приложение 3):
В отличие от светло-жёлтого осадка бромида серебра(I) и жёлтого осадка йодида серебра(I), фосфат серебра(I) растворяется при добавлении азотной кислоты.
Применение солей фосфорной кислоты. Многие средние и кислые соли фосфорной кислоты (Ca3(PO4)2, CaHPO4 · 2H2O, Ca(H2PO4)2 · H2O, NН4H2PO4, (NН4)2HPO4) используются в качестве удобрений. Фосфаты находят применение в производстве каучука, пластмасс, в металлургии. Фосфат натрия уменьшает жёсткость воды и улучшает моющее действие стиральных порошков. Тем не менее во многих государствах в настоящее время установлены ограничения по применению фосфатов в качестве стиральных моющих средств. Дело в том, что после стирки фосфаты попадают в сточные воды, а затем в водоёмы, способствуя бурному развитию планктона и водорослей — водоёмы «стареют». По некоторым данным, 1 г фосфата стимулирует рост 5–10 кг водорослей.
Оксид фосфора(V) — кислотный оксид.
Фосфорная кислота, в отличие от азотной, является при н. у. твёрдым веществом, относится к слабым кислотам и окислительные свойства проявляет только за счёт атомов водорода.
Соли фосфорной кислоты — фосфаты, гидрофосфаты и дигидрофосфаты — находят широкое применение в качестве удобрений.
Вопросы, задания, задачи
1. Назовите классы веществ, с которыми взаимодействует:
- а) оксид фосфора(V);
- б) фосфорная кислота.
2. Составьте формулы:
- а) дигидрофосфата калия; дигидрофосфата кальция; гидрофосфата магния; фосфата железа(III);
- б) дигидрофосфата магния; гидрофосфата железа(III); гидрофосфата цинка; фосфата натрия.
Запишите уравнения их электролитической диссоциации, учитывая отщепление только ионов металла.
3. Запишите три уравнения последовательных реакций, происходящих при добавлении раствора:
- а) гидроксида калия к раствору фосфорной кислоты;
- б) фосфорной кислоты к раствору гидроксида натрия.
Назовите образующиеся соли.
4. Составьте уравнения реакций с учётом указанных коэффициентов:
- а)
;
- б)
.
5. Определите количество теплоты, которая выделяется при сгорании фосфора массой 1 кг по термохимическому уравнению реакции:
4Р(тв) + 5О2(г) = 2Р2О5(тв) + 3010 кДж.
6. Можно ли в качестве осушителя газообразного аммиака применять P2O5? Ответ аргументируйте.
7. В трёх пронумерованных пробирках находятся растворы нитрата калия, фосфата калия, хлорида натрия. Предложите план распознавания веществ. Поясните уравнениями реакций в молекулярной и ионной формах.
8. Составьте уравнения реакций согласно схеме:
- а)
;
- б)
.
9. Необходимо приготовить раствор фосфорной кислоты массой 500 г с массовой долей вещества 5 %. Рассчитайте массы необходимых для этой цели оксида фосфора(V) и воды.
10. Рассчитайте объём воздуха (н. у.), который необходим для сжигания фосфора массой 1 кг. Чему равна масса фосфорной кислоты, образующейся при растворении полученного оксида фоcфора(V)?
*Самоконтроль
1. Оксид фосфора P2O5 является:
- а) солеобразующим;
- б) восстановителем;
- в) жидким при н. у.;
- г) кислотным.
2. Для фосфорной кислоты справедливы утверждения:
- а) сильная двухосновная кислота;
- б) в водных растворах — слабый электролит;
- в) образует три вида солей — фосфаты, гидро- и дигидрофосфаты;
- г) H3PO4 соответствует оксиду фосфора(III).
3. Осадок жёлтого цвета с нитратом серебра(I) образуют растворы:
- a) Nа3РO4;
- б) K3PO4;
- в) KI;
- г) NaNO3.
4. Правильно составлены формулы солей фосфорной кислоты:
- а) Nа2РO4;
- б) (NH4)2НРO4;
- в) Zn2(РO4)3;
- г) Al(Н2РO4)3.
5. При мольном соотношении аммиака и оксида фосфора(V) 2 : 1 в водном растворе образуется:
- а) фосфат аммония;
- б) нитрат фосфора;
- в) гидрофосфат аммония;
- г) дигидрофосфат аммония.