§ 35. Серная кислота
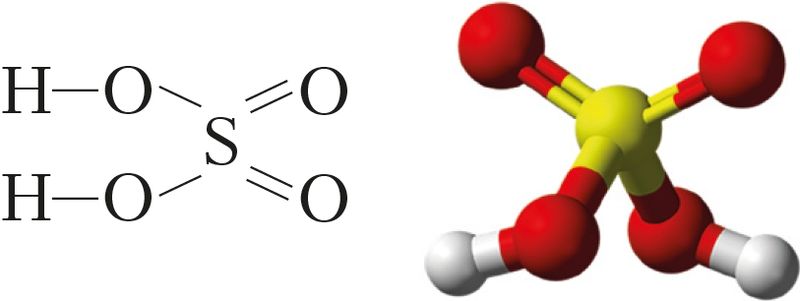
Серная кислота Н2SO4 — важнейшая из минеральных кислот.
Это вещество молекулярного строения. Из структурной формулы видно, что серная кислота является гидроксидом и относится к двухосновным кислотам (рис. 83).
Промышленное получение серной кислоты — многостадийный процесс, сырьё для него — это пирит (железный или серный колчедан) FeS2 и другие сульфидные руды, сера S, сероводород H2S (из нефти), отходы металлургического производства. Схема получения кислоты из пирита выглядит так:
Как видно, процесс включает три стадии, выражаемые следующими уравнениями реакций:
На третьей стадии оксид серы(VI) SO3 в поглотительной башне орошается концентрированной серной кислотой с массовой долей кислоты 96–98 % (то есть содержание воды всего 2–4 %). При этом получают раствор оксида серы(VI) в серной кислоте (олеум). Воду для поглощения SO3 не используют, так как из-за выделения большого количества теплоты образуется «сернокислотный туман», который трудно сконденсировать.
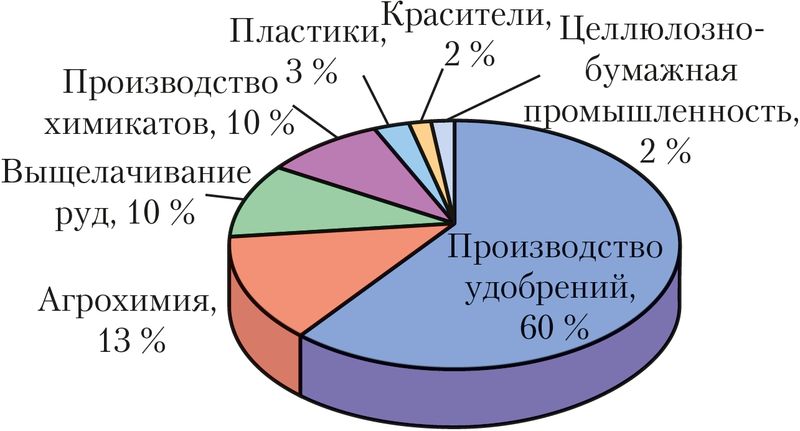
Мировое производство серной кислоты — около 200 млн тонн в год. Самый крупный потребитель серной кислоты — производство минеральных удобрений. Кроме того, она используется для получения различных минеральных кислот и солей, химических волокон, красителей, взрывчатых веществ, в промышленном органическом синтезе, в нефтяной, металлообрабатывающей, текстильной, кожевенной, пищевой и других отраслях промышленности (рис. 84), как электролит в свинцовых аккумуляторах (рис. 85).