§ 26. Понятие о водородном показателе (рН) раствора
Вода является слабым электролитом и только в небольшой степени диссоциирует на ионы Н+ и ОН–:
При 25 °С степень диссоциации α воды равна примерно 2 ∙ 10–9. Это означает, что из миллиарда молекул воды только две молекулы находятся в виде ионов Н+ и ОН–.
Концентрация ионов водорода с(Н+) равна 10–7 моль/дм3. Такова же концентрация гидроксильных групп с(ОН–).
Произведение концентраций ионов Н+ и OH– в воде и водных растворах является величиной постоянной при определённой температуре. Так, при 25 °C:
Растворы, в которых концентрация катионов водорода равна концентрации гидроксид-анионов, называют нейтральными. Если концентрация катионов водорода в растворе больше концентрации гидроксид-анионов, то есть c(Н+) > c(ОН–), то среда раствора кислая. Если же в растворе преобладают гидроксид-анионы, то есть c(ОН–) > c(Н+), то среда раствора щелочная.
Количественно кислотность и связанную с ней осно́вность (щёлочность) среды растворов выражают с помощью водородного показателя рH (читается «пэ-аш»). Водородный показатель представляет собой десятичный логарифм концентрации ионов водорода в растворе, взятый со знаком «минус»:
рH = –lgc(H+).
Водородный показатель pH — это мера концентрации в растворе катионов водорода H+, количественно выражающая кислотность раствора.
Водородный показатель является безразмерной величиной.
Например, при молярной концентрации катионов H+ c(H+) = 10–5 моль/дм3 рН равен 5, а при c(H+) = 10–3 моль/дм3 рН равен 3.
Пример 1. Определите рН раствора серной кислоты, молярная концентрация которой равна 0,005 моль/дм3.
Дано:
с(H2SO4) = 0,005 моль/дм3
pH — ?
Решение
Пусть V(р-ра) = 1 дм3.
Тогда
n(H2SO4) = 0,005 моль/дм3 · 1 дм3 = 0,005 моль.
Определим количество ионов водорода по уравнению диссоциации кислоты:
, откуда х = 0,01 моль, то есть n(Н+) = 0,01 моль.
Молярная концентрация ионов водорода равна:
Рассчитаем водородный показатель:
рН = –lgс(Н+) = –lg10–2 = 2.
Ответ: рН = 2.
Рассчитаем водородный показатель в щелочном растворе.
Пример 2. Определите pH раствора NaOH c молярной концентрацией 0,01 моль/дм3.
Дано:
с(NaOH) = 0,01 моль/дм3
pH — ?
Решение
Концентрация анионов OH– в таком растворе равна 10–2 моль/дм3. Рассчитаем концентрацию ионов водорода, зная, что с(Н+) ∙ с(ОН)– = 10–14 (моль/дм3)2., откуда
следовательно,
рН = –lgc(H+) = –lg10–12 = 12 (щелочная среда).
Ответ: рН = 12.
Обратите внимание на то, что и в щелочной среде катионы H+ продолжают присутствовать в водном растворе.
Поскольку в воде при 20–25 °С концентрации ионов H+ и OH– одинаковы и равны 10–7 моль/дм3, то для чистой воды рН = –lgc(H+) = –lg10–7 = 7. Такое значение рН соответствует нейтральной среде. Значению рН < 7 соответствует бо́льшая кислотность раствора, а рН > 7 соответствует бо́льшая щёлочность раствора (рис. 59).
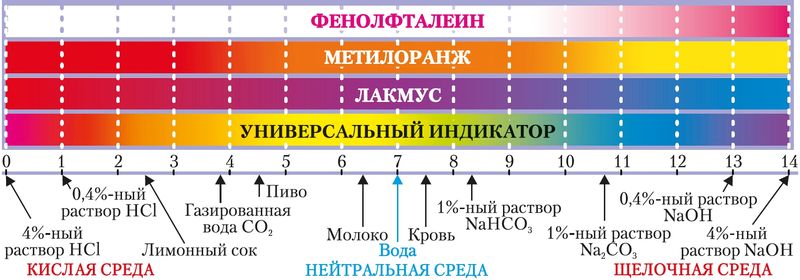
Итак, значение рН можно рассчитать, а также оценить с помощью отдельных индикаторов (лакмуса, фенолфталеина, метилоранжа), универсального индикатора cо шкалой рН и приборов — рН-метров (рис. 59, 60).

Измерение рН необходимо в медицине, сельском хозяйстве, науке, на производстве. В организме здорового человека рН крови составляет 7,4, желудочного сока — 1,7, слюны — 6,9, слёз — 7,3–7,5. При консервировании добавление уксусной кислоты в маринад до pH < 4,5 подавляет деятельность большинства бактерий. С аналогичной целью в состав прохладительных напитков вводят лимонную кислоту для понижения значения рН до 3. Для нормального развития растений чаще всего необходимо уменьшать повышенную кислотность почв известкованием с помощью мела CaCO3, доломитовой муки CaMg(CO3)2 или некоторых удобрений до рН = 6,0–6,5 (табл. 16).
Таблица 16. Классификация диапазонов рH почвы
| Кислотность почвы | Диапазон рH |
| Кислая | 3,5–6,0 |
| Нейтральная и близкая к нейтральной | 6,1–7,8 |
| Щелочная | 7,9–9,0 и выше |