§ 25. Электролитическая диссоциация веществ в растворах

Аррениус —
шведский физико-
химик, автор теории
электролитической
диссоциации (1887 г.)
К началу XIX века естествоиспытатели установили, что все растворы можно разделить на две большие группы — непроводящие электрический ток и проводящие его. Немецкий физик Г. С. Ом выявил, что растворы-проводники проводят ток по тем же законам, что и металлы-проводники. Английский физик М. Фарадей изучил явление электролиза и установил его основные законы. Наблюдаемые в растворах явления и закономерности в 1887 году объяснил шведский учёный Сванте Аррениус, предложивший теорию электролитической диссоциации. Её сущность можно выразить следующим образом:
электролиты распадаются на ионы в расплавах под действием высокой температуры, а в растворах вследствие взаимодействия с растворителем (рис. 56).
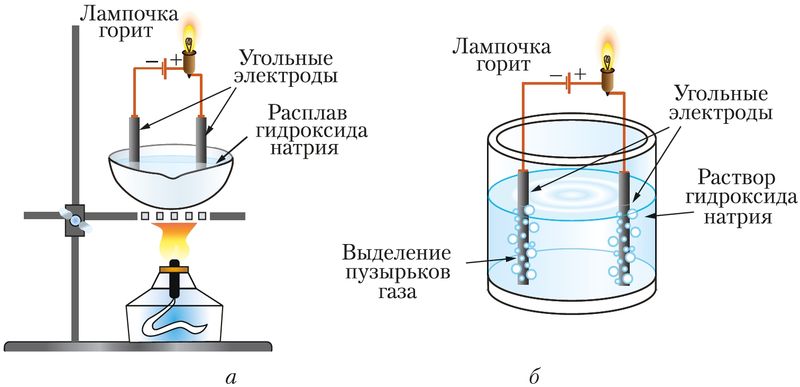
Процесс распада электролита на ионы называют электролитической диссоциацией.
В твёрдом состоянии большинство ионных и молекулярных соединений — это диэлектрики, не проводящие ток. Так, электропроводность твёрдого NaCl в 1000 млрд раз меньше, чем у металлов или графита. В то же время водные растворы электролитов проводят ток вследствие того, что ионные и многие молекулярные соединения под влиянием полярных молекул воды при растворении распадаются (диссоциируют) на катионы и анионы.
Электролит — это вещество, которое проводит электрический ток вследствие диссоциации на катионы и анионы в расплаве или в растворе.
Электропроводность электролитов обусловлена подвижностью катионов и анионов в расплавах и растворах.
К электролитам относятся соли, щёлочи, кислоты, то есть соединения с ионной или ковалентной полярной химической связью.