§ 3.5. Взаимосвязь между классами неорганических соединений
Многообразие неорганических соединений наиболее логично отражают так называемые генетические ряды, которые содержат соединения одного элемента, принадлежащие различным классам. Как правило, такой ряд представлен элементом, его оксидом, гидроксидом и соответствующей солью. Например, генетический ряд типичного металла и генетический ряд неметалла выглядят так:
| Металл | → | основный оксид | → | гидроксид (основание) | → | соль |
| Са | → | СаО | → | Са(ОН)2 | → | Са(NO3)2 |
| Неметалл | → | кислотный оксид | → | гидроксид (кислота) | → | соль |
| S | → | SO2 | → | Н2SO3 | → | Na2SO3 |
Стрелка (→) в данных схемах означает «соответствует». Так, типичному металлу соответствуют основный оксид, гидроксид, соль, в частности Са — оксид СаО, гидроксид Са(ОН)2, соль Са(NO3)2.
Свойства соединений металлов и неметаллов по своей сути противоположны, поэтому вещества разных генетических рядов могут взаимодействовать друг с другом, образуя преимущественно соли. Некоторые варианты таких попарных взаимодействий могут быть отражены схемами на основе генетических рядов, из которых видно, что продуктами взаимодействия веществ разных генетических рядов являются, в основном, соли (рис. 6.5, 6.6).
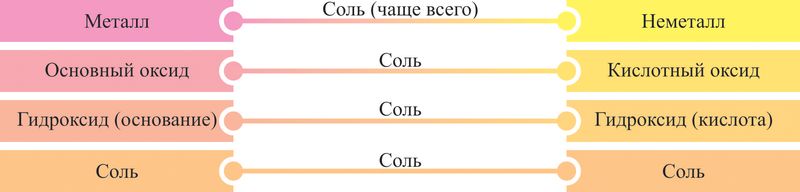
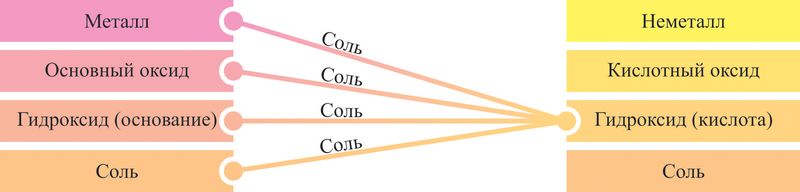
При взаимодействии металлов и неметаллов образуются как соли (галогениды, сульфиды — NaCl, Al2S3), так и бинарные соединения, не относящиеся к классу солей (нитриды, фосфиды, карбиды, гидриды, оксиды — Li3N, Ca3P2, Al4C3, NaH, CaO).
Генетические ряды в органической химии образуют соединения, содержащие одинаковое число атомов углерода:
С3Н8 → С3Н7Сl → С3Н7ОН → C2H5СНО → C2H5СОOH → CH3CH(Cl)СОOH → CH3CH(NH2)СОOH → NH—CH(CH3)CO
Знание особенностей каждого вида взаимодействий необходимо при выполнении различных заданий и решении экспериментальных задач. В практической деятельности химики получают новые вещества из имеющихся в их распоряжении: например, серную кислоту — из серного колчедана, аммиак — из азота, азотную кислоту — из аммиака, цинк — из цинковой обманки и т. д. При этом, как правило, необходимо провести серию реакций, чтобы получить нужный продукт. Например, один из вариантов получения цинка из природного минерала ZnS можно представить схемой превращений:
ZnS → ZnO → Zn,
для осуществления которых необходимы реакции:
1) окисления сульфида цинка кислородом (обжиг):
2ZnS + 3O2 = 2ZnO + 2SO2;
2) восстановления металла из оксида:
ZnO + С = СО + Zn.
На выбор пути превращений и разработку технологических процессов влияют знание свойств веществ, учёт доступности реагентов, безопасности процессов и многие другие факторы.
В качестве примера рассмотрим превращение веществ одного генетического ряда — основного оксида в гидроксид.
Пример 1. Составьте уравнение реакции, позволяющей получить щёлочь из основного оксида: СаО → Са(ОН)2.
Решение
Так как кальций — активный металл, то его оксид реагирует с водой, образуя щёлочь:
CaO + H2O = Ca(OH)2 (взаимодействие активного металла с водой).
Пример 2. Составьте уравнения реакций, позволяющих получить нерастворимое основание из основного оксида: FeO → Fe(OH)2.
Решение
Так как Fe(OH)2 — нерастворимое основание, то его можно получить лишь из раствора соли. Значит, исходный оксид FeO необходимо первоначально перевести в растворимую соль:
FeO + Н2SO4 = FeSO4 + H2O (растворение оксида в кислоте, получение растворимой соли).
Затем к раствору соли необходимо добавить раствор щёлочи:
FeSO4 + 2NaOH → Fe(OH)2↓ + NaSO4 (получение нерастворимого основания взаимодействием растворов соли и щёлочи).
Таким образом, выбор реагентов зависит от того, чем является продукт превращения — гидроксид металла: щёлочью или нерастворимым основанием. Для получения щёлочи из оксида достаточно иметь воду, а нерастворимое основание можно получить только из раствора соли. Поэтому оксид необходимо предварительно превратить в растворимую соль, а затем добавить раствор щёлочи.