§ 47. Амінакіслоты
| Сайт: | Профильное обучение |
| Курс: | Хімія. 10 клас |
| Книга: | § 47. Амінакіслоты |
| Напечатано:: | Гость |
| Дата: | Пятница, 4 Июль 2025, 11:39 |
Амінакіслоты
У малекулах амінакіслот змяшчаюцца адначасова амінагрупа ![]() NH2 і карбаксільная група
NH2 і карбаксільная група ![]() COOH. Паспрабуем сканструяваць такую малекулу. Для гэтага да атама вугляроду далучым карбаксільную групу і амінагрупу:
COOH. Паспрабуем сканструяваць такую малекулу. Для гэтага да атама вугляроду далучым карбаксільную групу і амінагрупу:
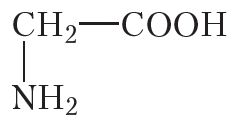
Атрымалася найпрасцейшая амінакіслата — амінавоцатная, або гліцын. Бліжэйшым гамолагам гліцыну з’яўляецца амінакіслата аланін:
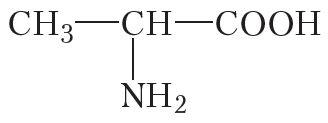
Наменклатура амінакіслот
Назвы амінакіслот складаюцца з назвы адпаведнай карбонавай кіслаты з прыстаўкай аміна-, перад якой указана становішча амінагрупы:

Часам пры пабудове назваў амінакіслот становішча амінагрупы абазначаюць не лічбамі, а літарамі грэчаскага алфавіту:

Некаторыя амінакіслоты маюць трывіяльныя назвы, напрыклад, амінаэтанавая кіслата называецца гліцын, а 2-амінапрапанавая — аланін.
Фізічныя ўласцівасці амінакіслот
Амінакіслоты — бясколерныя крышталічныя рэчывы, добра растваральныя ў вадзе, многія з іх маюць салодкі смак. Тэмпературы плаўлення амінакіслот дастаткова высокія, так, tпл амінавоцатнай кіслаты роўна 233 °С. Гэта ўказвае на тое, што паміж малекуламі амінакіслот ёсць вельмі моцнае ўзаемадзеянне.
Хімічныя ўласцівасці амінакіслот
Малекулы амінакіслот змяшчаюць адначасова амінагрупу ![]() NH2 і карбаксільную групу
NH2 і карбаксільную групу ![]() COOH, таму для іх характэрны ўласцівасці як амінаў, так і карбонавых кіслот.
COOH, таму для іх характэрны ўласцівасці як амінаў, так і карбонавых кіслот.
1. Узаемадзеянне з кіслотамі
Падобна амінам, амінакіслоты ўтвараюць солі пры ўзаемадзеянні з кіслотамі:
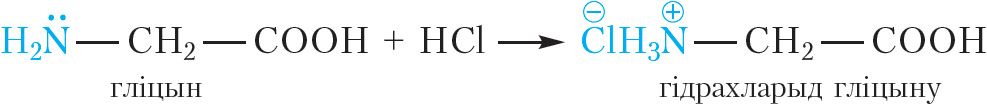
Цікава ведаць
Часта ў інструкцыях па прымяненню лекаў, набытых у аптэцы, можна прачытаць доўгую назву дзеючага рэчыва лекаў і прыпіску «гідрахларыд». Што гэта значыць? Малекулы многіх лекавых прэпаратаў змяшчаюць амінагрупы, якія лёгка акісляюцца нават кіслародам паветра. Калі ж амінагрупу перавесці ў солевую форму, яна будзе намнога больш устойлівай да акіслення, пры гэтым, як правіла, павялічваецца растваральнасць лекавага прэпарата. На практыцы нейтралізацыя амінагруп ажыццяўляецца ўзаемадзеяннем з хлоравадародам HCl. Адсюль і назва «гідрахларыд».
2. Узаемадзеянне са шчолачамі
Падобна карбонавым кіслотам, амінакіслоты рэагуюць са шчолачамі з утварэннем солей:

Такім чынам, амінакіслоты ўтвараюць солі і з кіслотамі, і са шчолачамі. Гэта значыць амінакіслоты з’яўляюцца амфатэрнымі арганічнымі злучэннямі.
Растворы амінакіслот не змяняюць афарбоўку індыкатараў. Гэта тлумачыцца тым, што аміна- і карбаксільная групы ў амінакіслотах нейтралізуюць адна адну.
3. Утварэнне складаных эфіраў
Як і карбонавыя кіслоты, амінакіслоты ўтвараюць складаныя эфіры пры ўзаемадзеянні са спіртамі. Каталізатарамі дадзенай рэакцыі з’яўляюцца неарганічныя кіслоты (напрыклад, HCl):
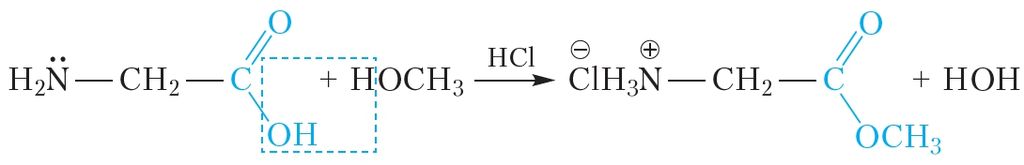
Звярніце ўвагу, што ў ходзе рэакцыі HCl не толькі выконвае ролю каталізатара, але і ўзаемадзейнічае з амінагрупай, утвараючы соль.
4. Утварэнне пептыдаў
Пры пэўных умовах малекулы амінакіслот могуць рэагаваць адна з адной:
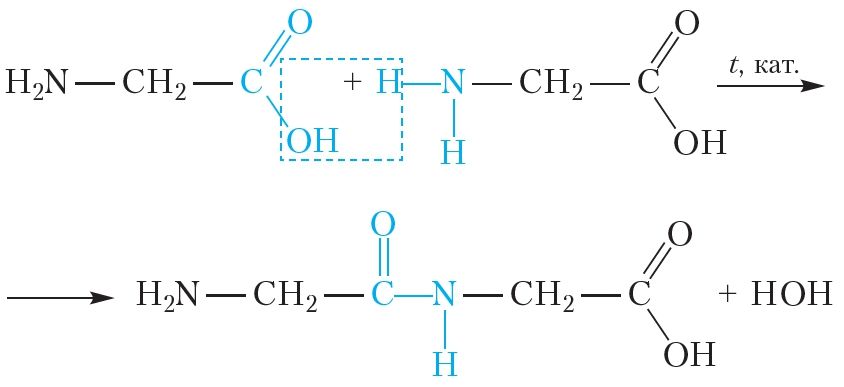
У ходзе рэакцыі ад карбаксільнай групы адной малекулы амінакіслаты адшчапляецца група ![]() OH, а ад амінагрупы другой малекулы — атам вадароду. У выніку фарміруецца кавалентная сувязь паміж двума амінакіслотнымі астаткамі і ўтвараецца малекула вады. Група атамаў
OH, а ад амінагрупы другой малекулы — атам вадароду. У выніку фарміруецца кавалентная сувязь паміж двума амінакіслотнымі астаткамі і ўтвараецца малекула вады. Група атамаў 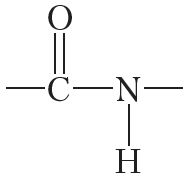 называецца пептыднай, або аміднай, групай, а сувязь паміж амінакіслотнымі астаткамі — пептыднай, або аміднай, сувяззю.
называецца пептыднай, або аміднай, групай, а сувязь паміж амінакіслотнымі астаткамі — пептыднай, або аміднай, сувяззю.
Пры ўзаемадзеянні дзвюх малекул амінакіслот утвараецца дыпептыд. Дыпептыд можа ўзаемадзейнічаць з наступнай малекулай амінакіслаты з утварэннем трыпептыду і г. д.
Атрыманне амінакіслот
α-Амінакіслоты могуць быць атрыманы з адпаведных карбонавых кіслот. Для гэтага спачатку атам вадароду α-вугляроднага атама карбонавай кіслаты замяшчаюць на галаген (§ 33):
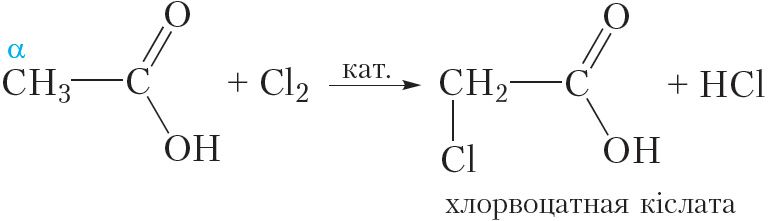
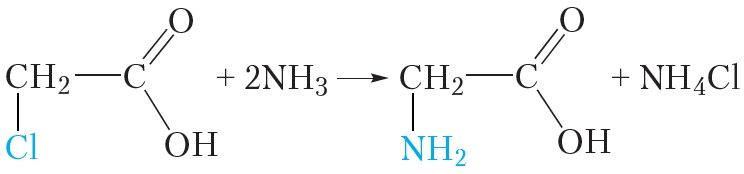
Потым атам галагену ў малекуле α-галагензамешчанай карбонавай кіслаты замяшчаюць амінагрупай:
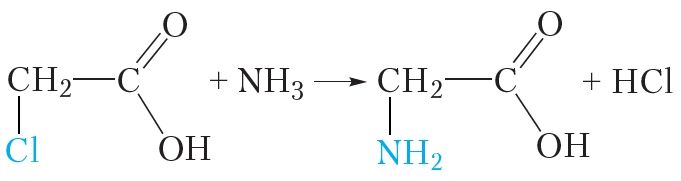
Хлоравадарод, які вылучаецца ў ходзе рэакцыі, узаемадзейнічае з малекуламі аміяку:
![]()
таму для рэакцыі з 1 моль хлорвоцатнай кіслаты патрабуецца 2 моль аміяку:
Прымяненне амінакіслот
У жывых арганізмах, у тым ліку ў арганізме чалавека, з амінакіслот утвараюцца бялкі. Некаторыя амінакіслоты выкарыстоўваюць у якасці лекавых сродкаў і харчовых дабавак. Амінакіслоты прымяняюцца для атрымання высокамалекулярных злучэнняў, з якіх вырабляюць валокны і пластмасы.
Разгледзім атрыманне сінтэтычнага валакна капрон. Утварэнне палімеру, з якога атрымліваюць валакно, можна прадставіць наступнай схемай:
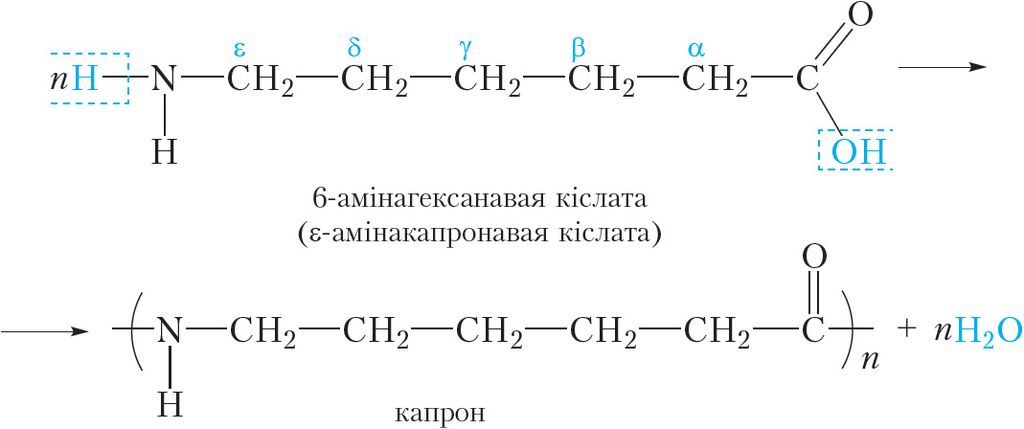
Астаткі 6-амінагексанавай кіслаты ў капроне звязаны аміднымі сувязямі, таму валакно капрон адносіцца да поліамідных. Паколькі макрамалекулы капрону атрымліваюць сінтэтычным шляхам, то капрон — сінтэтычнае валакно. У нашай краіне капрон атрымліваюць на філіяле «Завод Хімвалакно» ААТ «Гродна Азот». Яшчэ адным прыкладам сінтэтычных валокнаў з’яўляецца поліэфірнае валакно лаўсан (§ 38).
Аб сінтэтычным валакне нейлоне вы даведаецеся, перайшоўшы па спасылцы ў QR-кодзе.
Амінакіслоты — арганічныя злучэнні, малекулы якіх змяшчаюць амінагрупу ![]() NH2 і карбаксільную групу
NH2 і карбаксільную групу ![]() COOH.
COOH.
Для амінакіслот характэрны ўласцівасці як амінаў, так і карбонавых кіслот.
Амінакіслоты ўтвараюць солі пры ўзаемадзеянні і з кіслотамі, і са шчолачамі. Такім чынам, амінакіслоты — амфатэрныя арганічныя злучэнні.
Растворы амінакіслот не змяняюць афарбоўку індыкатараў, паколькі аміна- і карбаксільная групы ў амінакіслотах нейтралізуюць адна адну.
Малекулы амінакіслот могуць рэагаваць адна з адной, утвараючы пептыды.
Полікандэнсацыяй 6-амінагексанавай кіслаты атрымліваюць сінтэтычнае валакно капрон.
*Нейлон
Нейлон утвараецца ў выніку полікандэнсацыі гексаметылендыаміну (аміну, у малекуле якога маюцца дзве амінагрупы і шэсць метыленавых ![]() СН2
СН2 ![]() груп) з адыпінавай кіслатой, у малекуле якой дзве карбаксільныя і чатыры метыленавыя групы:
груп) з адыпінавай кіслатой, у малекуле якой дзве карбаксільныя і чатыры метыленавыя групы:
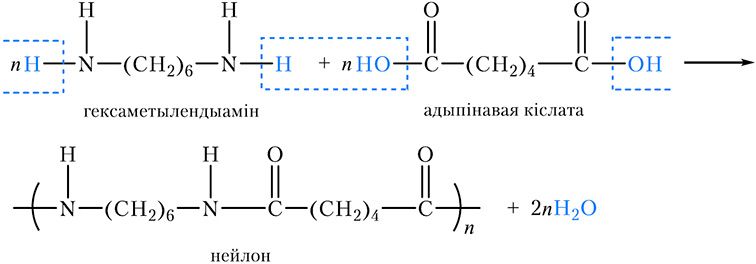
З нейлону вырабляюць валокны, якія характарызуюцца высокай трываласцю і зносастойкасцю.
Пытанні і заданні
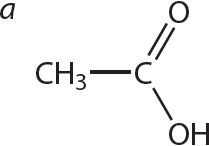
1. Арганічнае рэчыва А ўтварае солі пры ўзаемадзеянні і з кіслотамі, і са шчолачамі. Укажыце формулу рэчыва А.
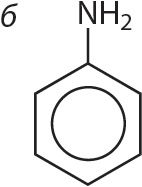
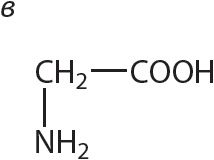
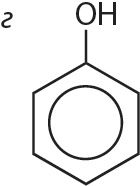
2. Прывядзіце ўраўненні рэакцый аланіну: а) з салянай кіслатой; б) з растворам гідраксіду натрыю.
3. Напішыце структурную формулу дыпептыду, утворанага астаткамі аланіну.
4. Напішыце ўраўненні рэакцый, якія адпавядаюць наступнай схеме ператварэнняў:
ацэтылен (1 моль) ![]()
5. Колькі розных дыпептыдаў будзе атрымана пры награванні сумесі гліцыну і аланіну? Прывядзіце формулы гэтых дыпептыдаў.
6. Колькі амінакіслотных астаткаў і пептыдных сувязей змяшчаецца ў малекуле лінейнага (нецыклічнага) тэтрапептыду?
7. Прывядзіце ўраўненні рэакцый атрымання капрону, лаўсану, поліэтылену, сінтэтычнага каўчуку з адпаведных манамераў. Якія з прыведзеных вамі рэакцый з’яўляюцца рэакцыямі полімерызацыі, а якія — полікандэнсацыі?
8. Арганічнае рэчыва А змяшчае 11,97 % азоту, 9,40 % вадароду і 27,35 % кіслароду па масе і ўтвараецца пры ўзаемадзеянні арганічнага рэчыва B з прапанолам-1, насычаным хлоравадародам, і наступным выцясненнем з солі. Вядома, што рэчыва B мае прыроднае паходжанне і здольна ўзаемадзейнічаць як з кіслотамі, так і са шчолачамі.
а) Устанавіце малекулярную формулу рэчыва А.
б) Састаўце ўраўненні рэакцый, якія працякаюць.
9*. У выніку спальвання 3,045 г трыпептыду ў кіслародзе было атрымана 1,755 г вады, 4,620 г вуглякіслага газу і 504 см3 (н. у.) азоту. Устанавіце малекулярную формулу трыпептыду, калі вядома, што яго малекула змяшчае тры атамы азоту. Колькі ізамерных трыптыдаў адпавядае ўстаноўленай вамі малекулярнай формуле? Прывядзіце іх структурныя формулы. Улічвайце, што ў саставе трыпептыду змяшчаюцца астаткі толькі α-амінакіслот.
