§ 20. Химические свойства, получение и применение бензола
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 20. Химические свойства, получение и применение бензола |
| Напечатано:: | Гость |
| Дата: | Sunday, 19 October 2025, 04:43 |
Химические свойства бензола
Как вы уже знаете, в молекуле бензола имеется устойчивая сопряжённая система π-связей. Поэтому для бензола характерны реакции замещения, так как в этих реакциях сопряжённая система сохраняется. Наоборот, реакции присоединения для бензола малохарактерны. Так, бензол не обесцвечивает бромную воду, но в присутствии катализатора он вступает с бромом в реакцию замещения.
1. Галогенирование
Для осуществления этой реакции бензол смешивают с бромом в колбе и добавляют катализатор FeBr3. При этом протекает реакция замещения одного атома водорода на бром:
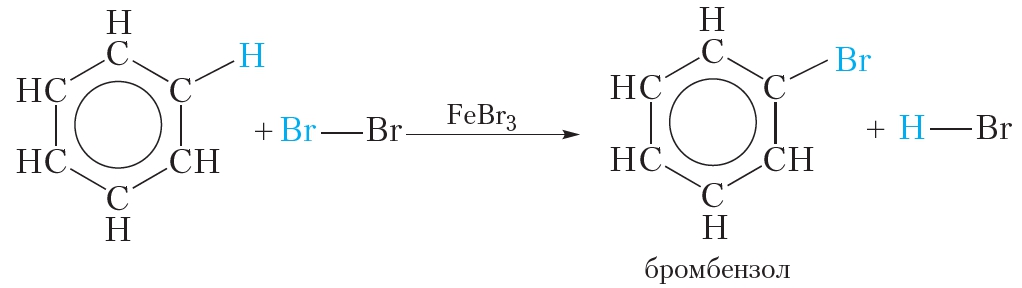
О протекании реакции можно судить по выделению бромоводорода, изменяющего цвет влажной индикаторной бумажки, помещённой в верхнюю часть колбы. Продукт бромирования бензола называется бромбензол.
Как видно, в этой реакции единая система π-электронов сохраняется. Подобным образом проводят и хлорирование бензола:
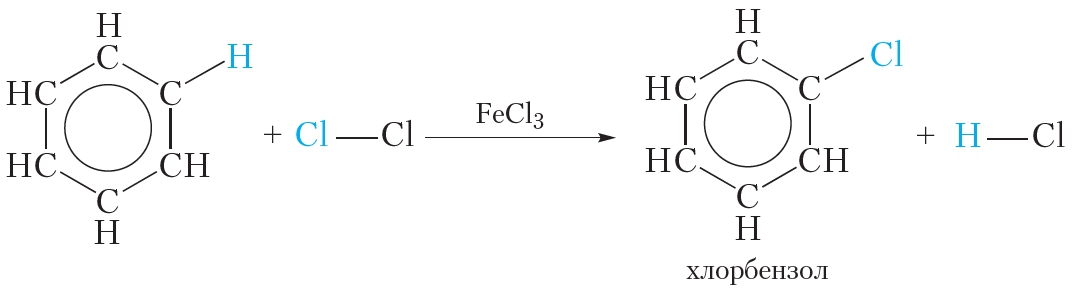
Так называются реакции, в результате которых в молекулу органического соединения вводится группа — NO2, называемая нитрогруппой.
Если к смеси концентрированных азотной и серной кислот прибавить бензол, происходит реакция нитрования бензола, в результате которой образуется тяжёлая желтоватая жидкость с запахом горького миндаля — нитробензол:
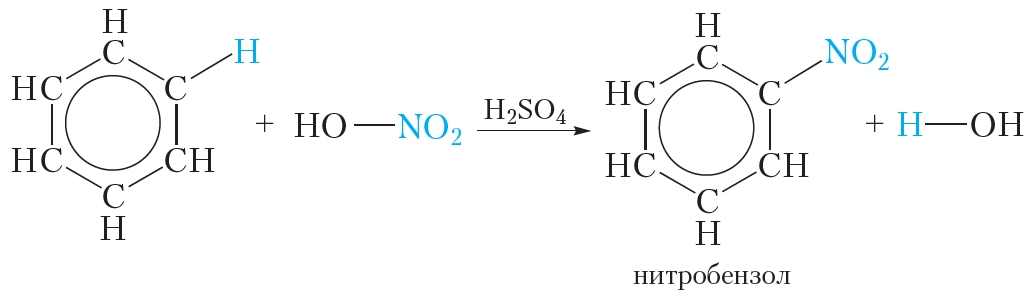
 Данная реакция так же, как и галогенирование, относится к реакциям замещения — один атом водорода в молекуле бензола замещается на группу — NO2.
Данная реакция так же, как и галогенирование, относится к реакциям замещения — один атом водорода в молекуле бензола замещается на группу — NO2.
Смесь концентрированных азотной и серной кислот называется нитрующей смесью. В нитрующей смеси азотная кислота выполняет роль нитрующего реагента, а серная кислота является катализатором.
С нитрованием гомолога бензола — толуола, продуктом которого является взрывчатое вещество, вы можете познакомиться, перейдя по ссылке в QR-коде.
3. Гидрирование
В жёстких условиях бензол может вступать в реакции присоединения. Примером реакции присоединения с участием бензола является его гидрирование, которое протекает при температуре около 200 °С под давлением в присутствии катализаторов гидрирования (никель или платина). При этом одна молекула бензола присоединяет сразу три молекулы водорода и превращается в циклогексан:
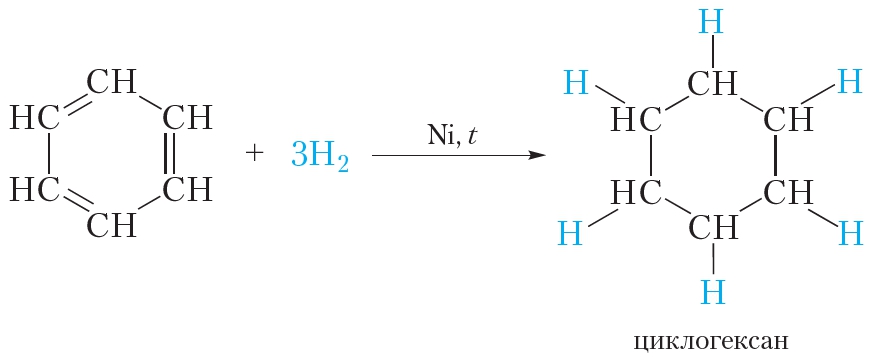
 Реакция гидрирования бензола протекает в более жёстких условиях, чем гидрирование алкенов, так как в молекуле бензола в ходе гидрирования разрушается устойчивая сопряжённая система π-связей.
Реакция гидрирования бензола протекает в более жёстких условиях, чем гидрирование алкенов, так как в молекуле бензола в ходе гидрирования разрушается устойчивая сопряжённая система π-связей.
С реакцией присоединения хлора к бензолу вы можете познакомиться, перейдя по ссылке в QR-коде.
4. Горение
Подобно всем углеводородам, бензол горит. Уравнение реакции горения бензола:Получение бензола
Из природных источников
Благодаря высокой устойчивости сопряжённой системы p-связей, ароматические фрагменты встречаются в составе каменного угля. Поэтому одним из способов получения бензола является переработка каменного угля. При сильном нагревании без доступа воздуха каменный уголь подвергается сложным химическим превращениям. В результате образуется много летучих продуктов, из которых, наряду с другими веществами, извлекают бензол.
Бензол получают также в результате переработки нефти. Эти процессы будут рассмотрены в следующем параграфе.
Из ацетилена
Бензол можно получить из ацетилена:
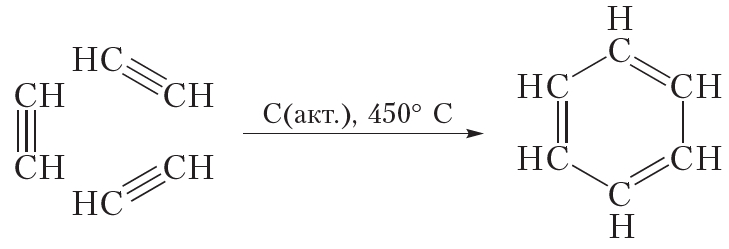
В данной реакции из трёх молекул ацетилена образуется одна циклическая молекула бензола, поэтому эта реакция называется реакцией циклотримеризации. Данная реакция протекает при пропускании ацетилена над нагретым активированным углём.
Применение бензола
Значительная часть бензола используется для синтеза других веществ. Так, нитрованием бензола получают нитробензол, который является исходным веществом для синтеза анилина (§ 45). Хлорированием бензола получают хлорбензол, который применяется для получения фенола (§ 27), пестицидов и т. д. Из бензола получают этилбензол. Дегидрированием этилбензола синтезируют винилбензол (стирол), который является сырьём для производства полимеров.
Бензол и некоторые его гомологи применяются в качестве растворителей органических веществ, однако из-за высокой токсичности бензола его применение в этом качестве ограниченно.
|
Для бензола характерны реакции замещения, в которых сопряжённая система π-связей сохраняется. Бензол не обесцвечивает бромную воду, но в присутствии катализатора вступает с бромом в реакцию замещения с образованием бромбензола. В жёстких условиях бензол вступает в реакцию присоединения с водородом. В результате образуется циклогексан. Бензол получают в результате переработки нефти и каменного угля. Кроме того, бензол может быть получен по реакции циклотримеризации ацетилена. |
*Нитрование толуола
Нитрование толуола
Примером нитросоединения с несколькими нитрогруппами в молекуле является продукт нитрования ближайшего гомолога бензола — толуола. При этом три атома водорода бензольного кольца замещаются на нитрогруппы:
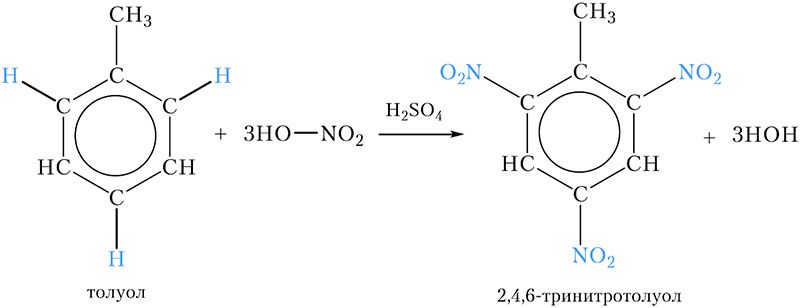
Название продукта — 2,4,6-тринитротолуол, его часто называют просто тринитротолуолом, ТНТ или тротилом. Тринитротолуол является взрывчатым веществом, которое используется в промышленности и военном деле.
*Хлорирование бензола
Хлорирование бензола
Молекула бензола может присоединить три молекулы хлора. Реакция протекает при нагревании и облучении ультрафиолетовым светом:
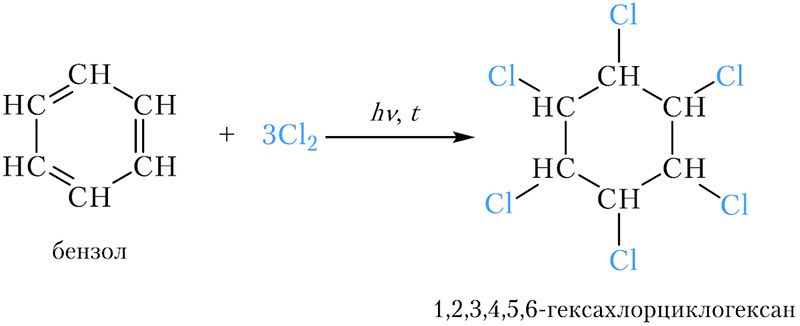
Образуется 1,2,3,4,5,6-гексахлорциклогексан, или гексахлоран. Это вещество долгое время использовалось в качестве инсектицида. Сейчас оно не применяется ввиду высокой токсичности.
Реакции гомологов бензола с участием боковой цепи
Гомологи бензола могут вступать в реакции замещения атомов водорода боковой цепи другими атомами. Используя это свойство, можно легко различить бензол и толуол. Для этого в две пробирки наливают по 2–3 см3 бензола и толуола соответственно, затем по 2–3 см3 бромной воды. Пробирки закрывают пробками и встряхивают. При этом бром из водной фазы за счёт лучшей растворимости в углеводородах переходит в органический слой, который находится сверху. При этом органический слой окрашивается в оранжевый цвет. Пробирки некоторое время интенсивно освещают. Через несколько минут можно наблюдать, что в одной из пробирок оранжевая окраска органического слоя сохранилась, тогда как во второй пробирке органический слой обесцветился. Обесцвечивание произошло в пробирке с толуолом за счёт протекания реакции замещения атома водорода метильной группы на атом брома:
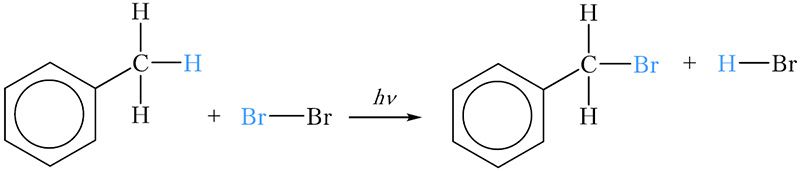
Образовавшееся бромпроизводное толуола не имеет окраски.
Эта реакция напоминает реакцию замещения атомов водорода в молекулах алканов атомами галогенов. Реакция протекает при освещении, это свидетельствует о радикальном механизме реакции замещения, инициируемой светом (§ 10).
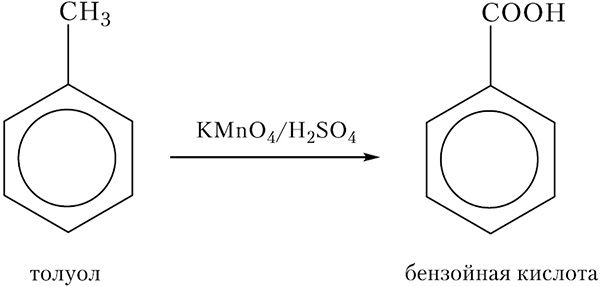
Атом углерода метильной группы в молекуле толуола легко окисляется, при этом образуется бензойная кислота. В качестве окислителя обычно используют раствор перманганата калия, подкисленный серной кислотой, либо хромовую смесь (раствор дихромата калия K2Cr2O7, подкисленный H2SO4). Схема реакции окисления толуола:
Вопросы и задания
1. Как распознать на основании химических свойств три жидкости: бензол, гексан и гексен-1? Приведите уравнения соответствующих реакций. Укажите условия их протекания. Опишите наблюдаемые явления.
2. Напишите уравнения реакций взаимодействия метана и бензола с хлором. Укажите условия их протекания. Почему обе реакции называются реакциями замещения?
3. Известно, что в присутствии платины этилен присоединяет водород даже при комнатной температуре. Бензол в этих условиях водород не присоединяет. Реакция присоединения водорода к бензолу протекает в жёстких условиях — при температуре 200 оС под давлением и в присутствии никеля в качестве катализатора. Объясните, с чем связано такое различие в реакционной способности этилена и бензола.
4. Приведите уравнение реакции циклотримеризации ацетилена в присутствии активированного угля. Какие продукты могут образоваться при циклотримеризации пропина в подобных условиях? Приведите их структурные формулы и дайте им названия.
5. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
![]()
6*. Напишите уравнение реакции нитрования толуола. Назовите продукт реакции. Где он используется?
7*. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
гептен-1 ![]() гептан
гептан ![]() толуол
толуол ![]() 2,4,6-тринитротолуол.
2,4,6-тринитротолуол.
8*. Напишите структурные формулы всех гомологов бензола состава С9Н12. Назовите их.
9*. Каково строение углеводорода состава С8Н8, обесцвечивающего бромную воду, легко полимеризующегося, а при окислении дающего бензойную кислоту? Напишите уравнения описанных реакций.
(Ответ: стирол.)
10*. Установите строение ароматического углеводорода состава С9Н12, при моногалогенировании которого в присутствии катализатора получается только одно галогенпроизводное.
(Ответ: 1,3,5-триметилбензол.)